向100mL含 、
、 、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
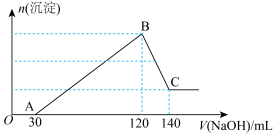
(1)写出OA段发生的离子方程式___________ ;
(2)依据表格中信息,计算滴加氢氧化钠溶液的物质的量浓度为___________ :(保留一位小数)
(3)原溶液中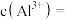
___________ ,
___________ ;
(4)将最终生成的沉淀过滤、洗涤、干燥后,放入坩埚中灼烧,得到的固体质量为4.9克。若灼烧后的固体为 ,则x的值为多少?
,则x的值为多少?___________ (无计算过程不给分)。
 、
、 、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
(1)写出OA段发生的离子方程式
(2)依据表格中信息,计算滴加氢氧化钠溶液的物质的量浓度为
| 分子式:NaOH 相对分子质量:40 密度:  NaOH的质量分数:16.7% |
(3)原溶液中
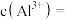

(4)将最终生成的沉淀过滤、洗涤、干燥后,放入坩埚中灼烧,得到的固体质量为4.9克。若灼烧后的固体为
 ,则x的值为多少?
,则x的值为多少?
更新时间:2024-01-26 10:53:32
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
CH2==CH2+Cl2→CH2Cl—CH2Cl ①
CH2Cl—CH2Cl→CH2="=CHCl+HCl "②
已知反应①中二氯乙烷的产率(产率= ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯__________ t,同时得到副产物氯化氢__________ t。(计算结果保留1位小数)
CH2==CH2+Cl2→CH2Cl—CH2Cl ①
CH2Cl—CH2Cl→CH2="=CHCl+HCl "②
已知反应①中二氯乙烷的产率(产率=
 ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】计算填空:
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为_______ 。
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为_______ 。
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为_______ 。
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为_______ g。(已知:2NaHCO3 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)
(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=______ mol/L。
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为
 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】向100mL含HCl的AlCl3溶液中逐滴加入0.1mol·L-1的NaOH溶液,加入NaOH溶液的体积V(mL)与产生Al(OH)3沉淀的物质的量n(mol)的关系如图:
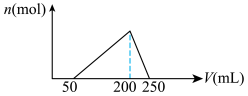
试计算:(请写出运算过程)
(1)原溶液中HCl的物质的量浓度。____________
(2)原溶液中AlCl3的物质的量浓度。____________

试计算:(请写出运算过程)
(1)原溶液中HCl的物质的量浓度。
(2)原溶液中AlCl3的物质的量浓度。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】把 、
、 、
、 三种固体组成的混合物溶于足量水后有
三种固体组成的混合物溶于足量水后有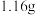 白色沉淀,在所得的浊液中逐滴加入
白色沉淀,在所得的浊液中逐滴加入 溶液,加入
溶液,加入 溶液的体积与生成沉淀的质量关系如图所示,试回答:
溶液的体积与生成沉淀的质量关系如图所示,试回答:
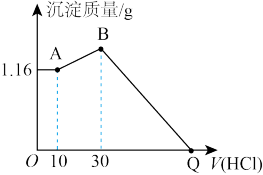
(1)写出AB段反应的离子方程式_______ 。B点的沉淀物的化学式为_______ 。
(2)求原混合物中NaOH的质量:_______ 。
(3)求Q点加入的HCl溶液体积:_______ 。
 、
、 、
、 三种固体组成的混合物溶于足量水后有
三种固体组成的混合物溶于足量水后有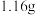 白色沉淀,在所得的浊液中逐滴加入
白色沉淀,在所得的浊液中逐滴加入 溶液,加入
溶液,加入 溶液的体积与生成沉淀的质量关系如图所示,试回答:
溶液的体积与生成沉淀的质量关系如图所示,试回答:
(1)写出AB段反应的离子方程式
(2)求原混合物中NaOH的质量:
(3)求Q点加入的HCl溶液体积:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】向20mL某物质的量浓度的AlCl3溶液中滴加2mol/LNaOH溶液时,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH溶液的体积(mL)和所得沉淀的物质的量(mol)的关系如图所示。则:
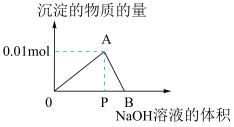
(1)写出OA段发生反应的离子方程式:OA段___ ,图中线段OP:PB=__ ,
(2)计算原AlCl3溶液的物质的量浓度为__ mol/L,
(3)图中A对应的横坐标为__ mL,
(4)当加入5mLNaOH溶液时,产生沉淀量为__ mol,
(5)当加入的NaOH溶液过量时,使最初生成的沉淀部分溶解,要得到与(4)中相同的沉淀量,加入NaOH溶液的体积为__ mL。

(1)写出OA段发生反应的离子方程式:OA段
(2)计算原AlCl3溶液的物质的量浓度为
(3)图中A对应的横坐标为
(4)当加入5mLNaOH溶液时,产生沉淀量为
(5)当加入的NaOH溶液过量时,使最初生成的沉淀部分溶解,要得到与(4)中相同的沉淀量,加入NaOH溶液的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将 36.0gFeC2O4•2H2O隔绝空气加热使之分解, 最终可得到 15.2g 某种铁的氧化物, 请通过计算推测该铁的氧化物的组成: __________________ ( 写出化学式)。并写出计算过程:________________________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】准确称取10.0g铝土矿样品(含Al2O3、Fe2O3、SiO2),加入100 mL硫酸溶液,充分反应后向滤液中加入10mol/L的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液的体积关系如图所示:
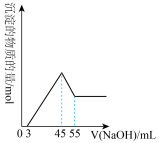
(1)计算所用硫酸溶液的物质的量浓度为______________ ;
(2)Al2O3的物质的量为________________ mol;
(3)SiO2的质量为_________ g。

(1)计算所用硫酸溶液的物质的量浓度为
(2)Al2O3的物质的量为
(3)SiO2的质量为
您最近一年使用:0次




