计算填空:
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为_______ 。
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为_______ 。
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为_______ 。
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为_______ g。(已知:2NaHCO3 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)
(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=______ mol/L。
(1)40.5g某金属氯化物MCl2中含有Cl- 0.6mol,则M的相对原子质量为
(2)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(3)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO与CO2气体的体积比为
(4)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少3.1g,则原混合物中碳酸钠的质量为
 Na2CO3+H2O+CO2)
Na2CO3+H2O+CO2)(5)某NaOH溶液中H2O和Na+的物质的量之比为20:1,测得该溶液的密度为1.1g /mL。 溶液中c(Na+)=
更新时间:2023-11-13 18:10:47
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将20.0g质量分数为14.0%的KNO3溶液跟30.0g质量分数为24.0%的KNO3溶液混合,得到密度为1.15g•cm-3的混合溶液。计算:
(1)混合后溶液中溶质的质量分数为____ 。
(2)混合后溶液中溶质的物质的量浓度为___ 。
(3)在1000g水中需溶解____ molKNO3才能使其浓度恰好与上述混合后溶液的浓度相等。
(1)混合后溶液中溶质的质量分数为
(2)混合后溶液中溶质的物质的量浓度为
(3)在1000g水中需溶解
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.根据下列各题中所给出的数据,可分别求出其溶液中溶质的质量分数或溶液中溶质的物质的量浓度,试判断并求解。
(1)已知某氢氧化钠溶液VL中含有n个氢氧根离子,可求出此溶液的___ 是___ 。
(2)已知某氢氧化钠溶液中Na+与H2O的个数之比为1:a,则可求出此溶液的___ 为___ 。
Ⅱ.常温下,10.0mL1.0mol•L-1的H2SO4(aq),加水稀释到500mL,所得H2SO4溶液的浓度为___ mol•L-1;蒸发浓缩使溶液的体积为2.40mL,所得H2SO4溶液的浓度为___ mol•L-1。(结果保留小数点后一位)
Ⅲ.已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中溶质的质量分数为___ 。(结果保留小数点后一位)
Ⅳ.现有一混合物的水溶液,可能含有以下离子中的几种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-现取三份各100mL溶液进行如下实验: 第一份加入AgNO3溶液有沉淀产生;第二份加足量NaOH溶液加热后,收集到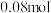 气体;第三份加足量
气体;第三份加足量 溶液后,得到干燥沉淀
溶液后,得到干燥沉淀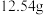 ,经足量盐酸洗涤、干燥后,沉淀质量为
,经足量盐酸洗涤、干燥后,沉淀质量为 。
。
该混合液中一定含有___ ,可能含___ ,且n(K+)___ (填取值范围)
(1)已知某氢氧化钠溶液VL中含有n个氢氧根离子,可求出此溶液的
(2)已知某氢氧化钠溶液中Na+与H2O的个数之比为1:a,则可求出此溶液的
Ⅱ.常温下,10.0mL1.0mol•L-1的H2SO4(aq),加水稀释到500mL,所得H2SO4溶液的浓度为
Ⅲ.已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中溶质的质量分数为
Ⅳ.现有一混合物的水溶液,可能含有以下离子中的几种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-现取三份各100mL溶液进行如下实验: 第一份加入AgNO3溶液有沉淀产生;第二份加足量NaOH溶液加热后,收集到
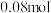 气体;第三份加足量
气体;第三份加足量 溶液后,得到干燥沉淀
溶液后,得到干燥沉淀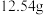 ,经足量盐酸洗涤、干燥后,沉淀质量为
,经足量盐酸洗涤、干燥后,沉淀质量为 。
。该混合液中一定含有
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】在25 ℃时,将a mol·L-1的氨水溶液与0.02 mol·L-1HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示25 ℃时NH3·H2O的电离常数Kb=___________ 。用质量分数为17%、密度为0.93 g·cm-3的氨水,配制200 mL a mol·L-1的氨水,所需原氨水的体积V=___________ mL
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
请回答下列问题。
(1)H2O的摩尔质量为___________ ,0.18g H2O的物质的量为_______________ mol
(2)配制0.1mol/L H2SO4溶液500mL,则需要H2SO4的质量为_____________ g
(3)在上述的反应中,若生成22g CO2
ⅰ.标准状况下,CO2的体积为_________ L
ⅱ.转移电子的数目为________________
(4)标准状况下,由CO和CO2 组成的混合气体为6.72 L,质量为12 g,则该混合气体的平均相对分子质量是_____________
3C + 2K2Cr2O7 + 8H2SO4(稀)= 3CO2↑ + 2K2SO4 + 2Cr2(SO4)3 + 8 H2O
请回答下列问题。
(1)H2O的摩尔质量为
(2)配制0.1mol/L H2SO4溶液500mL,则需要H2SO4的质量为
(3)在上述的反应中,若生成22g CO2
ⅰ.标准状况下,CO2的体积为
ⅱ.转移电子的数目为
(4)标准状况下,由CO和CO2 组成的混合气体为6.72 L,质量为12 g,则该混合气体的平均相对分子质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是_______ 。
(2)下列所给出的几组物质中:标准状况下体积最大的是_______ ;质量最大的是_______ 。(填序号)
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是_______ mol,具有相同氧原子数的硫酸分子有_______ 个。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)已知一混合溶液中有Na+、Cl-、SO 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为 _______ 。
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是
(2)下列所给出的几组物质中:标准状况下体积最大的是
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)已知一混合溶液中有Na+、Cl-、SO
 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】已知阿伏加 德罗常数的值为NA,根据所学知识填空。
(1)3molH2O含有__ 个H2O;
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的质量是__ g;
(3)已知NH3的相对分子质量为17,则NH3的摩尔质量为__ g/mol;
(4)若某原子的摩尔质量为Mg·mol-1,则一个该原子的真实质量是___ g;
(5)CO2中含有6.02×1023个O,则CO2的物质的量为__ mol;
(6)6.02×1022个OH-的电子物质的量为___ mol。
(7)已知一个铁原子的质量为bg,则铁的摩尔质量为___ g/mol。
(1)3molH2O含有
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的质量是
(3)已知NH3的相对分子质量为17,则NH3的摩尔质量为
(4)若某原子的摩尔质量为Mg·mol-1,则一个该原子的真实质量是
(5)CO2中含有6.02×1023个O,则CO2的物质的量为
(6)6.02×1022个OH-的电子物质的量为
(7)已知一个铁原子的质量为bg,则铁的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将乙烯和乙烷的混合气体11.2 L(标准状况)通入足量的溴的四氯化碳溶液中,充分反应后,溴的四氯化碳溶液质量增加了8.4g。求原混合物气体中乙烯与乙烷的物质的量之比和质量之比__________ 、_____________ 。
您最近一年使用:0次
【推荐2】铝合金由于其优良的性能,已经成为人类生活中常用的金属材料。硬铝7075在航空工业中Zn—5.85%。有着广泛的应用,其化学成分为:Al—90.72%、Cu—1.39%、Mg—2.04%、Zn—5.85%。
(1)某学习小组为了验证其成分,称取1.00g该硬铝,加入足量的氢氧化钠溶液中,充分反应后生成的气体经干燥后在标准状态下的体积为___ L(保留3位有效数字)。已知:Zn+2NaOH=Na2ZnO2+H2↑。
实验时需配制2mol/L的氢氧化钠溶液(ρ=1.08g/mL),其质量百分比浓度为___ %(保留3位有效数字)。
定量实验至少测定组数据,配制时还需多备组的量以防实验中操作错误,因此配制上述实验所用的氢氧化钠溶液,至少需要称量固体氢氧化钠___ g。
一种由铝土矿(主要含氧化铝,还有二氧化硅、氧化铁和其他杂质)的工艺流程如图:
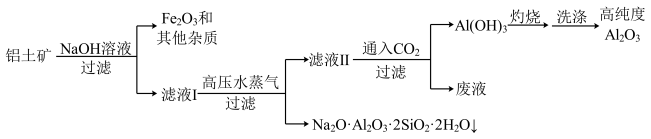
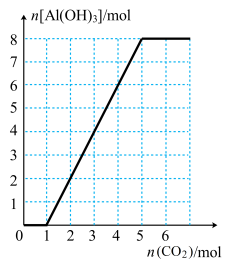
(2)取一定量的滤液Ⅱ,通入二氧化碳,生成氢氧化铝沉淀的量如图所示,若溶液中生成的碳酸钠为3mol时,通入的二氧化碳可能为___ mol。
(3)实际生产中,由滤液Ⅱ到高纯度Al2O3(纯度99.0%)的过程中会损失2%的铝,电解熔融的氧化铝制取金属铝的过程会损失电解熔融的氧化铝制取金属铝4%的铝,若要生产10吨硬铝7075,至少需要多少吨铝土矿___ (含氧化铝55.1%、二氧化硅6.0%)?(保留3位有效数字)
(1)某学习小组为了验证其成分,称取1.00g该硬铝,加入足量的氢氧化钠溶液中,充分反应后生成的气体经干燥后在标准状态下的体积为
实验时需配制2mol/L的氢氧化钠溶液(ρ=1.08g/mL),其质量百分比浓度为
定量实验至少测定组数据,配制时还需多备组的量以防实验中操作错误,因此配制上述实验所用的氢氧化钠溶液,至少需要称量固体氢氧化钠
一种由铝土矿(主要含氧化铝,还有二氧化硅、氧化铁和其他杂质)的工艺流程如图:

(2)取一定量的滤液Ⅱ,通入二氧化碳,生成氢氧化铝沉淀的量如图所示,若溶液中生成的碳酸钠为3mol时,通入的二氧化碳可能为

(3)实际生产中,由滤液Ⅱ到高纯度Al2O3(纯度99.0%)的过程中会损失2%的铝,电解熔融的氧化铝制取金属铝的过程会损失电解熔融的氧化铝制取金属铝4%的铝,若要生产10吨硬铝7075,至少需要多少吨铝土矿
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】已知单质铜与稀硝酸的反应为3Cu+8HNO3===2NO↑+4H2O+3Cu(NO3)2(Cu的相对原子质量为64)。现把19.2 g Cu放入200 mL 5 mol·L-1硝酸中,充分反应,问:
(1)哪种物质过量?______
(2)参加反应的硝酸的物质的量为多少?______
(3)在标准状况下产生的气体的体积为多少?______
(4)生成水的分子数为多少?______
(5)若反应前后溶液的体积不变,则生成Cu(NO3)2的物质的量浓度为多少?______
(1)哪种物质过量?
(2)参加反应的硝酸的物质的量为多少?
(3)在标准状况下产生的气体的体积为多少?
(4)生成水的分子数为多少?
(5)若反应前后溶液的体积不变,则生成Cu(NO3)2的物质的量浓度为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】碳酸钠与100mL某浓度的盐酸恰好完全反应后得到气体5.6L(标准状况)。试求:
(1)碳酸钠的物质的量
(2)所用盐酸的物质的量浓度
(1)碳酸钠的物质的量
(2)所用盐酸的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】往100mLNaOH溶液中通入CO2,充分反应后,在减压和降温的条件下,小心将溶液蒸干得到白色固体M。通入CO2的体积V(CO2)(标准状况)与M的质量m(g)的关系如图所示。
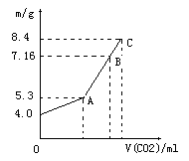
(1)A点时,白色固体的化学式__________ ,通入的CO2的体积为________ mL(标准状况下,下同)
(2)C点时,白色固体M的化学式为________ ,通入的CO2的体积为__________ mL;
(3)B点时M的组成为______ (用化学式表示)通入的CO2的体积为_____________ mL;
(4)原NaOH溶液的物质的量浓度为__________________________ 。

(1)A点时,白色固体的化学式
(2)C点时,白色固体M的化学式为
(3)B点时M的组成为
(4)原NaOH溶液的物质的量浓度为
您最近一年使用:0次



