1 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 和 和 的混合气体中所含氮原子数为 的混合气体中所含氮原子数为 |
B. 熔融的 熔融的 中含有 中含有 个阳离子 个阳离子 |
C.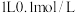 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
D. 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
您最近半年使用:0次
2 . 氢氟酸可以溶蚀石英玻璃,反应方程式为: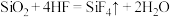 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
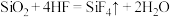 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.每60gSiO2含NA个SiO2分子 | B.标准状况下,1molHF体积为22.4L |
| C.1molH2O含有孤对电子数为2NA | D.0.1mol/L的氢氟酸中含H+数小于0.1NA |
您最近半年使用:0次
名校
解题方法
3 . 将25.6g铜与一定量的浓硝酸反应,铜消耗完时,共产生 混合气体11.2L(标准状况),则整个反应过程中消耗
混合气体11.2L(标准状况),则整个反应过程中消耗 总的物质的量为
总的物质的量为
 混合气体11.2L(标准状况),则整个反应过程中消耗
混合气体11.2L(标准状况),则整个反应过程中消耗 总的物质的量为
总的物质的量为| A.1mol | B. | C.1.6mol | D.1.3mol |
您最近半年使用:0次
名校
4 . 设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A. 苯分子含碳碳双键数目为 苯分子含碳碳双键数目为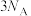 |
B. 正丁烷和 正丁烷和 异丁烷的混合物中共价键数目为 异丁烷的混合物中共价键数目为 |
C.常温常压下, 乙烯含 乙烯含 键数目为 键数目为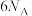 |
D. 羟基所含电子数为 羟基所含电子数为 |
您最近半年使用:0次
5 . 水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法错误的是
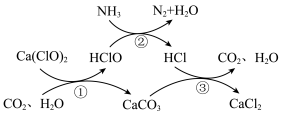
A.标准状况下, 所含的共用电子对数目为 所含的共用电子对数目为 |
B.标准状况下, 所含的原子总数为 所含的原子总数为 |
C.标准状况下, 气体溶于 气体溶于 水中形成的溶液浓度为 水中形成的溶液浓度为 |
D.反应②每生成 消耗 消耗 分子数目为 分子数目为 |
您最近半年使用:0次
解题方法
6 . 向 含
含 和
和 混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
 含
含 和
和 混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是
混合溶液中加入一定量锌粉,反应过程中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是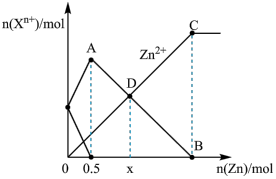
A.起始时, 溶液和 溶液和 溶液的物质的量浓度均为 溶液的物质的量浓度均为 |
B.D点的横坐标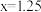 |
C.线段 表示溶液中 表示溶液中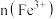 的变化趋势 的变化趋势 |
D.反应至 点时,溶液总质量增加 点时,溶液总质量增加 |
您最近半年使用:0次
7 . 下列说法中,正确的是
A. 的摩尔质量是 的摩尔质量是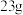 |
B.标准状况下, 的体积是 的体积是 |
C.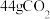 中含有的氧原子数约为 中含有的氧原子数约为 |
D.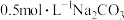 溶液中 溶液中 是 是 |
您最近半年使用:0次
8 . 设 为阿伏伽德罗常数的值,则下列说法正确的是
为阿伏伽德罗常数的值,则下列说法正确的是
 为阿伏伽德罗常数的值,则下列说法正确的是
为阿伏伽德罗常数的值,则下列说法正确的是A.常温常压下, 的体积为 的体积为 |
B.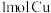 与足量的S充分反应,转移的电子数为 与足量的S充分反应,转移的电子数为 |
C. 与含 与含 的浓硫酸在加热的条件下反应时,生成的 的浓硫酸在加热的条件下反应时,生成的 在标准状况下的体积为 在标准状况下的体积为 |
D.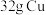 与足量浓 与足量浓 反应时,转移的电子数为 反应时,转移的电子数为 |
您最近半年使用:0次
名校
9 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 化学式为 化学式为 的单糖分子中含 的单糖分子中含 的数目为 的数目为 |
B.标准状况下, 溶于水,溶液中 溶于水,溶液中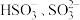 和 和 的微粒数之和小于 的微粒数之和小于 |
C.过量酸性 溶液与 溶液与 完全反应,转移电子数为 完全反应,转移电子数为 |
D.常温下,已知 ,则该温度下 ,则该温度下 饱和溶液中含有 饱和溶液中含有 个 个 |
您最近半年使用:0次
解题方法
10 . 某实验小组以含铁污泥(主要成分为 、
、 及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
(1)写出“酸浸”时, 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:___________ 。
(2)“滤液X”中含有的阳离子为___________ 。
(3)路线I中,加入 溶液的目的是
溶液的目的是___________ 。
(4)写出加入氨水“沉淀”时的离子方程式:___________ 。
(5)写出加入过量铁粉时发生反应的离子方程式:___________ 、___________ 。
(6)“酸浸”时加入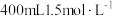 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为___________ g。
 、
、 及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。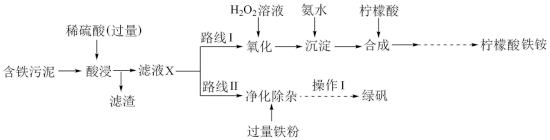
(1)写出“酸浸”时,
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(2)“滤液X”中含有的阳离子为
(3)路线I中,加入
 溶液的目的是
溶液的目的是(4)写出加入氨水“沉淀”时的离子方程式:
(5)写出加入过量铁粉时发生反应的离子方程式:
(6)“酸浸”时加入
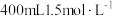 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
您最近半年使用:0次



