向100mL含HCl的AlCl3溶液中逐滴加入0.1mol·L-1的NaOH溶液,加入NaOH溶液的体积V(mL)与产生Al(OH)3沉淀的物质的量n(mol)的关系如图:
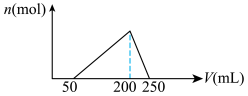
试计算:(请写出运算过程)
(1)原溶液中HCl的物质的量浓度。____________
(2)原溶液中AlCl3的物质的量浓度。____________

试计算:(请写出运算过程)
(1)原溶液中HCl的物质的量浓度。
(2)原溶液中AlCl3的物质的量浓度。
更新时间:2019-09-14 14:35:26
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)0.5 mol水中含有___________ 个氢原子。
(2)9g水与___________ g硫酸所含的分子数相等。
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液___________ mL。
(4)标准状况下,和4mol 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为___________ 。
(5) 个
个 与
与___________ mol  质量相等。
质量相等。
(1)0.5 mol水中含有
(2)9g水与
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液
(4)标准状况下,和4mol
 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为(5)
 个
个 与
与 质量相等。
质量相等。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某学生在实验室里分析一瓶部分变质的氢氧化钠样品的组成。他先称取mg此样品倒入某容器,然后加入245g10%的稀硫酸,结果恰好完全反应,收集到8.8g气体;再取相同质量的该样品配成405.2g溶液,加入一定质量的熟石灰后也恰好完全反应。求:
(1)该样品的组成情况和m的值_______ ;
(2)405.2g该样品溶液与熟石灰反应后所得溶液的溶质质量分数_______ 。
(1)该样品的组成情况和m的值
(2)405.2g该样品溶液与熟石灰反应后所得溶液的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】根据要求计算。
(1)0.5mol NaAlO2含有___ mol Na+;_____ mol AlO2-;含___ 个O。
(2)在100 mL 0.2 mol/L NaOH溶液中含溶质的物质的量___ mol;配制50 mL 0.2 mol/LFeSO4溶液,需要FeSO4____ g。
(3)1.06 g的Na2CO3的物质的量是___ mol;含有的CO32-离子数是___ 个。
(4)标准状况下,0.3 mol CH4的体积是___ ;含有碳原子质量是___ ;含有氢原子物质的量_____ 。
(1)0.5mol NaAlO2含有
(2)在100 mL 0.2 mol/L NaOH溶液中含溶质的物质的量
(3)1.06 g的Na2CO3的物质的量是
(4)标准状况下,0.3 mol CH4的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】硝酸发生氧化还原反应的时候,一般硝酸浓度越稀,对应的还原产物中氮的化合价越低。现有一定量的铁粉和铝粉混合物与一定量很稀的硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入1 mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。(提示:氢氧化铝不溶于弱酸弱碱,只溶于强酸强碱)

(1)铁与极稀的硝酸发生反应时得还原产物可能是____________ ;该反应的化学方程式为______________________________________________________________ 。
(2)B的数值是:______________ mol。
(3)C的数值是:______________ mL。

(1)铁与极稀的硝酸发生反应时得还原产物可能是
(2)B的数值是:
(3)C的数值是:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】取1.77g镁铝合金投入到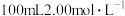 的盐酸中,合金完全溶解,放出氢气1.904L(已折算成标况)请计算:
的盐酸中,合金完全溶解,放出氢气1.904L(已折算成标况)请计算:
(1)镁铝合金中镁的质量分数=______ %(保留三位有效数字)
(2)上述溶液中继续滴加 的NaOH溶液,得到沉淀3.10g。则V的最大值=
的NaOH溶液,得到沉淀3.10g。则V的最大值=______ mL。(写出计算过程)
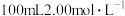 的盐酸中,合金完全溶解,放出氢气1.904L(已折算成标况)请计算:
的盐酸中,合金完全溶解,放出氢气1.904L(已折算成标况)请计算:(1)镁铝合金中镁的质量分数=
(2)上述溶液中继续滴加
 的NaOH溶液,得到沉淀3.10g。则V的最大值=
的NaOH溶液,得到沉淀3.10g。则V的最大值=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在含有H+、Mg2+、Al3+简单阳离子的100mL溶液中,逐滴滴加5mol·L-1的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
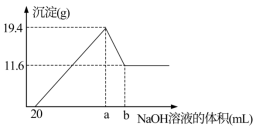
(1)沉淀减少时发生的离子方程式:___________ 。
(2)a点的数值为:___________ mL。

(1)沉淀减少时发生的离子方程式:
(2)a点的数值为:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将3mol/L NaOH溶液滴入到25mL 一定浓度的AlCl3溶液中。下图是整个过程的数学分析曲线。其中横轴表示加入OH-的物质的量,纵轴表示产生的Al(OH)3沉淀的物质的量。据图回答:
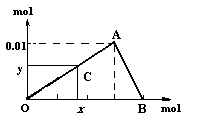
(1)当C点从O点向A点运动时,表示随着OH-的不断加入,沉淀量逐渐________ 。OA曲线表示的离子反应是:______________________________ ;由此可得A点的坐标为_______ ;此时加入氢氧化钠溶液的体积为____________ ;
(2)AB曲线表示的离子反应为:___________________ ,由此可得B点的坐标为:_________ 。
(3)由上述分析,可求得AlCl3溶液中Al3+离子的浓度为:_____ mol/L。
(4)当x=0.035时,铝元素在体系中的存在形式为________ ,其物质的量为____________ 。

(1)当C点从O点向A点运动时,表示随着OH-的不断加入,沉淀量逐渐
(2)AB曲线表示的离子反应为:
(3)由上述分析,可求得AlCl3溶液中Al3+离子的浓度为:
(4)当x=0.035时,铝元素在体系中的存在形式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16 g白色沉淀,再向所得浊液中逐渐加入1.00mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。
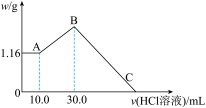
(1)A点的沉淀物的化学式为___________ 。
(2)写出A点至B点发生反应的离子方程式:___________ 。
(3)某溶液中溶有MgCl2和AlCl3两种溶质,若把两者分开,应选用的试剂为:NaOH溶液、___________ (填化学式)和盐酸。
(4)C点(此时沉淀恰好完全溶解)HCl溶液的体积为___________ mL。

(1)A点的沉淀物的化学式为
(2)写出A点至B点发生反应的离子方程式:
(3)某溶液中溶有MgCl2和AlCl3两种溶质,若把两者分开,应选用的试剂为:NaOH溶液、
(4)C点(此时沉淀恰好完全溶解)HCl溶液的体积为
您最近一年使用:0次



