名校
解题方法
1 . 回答下列问题
(1)0.5 mol水中含有___________ 个氢原子。
(2)9g水与___________ g硫酸所含的分子数相等。
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液___________ mL。
(4)标准状况下,和4mol 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为___________ 。
(5) 个
个 与
与___________ mol  质量相等。
质量相等。
(1)0.5 mol水中含有
(2)9g水与
(3)欲配置500mL 0.6mol/L的NaOH溶液,需3mol/L的NaOH溶液
(4)标准状况下,和4mol
 含有相同氢原子数的
含有相同氢原子数的 的体积为
的体积为(5)
 个
个 与
与 质量相等。
质量相等。
您最近一年使用:0次
名校
解题方法
2 . 移取20.00 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。
已知:
① 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;
② 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化
(1)加入 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为_______ 。
(2)酸化后 歧化发生离子反应方程式为
歧化发生离子反应方程式为_______ 。
(3)加入 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为_______ 。
(4)则溶液中的 的浓度为
的浓度为_______ ; 的浓度为
的浓度为_______ 。
(5)若溶液酸化后将 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将_______ (填“偏大”、“偏小”或“不变”)。
 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。已知:
①
 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;②
 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化(1)加入
 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为(2)酸化后
 歧化发生离子反应方程式为
歧化发生离子反应方程式为(3)加入
 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为(4)则溶液中的
 的浓度为
的浓度为 的浓度为
的浓度为(5)若溶液酸化后将
 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将
您最近一年使用:0次
3 . 化学计量在化学中占有重要地位,请回答下列问题:
(1)青蒿素C15H22O5的摩尔质量为_______ 。
(2)在标准状况下,22.4 L由O2和N2组成的混合气体中,含有的分子总数约为_______ 。
(3)在标准状况下,含有 个氦原子的氦气的体积约为
个氦原子的氦气的体积约为_______ 。
(4)某消毒小组人员用17 mol/L的浓硫酸配制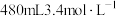 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为_______  ;所配溶液中的
;所配溶液中的 的物质的量浓度为
的物质的量浓度为_______ 。
(5)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。标准状况下,向Ⅰ中充入8 g SO2,Ⅱ中充入8 g O2,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为_______ 。

(6)把7.8克镁铝合金的粉末放入过量的盐酸中,得到8.96 LH2 (标准状况)。该合金中铝和镁的物质的量之比_______ 。
(1)青蒿素C15H22O5的摩尔质量为
(2)在标准状况下,22.4 L由O2和N2组成的混合气体中,含有的分子总数约为
(3)在标准状况下,含有
 个氦原子的氦气的体积约为
个氦原子的氦气的体积约为(4)某消毒小组人员用17 mol/L的浓硫酸配制
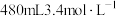 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为 ;所配溶液中的
;所配溶液中的 的物质的量浓度为
的物质的量浓度为(5)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。标准状况下,向Ⅰ中充入8 g SO2,Ⅱ中充入8 g O2,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为

(6)把7.8克镁铝合金的粉末放入过量的盐酸中,得到8.96 LH2 (标准状况)。该合金中铝和镁的物质的量之比
您最近一年使用:0次
名校
4 . 低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。结合下列有关图示和所学知识回答:
(1)用 催化加氢可以制取乙烯:
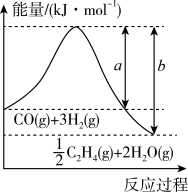
催化加氢可以制取乙烯: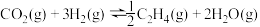 。若该反应体系的能量随反应过程变化关系如图所示,则该反应的
。若该反应体系的能量随反应过程变化关系如图所示,则该反应的
_______ (用含a、b的式子表示)。又知:相关化学键的键能如下表所示,实验测得上述反应的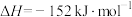 ,则表中的x=
,则表中的x=_______ 。
注:乙烯结构如图: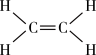
(2)用 表示阿伏加德罗常数,在
表示阿伏加德罗常数,在 (气态)完全燃烧生成
(气态)完全燃烧生成 和液态水的反应中,每有
和液态水的反应中,每有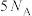 个电子转移时,放出
个电子转移时,放出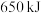 的热量。其燃烧热的热化学方程式为
的热量。其燃烧热的热化学方程式为_______ 。
(3)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
①科学家提出由 制取C的太阳能工艺如图所示。
制取C的太阳能工艺如图所示。
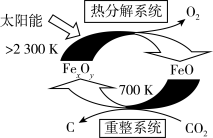
已知“重整系统”发生的反应中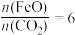 ,则
,则 的化学式为
的化学式为_______ 。“热分解系统”中每分解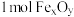 ,转移电子的物质的量为
,转移电子的物质的量为_______ mol。
②工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: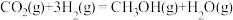
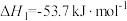 ,
,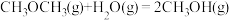
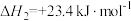 ,则
,则
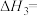
_______  。
。
(1)用
 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: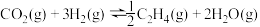 。若该反应体系的能量随反应过程变化关系如图所示,则该反应的
。若该反应体系的能量随反应过程变化关系如图所示,则该反应的
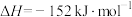 ,则表中的x=
,则表中的x=
| 化学键 |  |  | 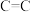 |  |  |
键能/ | 803 | 436 | x | 414 | 464 |
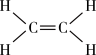
(2)用
 表示阿伏加德罗常数,在
表示阿伏加德罗常数,在 (气态)完全燃烧生成
(气态)完全燃烧生成 和液态水的反应中,每有
和液态水的反应中,每有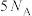 个电子转移时,放出
个电子转移时,放出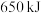 的热量。其燃烧热的热化学方程式为
的热量。其燃烧热的热化学方程式为(3)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
①科学家提出由
 制取C的太阳能工艺如图所示。
制取C的太阳能工艺如图所示。
已知“重整系统”发生的反应中
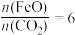 ,则
,则 的化学式为
的化学式为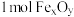 ,转移电子的物质的量为
,转移电子的物质的量为②工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: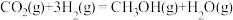
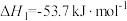 ,
,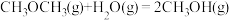
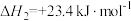 ,则
,则
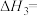
 。
。
您最近一年使用:0次
2022-05-20更新
|
295次组卷
|
2卷引用:吉林省长春吉大附中实验学校2021-2022学年高一下学期线上测试化学试题
名校
5 . 请回答下列问题:
(1)标准状况下O2、SO2、CH4的密度之比是___________ 。
(2)取一定量的Na2S样品,此样品中含有Na+ 1.2mol,则该样品的质量是___________ 。
(3)等质量的氧气和臭氧所含原子数之比为___________ ;分子的物质的量之比为___________ 。
(4)标准状况下33.6L CO2的质量是___________ 。
(1)标准状况下O2、SO2、CH4的密度之比是
(2)取一定量的Na2S样品,此样品中含有Na+ 1.2mol,则该样品的质量是
(3)等质量的氧气和臭氧所含原子数之比为
(4)标准状况下33.6L CO2的质量是
您最近一年使用:0次
6 . 计算填空:
(1)_______ molH2O中所含有的氧原子数与1.5 molCO2的氧原子数相同。
(2)质量为9.8g的H2SO4物质的量是_______ 。
(3)1.204×1024个H2的物质的量是_______ 。
(4)_______ g H2O与34g NH3含有相同的氢原子数。
(5)相同物质的量的CO2和O2,其分子数之比为_______ ,原子数之比为_______ ,氧原子数之比为_______ ;在2molNa2SO4溶液中Na+的物质的量为_______ mol
(6)1molCO2 中所含的质子的数目_______
(1)
(2)质量为9.8g的H2SO4物质的量是
(3)1.204×1024个H2的物质的量是
(4)
(5)相同物质的量的CO2和O2,其分子数之比为
(6)1molCO2 中所含的质子的数目
您最近一年使用:0次
名校
7 . 回答下列问题:
(1)在0.5mol 中,所含硫酸根离子个数共有
中,所含硫酸根离子个数共有___________ 。
(2)标准状况下,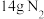 所占有的体积为
所占有的体积为___________ 。
(3)标准状况下,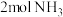 与
与___________ 
 的体积相等。
的体积相等。
(4) 和
和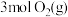 的质量之比
的质量之比___________ ,体积之比为___________ 。
(5)两份质量相等的 和
和 ,物质的量之比
,物质的量之比___________ ,所含氧原子数目之比为___________
(1)在0.5mol
 中,所含硫酸根离子个数共有
中,所含硫酸根离子个数共有(2)标准状况下,
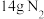 所占有的体积为
所占有的体积为(3)标准状况下,
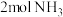 与
与
 的体积相等。
的体积相等。(4)
 和
和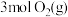 的质量之比
的质量之比(5)两份质量相等的
 和
和 ,物质的量之比
,物质的量之比
您最近一年使用:0次



