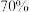请回答下列问题:
(1)标准状况下O2、SO2、CH4的密度之比是___________ 。
(2)取一定量的Na2S样品,此样品中含有Na+ 1.2mol,则该样品的质量是___________ 。
(3)等质量的氧气和臭氧所含原子数之比为___________ ;分子的物质的量之比为___________ 。
(4)标准状况下33.6L CO2的质量是___________ 。
(1)标准状况下O2、SO2、CH4的密度之比是
(2)取一定量的Na2S样品,此样品中含有Na+ 1.2mol,则该样品的质量是
(3)等质量的氧气和臭氧所含原子数之比为
(4)标准状况下33.6L CO2的质量是
更新时间:2021-12-23 18:07:29
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】计算填空。
(1)2.3gNa和足量的水反应生成气体在标况下气体的体积是___ 。
(2)5.1g镁和铝混合物与足量的盐酸反应放出气体在标准下5.6L,则镁和铝物质的量之比是___ 。
(3)2.8g铁与足量的氯气反应转移电子数是___ 。
(1)2.3gNa和足量的水反应生成气体在标况下气体的体积是
(2)5.1g镁和铝混合物与足量的盐酸反应放出气体在标准下5.6L,则镁和铝物质的量之比是
(3)2.8g铁与足量的氯气反应转移电子数是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】请写出具体计算过程。
2.45 g氯酸钾与一定质量的二氧化锰混合后加热一段时间,将残留物充分溶解,除去二氧化锰后加入稀硫酸,发生如下反应:
已知加入20 mL稀硫酸时,可生成Cl2 112.0 mL(标准状况下);若加入40 mL稀硫酸,可生成Cl2 201.6 mL(标准状况下)。
(1)计算稀硫酸的物质的量浓度。________
(2)计算氯酸钾的分解率(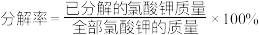 )
)_________
2.45 g氯酸钾与一定质量的二氧化锰混合后加热一段时间,将残留物充分溶解,除去二氧化锰后加入稀硫酸,发生如下反应:

已知加入20 mL稀硫酸时,可生成Cl2 112.0 mL(标准状况下);若加入40 mL稀硫酸,可生成Cl2 201.6 mL(标准状况下)。
(1)计算稀硫酸的物质的量浓度。
(2)计算氯酸钾的分解率(
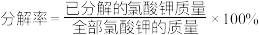 )
)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】根据所学知识,填写下列空白
(1)0.3 mol NH3分子中所含原子数与________ 个 H2O分子中所含原子数相等。
(2)已知17 gH2R中含1molH,则R的摩尔质量为__________ 。
(3)含有相同氧原子数的SO2和SO3,其分子的质量比为__________ 。
(4)标准状况下,a L HCl气体溶于水配制成b L溶液。其物质的量浓度为______ mol/L。
(5)实验室用Na2CO3·10H2O晶体配制0.5 mol/L 的Na2CO3溶液970 mL,用托盘天平应称取Na2CO3·10H2O的质量是______ 。
(6)标况下,体积为8.96 L的CO和CO2的混合气体的质量为14.4 g,则CO的质量为____ g,CO2的体积为_______ L,混合气体中碳、氧两种原子的个数比为_______ ,混合气体的平均摩尔质量为________ g/mol。
(1)0.3 mol NH3分子中所含原子数与
(2)已知17 gH2R中含1molH,则R的摩尔质量为
(3)含有相同氧原子数的SO2和SO3,其分子的质量比为
(4)标准状况下,a L HCl气体溶于水配制成b L溶液。其物质的量浓度为
(5)实验室用Na2CO3·10H2O晶体配制0.5 mol/L 的Na2CO3溶液970 mL,用托盘天平应称取Na2CO3·10H2O的质量是
(6)标况下,体积为8.96 L的CO和CO2的混合气体的质量为14.4 g,则CO的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在一定条件下,有a L O2和O3的混合气体,当其中的O3全部转化为O2时,体积变为1.2a L,求原混合气中O2和O3的质量百分含量_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题:
(1)同温同压下,同体积的气体甲烷(CH4)和二氧化碳的密度之比为___________ 。
(2)在Na2SO4和Fe(SO4)3的混合溶液中,Na+的物质的量浓度为0.1 mol/L, 的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为___________ mol/L。
(3)实验室将11.7 g氯化钠溶于水配制成500 mL溶液,取出50 mL该溶液,取出的溶液中n(Cl-)=___________ mol,c(Na+)=___________ mol/L。
(4)已知反应: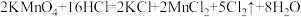 。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为
。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为___________ mol。
(1)同温同压下,同体积的气体甲烷(CH4)和二氧化碳的密度之比为
(2)在Na2SO4和Fe(SO4)3的混合溶液中,Na+的物质的量浓度为0.1 mol/L,
 的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则混合溶液中Fe3+的物质的量浓度为(3)实验室将11.7 g氯化钠溶于水配制成500 mL溶液,取出50 mL该溶液,取出的溶液中n(Cl-)=
(4)已知反应:
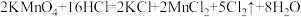 。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为
。若产生的Cl2在标准状况下的体积为5.6 L,则反应中被氧化的HCl的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】填写下列空白:
(1)有6.02×l023个H的H2O,其物质的量是_______ ;1molNa2SO4中所含的离子总数目为______ 。
(2)_____ molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为_______ 。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为________ 。
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,该混合气体对氢气的相对密度为____________ 。
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_____________ 。
(1)有6.02×l023个H的H2O,其物质的量是
(2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,该混合气体对氢气的相对密度为
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】设NA表示阿伏加 德罗常数。
(1)已知一个NO、NO2分子的质量分别是a g、b g,则氧原子的摩尔质量是(用含a、b数字的式子表示)_______ ,10 g NO2物质的量为(用含a、b数字的式子表示)____ 。
(2)已知H2+Cl2 2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?
2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?_________ 此时气体总质量是多少?________ 。
(1)已知一个NO、NO2分子的质量分别是a g、b g,则氧原子的摩尔质量是(用含a、b数字的式子表示)
(2)已知H2+Cl2
 2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?
2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】填写下列空白:
(1)1 mol H2O中约含有________ 个H2O、________ 个H、________ 个O、________ mol H、________ mol O。
(2)含有6.02×1023个H的H2O,其物质的量是_______ ;1 mol Na2SO4溶于水能电离出________ 个Na+、________ 个SO42-。
(3)________ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(4)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________ 。
(5)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________ 。
(6)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________ ,该混合气体对氢气的相对密度为________ 。
(7)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将a g该化合物加热至结晶水全部失去,剩余的残渣为b g,则n=________ 。
(8)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为____________ 。
(1)1 mol H2O中约含有
(2)含有6.02×1023个H的H2O,其物质的量是
(3)
(4)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(5)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(6)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(7)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将a g该化合物加热至结晶水全部失去,剩余的残渣为b g,则n=
(8)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】填空。
(1)2molCO2的质量为___________ g。
(2)在标准状况下2molO2所占有的体积约为___________  ,含氧原子的个数为
,含氧原子的个数为___________ 。
(3)用14.2g无水硫酸钠配制成500mL溶液,其物质的量浓度为___________ mol∙L-1。若从中取出50mL溶液,其溶质的质量为___________ g。
(1)2molCO2的质量为
(2)在标准状况下2molO2所占有的体积约为
 ,含氧原子的个数为
,含氧原子的个数为(3)用14.2g无水硫酸钠配制成500mL溶液,其物质的量浓度为
您最近一年使用:0次

 2NH3(g)
2NH3(g) ,该厂每天产生的
,该厂每天产生的 的NaOH溶液来吸收每天产生的
的NaOH溶液来吸收每天产生的