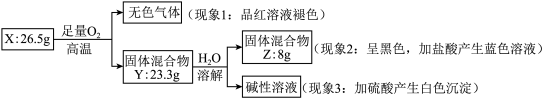
设NA表示阿伏加 德罗常数。
(1)已知一个NO、NO2分子的质量分别是a g、b g,则氧原子的摩尔质量是(用含a、b数字的式子表示)_______ ,10 g NO2物质的量为(用含a、b数字的式子表示)____ 。
(2)已知H2+Cl2 2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?
2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?_________ 此时气体总质量是多少?________ 。
(1)已知一个NO、NO2分子的质量分别是a g、b g,则氧原子的摩尔质量是(用含a、b数字的式子表示)
(2)已知H2+Cl2
 2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?
2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为多少个?
20-21高一上·全国·阶段练习 查看更多[1]
(已下线)【南昌新东方】2019 进贤一中 高一上第一次月考
更新时间:2020-04-17 10:07:28
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】请按要求,回答下列问题:
(1)等质量的O2与O3,所含氧原子数之比为_______ ;
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO 的物质的量是
的物质的量是_______ 。
(3)15.6g Na2X中含有0.4mol Na+,则Na2X的摩尔质量为_______ ,X的相对原子质量为_______ 。
(4)Cl﹣浓度为0.4mol·L﹣1的BaCl2溶液的物质的量浓度为_______ ,200mL该BaCl2溶液中含Ba2+的数目为_______ 。
(1)等质量的O2与O3,所含氧原子数之比为
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO
 的物质的量是
的物质的量是(3)15.6g Na2X中含有0.4mol Na+,则Na2X的摩尔质量为
(4)Cl﹣浓度为0.4mol·L﹣1的BaCl2溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】现有3.2g某气体(分子式:RH4),摩尔质量为16 g·mol-1,则:
(1)R的相对原子质量为____________
(2)该气体所含分子数为___________________ NA。
(3)该气体在标准状况下的体积约为___________________ L。
(4)其中氢原子数目与___________ gNH3中的氢原子数目相同
(1)R的相对原子质量为
(2)该气体所含分子数为
(3)该气体在标准状况下的体积约为
(4)其中氢原子数目与
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在标准状况下,一氧化碳和二氧化碳混合气体的质量为36 g,体积为22.4 L。
(1)混合气体中一氧化碳的体积是__________ 。
(2)混合气体中二氧化碳的物质的量是__________ 。
(1)混合气体中一氧化碳的体积是
(2)混合气体中二氧化碳的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】标准状况下,5L乙烯和乙炔的混合气体能与50g溴完全反应,求混合气体中乙烯和乙炔的体积分数_________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】湿法炼铜(铁与硫酸铜溶液反应)是一种重要的炼铜工艺。欲用该原理制备 铜单质,请计算至少需要铁的物质的量
铜单质,请计算至少需要铁的物质的量____________ 。
 铜单质,请计算至少需要铁的物质的量
铜单质,请计算至少需要铁的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,生成1.16 g白色沉淀。再向所得的悬浊液中逐滴加入1.00 mol/L 的盐酸溶液,加入盐酸溶液的体积与生成沉淀的关系如下图所示。试回答:
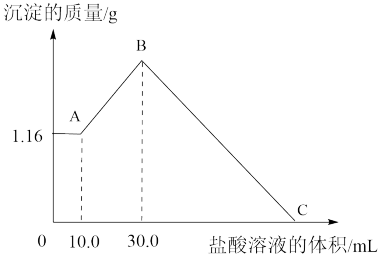
(1)写出A点到B点发生反应的离子方程式_______ 。
(2)写出B点到C点发生反应的离子方程式_______ 。
(3)C点加入盐酸溶液的体积为_______ 。
(4)原混合物中MgCl2的物质的量是_______ ,NaOH的质量是_______ 。

(1)写出A点到B点发生反应的离子方程式
(2)写出B点到C点发生反应的离子方程式
(3)C点加入盐酸溶液的体积为
(4)原混合物中MgCl2的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】完成下面有关计算,并在空白处填写结果。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是___ 。
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为___ ,需要二者的固体质量之比为___ 。
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为___ ,原Fe2(SO4)3溶液的物质的量浓度为____ 。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为
您最近一年使用:0次