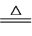请写出具体计算过程。
2.45 g氯酸钾与一定质量的二氧化锰混合后加热一段时间,将残留物充分溶解,除去二氧化锰后加入稀硫酸,发生如下反应:
已知加入20 mL稀硫酸时,可生成Cl2 112.0 mL(标准状况下);若加入40 mL稀硫酸,可生成Cl2 201.6 mL(标准状况下)。
(1)计算稀硫酸的物质的量浓度。________
(2)计算氯酸钾的分解率(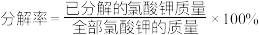 )
)_________
2.45 g氯酸钾与一定质量的二氧化锰混合后加热一段时间,将残留物充分溶解,除去二氧化锰后加入稀硫酸,发生如下反应:

已知加入20 mL稀硫酸时,可生成Cl2 112.0 mL(标准状况下);若加入40 mL稀硫酸,可生成Cl2 201.6 mL(标准状况下)。
(1)计算稀硫酸的物质的量浓度。
(2)计算氯酸钾的分解率(
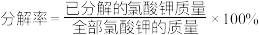 )
)
23-24高一上·上海·期中 查看更多[2]
更新时间:2023-11-26 13:40:51
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】完成下列填空:
(1)0.25 mol CO2在标准状况下的体积为________ ,含有的原子数目为________ 。
(2)0.98 g物质H2A中约含有6.02×1021个分子,则该物质的物质的量为________ ,H2A的摩尔质量为__________ ,A的相对原子质量为________ 。
(3)40 g的碳酸钙与足量的盐酸反应制备CO2,消耗盐酸__________ mol,标准状况下生成CO2 __________ L。
(1)0.25 mol CO2在标准状况下的体积为
(2)0.98 g物质H2A中约含有6.02×1021个分子,则该物质的物质的量为
(3)40 g的碳酸钙与足量的盐酸反应制备CO2,消耗盐酸
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】① HNO3的摩尔质量是_______ ,0.5mol HNO3的质量是_________ ,1.5mol HNO3含有_____ mol氧原子。
② 标准状况下11.2L CO2的物质的量是____ 。
② 标准状况下11.2L CO2的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)将3.22g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为___ g。
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L人造空气的质量是4.8g,其中氧气和氦气的分子数之比是___ ,氧气的质量是___ 。
(3)25.4g某二价金属A的氯化物中含有0.4molCl-,则A的摩尔质量为___ 。
(4)现有M、N两种气态化合物,其摩尔质量之比为2:1,将M、N两种气体分别溶于水(M、N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2,则两种溶液的物质的量浓度之比为___ 。
(1)将3.22g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L人造空气的质量是4.8g,其中氧气和氦气的分子数之比是
(3)25.4g某二价金属A的氯化物中含有0.4molCl-,则A的摩尔质量为
(4)现有M、N两种气态化合物,其摩尔质量之比为2:1,将M、N两种气体分别溶于水(M、N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2,则两种溶液的物质的量浓度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列问题:
(1)5.4gH2O中含有__________ mol H。
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO 的物质的量是
的物质的量是________ 。
(3)3.01×1024个OH-与__________ mol NH3的质量相同。
(4)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为__________ 。
(5)一定温度和压强下,3L气体A2与9L气体B2完全化合生成6L气体C,则气体C的化学式为__________ (用A、B表示)。
(1)5.4gH2O中含有
(2)硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO
 的物质的量是
的物质的量是(3)3.01×1024个OH-与
(4)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为
(5)一定温度和压强下,3L气体A2与9L气体B2完全化合生成6L气体C,则气体C的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】取100mL的Na2CO3和Na2SO4混合溶液,加入100 mL Ba(OH)2溶液,恰好完全反应,过滤得到白色沉淀和滤液,沉淀干燥后质量为14.51g。用过量稀盐酸处理上述沉淀,沉淀质量减少到4.66g,并有气体放出。计算:
(1)原混合液中Na2SO4的物质的量浓度为_________ mol ·L-1;
(2)过滤出沉淀后,所得滤液的物质的量浓度为___________ mol ·L-1(设反应前后溶液的密度均为1g·cm-3,且反应前后溶液体积变化忽略不计);
(3)在处理沉淀时产生的气体在标准状况下的体积为____________ L。
(1)原混合液中Na2SO4的物质的量浓度为
(2)过滤出沉淀后,所得滤液的物质的量浓度为
(3)在处理沉淀时产生的气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】沉钴得到的是CoC2O4·2H2O,热重分析实验发现,将该固体在空气中加热会发生如下分解过程:
若制备过程中煅烧控制温度约为340℃,则发生反应的化学方程式是:_______ 。
| 温度范围(℃) | 150~250 | 250~300 | 910~950 |
| 失重率(%) | 19.7 | 36.4 | 2.9 |
若制备过程中煅烧控制温度约为340℃,则发生反应的化学方程式是:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】已知某种气态化石燃料中含有碳和氢两种元素。为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(u形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
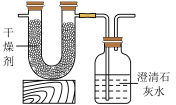
根据实验数据求:
(1)实验完毕后,生成物中水的质量为___ g。假设广口瓶里生成一种正盐,其质量为___ g。
(2)生成的水中氢元素的质量为____ g。
(3)生成的CO2中碳元素的质量为_____ g。
(4)气态化石燃料中碳元素与氢元素的质量比为_________ 。

| 实验前 | 实验后 | |
| (干燥剂+U形管)的质量 | 101.1g | 102.9g |
| (石灰水+广口瓶)的质量 | 312.0g | 314.2g |
根据实验数据求:
(1)实验完毕后,生成物中水的质量为
(2)生成的水中氢元素的质量为
(3)生成的CO2中碳元素的质量为
(4)气态化石燃料中碳元素与氢元素的质量比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】奶粉中蛋白质含量的国家标准是:每100g婴幼儿奶粉中含蛋白质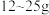 。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取
。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取 该奶粉样品进行反应后,生成的
该奶粉样品进行反应后,生成的 和
和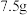 质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于
质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于________ (填“合格”或“不合格”)奶粉。
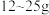 。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取
。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取 该奶粉样品进行反应后,生成的
该奶粉样品进行反应后,生成的 和
和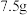 质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于
质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】氧化亚铜 可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将
可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将 和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知:
和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知: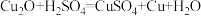 。请计算:
。请计算:
(1)原混合物中 的质量(写出计算过程)
的质量(写出计算过程) _______ 。
(2)在图中画出向20 g 和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据
和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据_______ 。

(3)氧化亚铜可用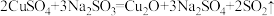 原理制备。
原理制备。
①反应过程中产生 可循环利用,因此应该选用
可循环利用,因此应该选用_______ 溶液来吸收它。
②反应过程中溶液pH将_______ (填“变大”“变小”或“不变”),因此制备过程,要控制溶液的酸碱度,因为如果反应时溶液pH过小,会导致产品下降,原因是_______ 。
 可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将
可用于生产船底防污漆,防止海洋生物对船舶设备的污损。现将 和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知:
和Cu的固体混合物20 g放入烧杯中,加入质量分数为24.5%的稀硫酸50 g,恰好完全反应。已知: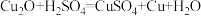 。请计算:
。请计算:(1)原混合物中
 的质量(写出计算过程)
的质量(写出计算过程) (2)在图中画出向20 g
 和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据
和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量变化曲线图,并标明必要的数据
(3)氧化亚铜可用
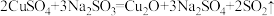 原理制备。
原理制备。①反应过程中产生
 可循环利用,因此应该选用
可循环利用,因此应该选用②反应过程中溶液pH将
您最近一年使用:0次