1 . 标准状况下,多少体积 含
含 个氢原子
个氢原子
 含
含 个氢原子
个氢原子| A.22.4L | B.44.8L | C.11.2L | D.33.6L |
您最近半年使用:0次
2 .  表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.1L0.1mol/L的 溶液中含有的氢离子数为 溶液中含有的氢离子数为 |
B.常温下,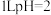 的 的 溶液中含 溶液中含 的数目为 的数目为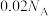 |
C.由  ,若反应放出46.1kJ的热量,则生成 ,若反应放出46.1kJ的热量,则生成 个 个 |
D.氢氧燃料电池装置中,当有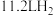 参加反应时,转移的电子数为 参加反应时,转移的电子数为 |
您最近半年使用:0次
名校
3 . 氨广泛应用于化工、化肥、制药等领域,一种新型制备氨的方法如下。下列说法正确的是

| A.反应③为放热反应 |
B. 是该反应的催化剂 是该反应的催化剂 |
C.图中生成目标产物 的反应②为氧化还原反应 的反应②为氧化还原反应 |
D.若生成 物质的量为 物质的量为 ,理论上消耗 ,理论上消耗 为 为 |
您最近半年使用:0次
4 . 硫化钠广泛应用于冶金、染料、皮革、电镀等工业。硫化钠的一种制备方法是
 。设
。设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是

 。设
。设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A.常温常压下,11.2L  中含有的分子数目为0.5 中含有的分子数目为0.5 |
B.0.2 的 的 溶液中含有 溶液中含有 的数目为0.4 的数目为0.4 |
C.常温常压下,1.2g C中含有的质子数目为1.2 |
D.该反应每生成1mol  ,转移电子数目为8 ,转移电子数目为8 |
您最近半年使用:0次
5 . 下列说法正确的是
| A.1.8gH2O中所含电子的数目为6.02×1023 |
| B.标准状况下,22.4LCCl4中含有的氯原子数为4×6.02×1023 |
| C.0.2mol/LAlCl3溶液中Cl-物质的量为0.6mol |
| D.1molFe与足量的盐酸完全反应转移的电子数为3×6.02×1023 |
您最近半年使用:0次
名校
6 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,22.4L氨气中含有的共价键数目为3NA |
| B.将含2molH2SO4的浓硫酸与足量的焦炭反应,转移电子数目为4NA |
| C.含1molHNO3的浓硝酸与足量的Cu反应转移电子数为NA |
D.1L0.1mol/L的氨水中,NH3分子、 分子共0.1NA 分子共0.1NA |
您最近半年使用:0次
7 . 回答下列问题:
(1)碳酸钠在水中的电离方程式___________ 。
(2)药物“胃舒平”中含有氢氧化铝,可用来治疗胃酸(主要成分是盐酸)过多,离子方程式为___________ 。
(3)已知Cl2可发生反应: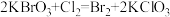 。
。
①氧化产物是___________ (填化学式,下同),还原产物是___________ 。
②氧化剂与还原剂个数比为___________ 。
(4)标准状况下,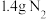 的体积是
的体积是___________ L。
(5)某氯化物MCl227g,含有0.4mol Cl-,则M的相对原子质量为___________ 。
(1)碳酸钠在水中的电离方程式
(2)药物“胃舒平”中含有氢氧化铝,可用来治疗胃酸(主要成分是盐酸)过多,离子方程式为
(3)已知Cl2可发生反应:
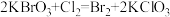 。
。①氧化产物是
②氧化剂与还原剂个数比为
(4)标准状况下,
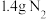 的体积是
的体积是(5)某氯化物MCl227g,含有0.4mol Cl-,则M的相对原子质量为
您最近半年使用:0次
8 . 下列说法正确的是
A.0.5mol  所占体积为11.2L 所占体积为11.2L |
B.标准状况下,1mol 的体积约为22.4L 的体积约为22.4L |
C.标准状况下,14gCO与 的混合气体的体积约为11.2L 的混合气体的体积约为11.2L |
| D.22.4L HCl气体溶于水配成1L溶液,浓度为1 mol/L |
您最近半年使用:0次
名校
9 . 氮化硅陶瓷,被誉为“先进陶瓷材料皇冠上的明珠”。氮化硅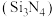 可由石英与焦炭在高温的氮气气流中通过以下反应制备:
可由石英与焦炭在高温的氮气气流中通过以下反应制备: 。设
。设 为阿伏伽德罗常数的值:下列说法正确的是
为阿伏伽德罗常数的值:下列说法正确的是
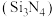 可由石英与焦炭在高温的氮气气流中通过以下反应制备:
可由石英与焦炭在高温的氮气气流中通过以下反应制备: 。设
。设 为阿伏伽德罗常数的值:下列说法正确的是
为阿伏伽德罗常数的值:下列说法正确的是A. 中含 中含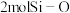 键 键 |
B.每生成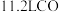 转移电子数目为 转移电子数目为 |
C.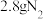 中含有的π键数目为 中含有的π键数目为 |
D.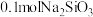 晶体中含离子数目小于 晶体中含离子数目小于 |
您最近半年使用:0次
10 . NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,22gCO2中含有的原子数为1.5NA |
| B.1mol/LNa2SO4溶液中所含钠离子数为2NA |
| C.常温下,1molCl2与足量的稀NaOH溶液反应,转移的电子数为2NA |
| D.标准状况下,22.4L的H2O中含有的H2O分子数为NA |
您最近半年使用:0次



