回答下列问题:
(1)在0.5mol 中,所含硫酸根离子个数共有
中,所含硫酸根离子个数共有___________ 。
(2)标准状况下,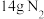 所占有的体积为
所占有的体积为___________ 。
(3)标准状况下,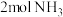 与
与___________ 
 的体积相等。
的体积相等。
(4) 和
和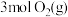 的质量之比
的质量之比___________ ,体积之比为___________ 。
(5)两份质量相等的 和
和 ,物质的量之比
,物质的量之比___________ ,所含氧原子数目之比为___________
(1)在0.5mol
 中,所含硫酸根离子个数共有
中,所含硫酸根离子个数共有(2)标准状况下,
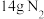 所占有的体积为
所占有的体积为(3)标准状况下,
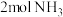 与
与
 的体积相等。
的体积相等。(4)
 和
和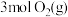 的质量之比
的质量之比(5)两份质量相等的
 和
和 ,物质的量之比
,物质的量之比
更新时间:2021-11-08 22:36:09
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)3.01×1023个CO2分子中含______ mol氧原子,在标准状况下其体积为____ L,0.4 molOH-的中有______ 个电子。
(2)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量为________ 。
(3)同温同压下,等质量的N2和CO2所含分子数比为_____ ,体积比为________ 。
(4)某气体在标准状况下的密度为1.25g/L,则28g该气体所含有的分子数为________ 。
(5)用98%的浓硫酸(ρ=1.84 g/cm3)配制1 mol/L的稀硫酸l00mL,配制过程中需量取浓硫酸____ mL。
(1)3.01×1023个CO2分子中含
(2)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量为
(3)同温同压下,等质量的N2和CO2所含分子数比为
(4)某气体在标准状况下的密度为1.25g/L,则28g该气体所含有的分子数为
(5)用98%的浓硫酸(ρ=1.84 g/cm3)配制1 mol/L的稀硫酸l00mL,配制过程中需量取浓硫酸
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】元素R的气态氢化物的化学式为HXR,在标准状况下,8.5gHXR气体的体积是5.6L,将5.1gHXR气体通入200mL 0.75mol/L的CuCl2溶液正好完全反应(非氧化还原反应,生成铜盐沉淀)
(1)求HXR的相对分子质量______________ 。
(2)推测X值为________ ,并确定R的元素符号_________ 。
(1)求HXR的相对分子质量
(2)推测X值为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)标准状况下,1.7 g NH3与 ________ L H2S气体含有的氢原子数相同。
(2)标准状况下,1.6g某气态氧化物RO2体积为0.56L,该气体的物质的量为_____ mol,RO2的相对分子质量为________ 。
(3)液态化合物在一定量的氧气中恰好完全燃烧,反应方程式为:XY2(l)+3O2(g)=XO2(g)+2YO2(g)冷却后,在标准状况下测得生成物的体积是336 mL,密度是2.56 g/L.
①反应前O2的体积是_____ mL(标准状况),化合物XY2的摩尔质量是_____ 。
②若XY2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为_____ 和_____ (写元素符号)。
(4)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________ (注:体积分数即为物质的量分数)
(5)在一定温度下,有摩尔质量为Mg/mol的某物质溶于适量的水中,得到物质的量浓度为c mol/L,密度为ρ g/mL的饱和溶液,则该温度下此物质的溶解度为____ 。
(2)标准状况下,1.6g某气态氧化物RO2体积为0.56L,该气体的物质的量为
(3)液态化合物在一定量的氧气中恰好完全燃烧,反应方程式为:XY2(l)+3O2(g)=XO2(g)+2YO2(g)冷却后,在标准状况下测得生成物的体积是336 mL,密度是2.56 g/L.
①反应前O2的体积是
②若XY2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为
(4)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(5)在一定温度下,有摩尔质量为Mg/mol的某物质溶于适量的水中,得到物质的量浓度为c mol/L,密度为ρ g/mL的饱和溶液,则该温度下此物质的溶解度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)在25℃、101 kPa的条件下,相同质量的CH4和A气体的体积之比是15:8,则A的摩尔质量为___ 。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4:11,则A的摩尔质量为___ 。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4:11,则A的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)在标准状况下①6.72L CH4②3.01×1023个HCl分子③ 13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是_____
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
(2)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g。则其中CO2为________ mol, CO占总体积的______ (保留一位小数),混合气体的摩尔质量为_______ (保留一位小数)。
(3)某混合气体中各气体的质量分数为:O232%,N228%,CO222%,CH416%,H22%,则此混合气体的平均摩尔质量为______ (保留两位小数)。
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
(2)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g。则其中CO2为
(3)某混合气体中各气体的质量分数为:O232%,N228%,CO222%,CH416%,H22%,则此混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】取 100mL18.3 mol/L 的 H2SO4 与 Zn 反应,当 Zn 完全溶解时,生成气体为22.4L(标准状况),将所得溶液稀释成 1L,测得溶液中H+浓度为 1 mol/L。
①反应转移的电子数目为_________ 。
②消耗硫酸的物质的量为__________ 。
③则所得气体中SO2 和 H2 的体积比约为___________ 。
①反应转移的电子数目为
②消耗硫酸的物质的量为
③则所得气体中SO2 和 H2 的体积比约为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】计算下列各数值。
(1)3.1g Na2X含有Na+ 为0.1mol,则Na2X的摩尔质量为__ ,X的相对原子质量为__ 。
(2)8.5g氢氧根离子含有的电子数目为_______ 。
(3)14g C2H4与C4H8的混合物所含质子的物质的量为__ 。
(4)1.43g Na2CO3·10H2O溶于水配成100mL溶液,则c(Na2CO3)为__ mol/L;取20mL该溶液,加入__ mL水得到0.004mol/L的Na2CO3溶液(设稀释时对溶液体积的影响忽略不计)。
(1)3.1g Na2X含有Na+ 为0.1mol,则Na2X的摩尔质量为
(2)8.5g氢氧根离子含有的电子数目为
(3)14g C2H4与C4H8的混合物所含质子的物质的量为
(4)1.43g Na2CO3·10H2O溶于水配成100mL溶液,则c(Na2CO3)为
您最近一年使用:0次



