1 . 下列离子方程式正确的是
A.向 溶液中加入过量氮水: 溶液中加入过量氮水: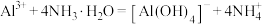 |
B.向 溶液中加入氯化铁溶液: 溶液中加入氯化铁溶液: |
C.将过量 通入“84”消毒液中: 通入“84”消毒液中: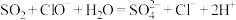 |
D.向碳酸氢铵溶液中加入少量氢氧化钠溶液: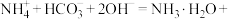  |
您最近半年使用:0次
名校
解题方法
2 . 向含有Fe3+、Fe2+、Cu2+的蚀刻铜箔回收液中,加入一定量铁粉,反应一段时间后,对反应后的混合物进行分析,下列说法错误的是
| A.若有固体剩余,则该固体一定含有Cu |
| B.若有固体剩余,则该溶液可能含有Cu2+ |
| C.若无固体剩余,则该溶液不可能含有Fe3+ |
| D.无论固体是否剩余,该溶液中一定含有Fe2+ |
您最近半年使用:0次
解题方法
3 . 某同学欲探究铁及其化合物的性质,下列实验方案可行的是
| A.将铁粉加入热的浓硫酸中:探究铁的活泼性 |
B.将热的NaOH溶液滴入 溶液中:制备 溶液中:制备 胶体 胶体 |
C.将铜粉加入 溶液中:验证 溶液中:验证 的氧化性强于 的氧化性强于 |
D.在蒸发皿中加热蒸干 溶液:制备 溶液:制备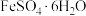 晶体 晶体 |
您最近半年使用:0次
解题方法
4 . 下列离子能大量共存的是
A.无色酚酞试液呈红色的溶液中: 、 、 、 、 、 、 |
B.无色透明的溶液中: 、 、 、 、 、 、 |
C.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
名校
5 . A、B是短周期元素m、n组成的常见二元化合物(原子序数m<n),常温下均为气体。X是一种能被磁铁吸引的金属单质,C、D、E为化合物。上述物质的转化关系如图所示。下列说法错误的是
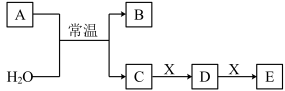
| A.元素的非金属性m<n |
| B.常温下,C的浓溶液与X不反应 |
| C.B可通过化合反应生成A |
D.D→E的离子方程式为: |
您最近半年使用:0次
名校
6 . 下列离子方程式书写正确的是
A.向NaClO溶液中通入足量SO2气体:ClO-+SO2+H2O=Cl-+ +2H+ +2H+ |
B.NO2气体通入足量NaOH溶液中:NO2+2OH-= +H2O +H2O |
C.向氯化铝溶液中滴加过量氨水:4NH3•H2O+Al3+= +4 +4 +2H2O +2H2O |
| D.向Fe(OH)3加入氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O |
您最近半年使用:0次
7 . Fe3S4固体是一种重要的磁性材料,以它为原料实现如下化合物的转化: 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。
请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为___________ ,无色酸性溶液F中的含硫阴离子有___________ 。
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式___________ 。
(3)下列说法正确的是___________。
(4)写出F→G反应的化学方程式___________ 。请设计实验方案确定溶液G中的阴离子___________ 。

 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式
(3)下列说法正确的是___________。
| A.固体A中可能含有FeO | B.无色气体E能完全溶于水 |
| C.溶液C呈酸性,是由于Fe3+水解 | D.溶液B可溶解铜 |
(4)写出F→G反应的化学方程式
您最近半年使用:0次
解题方法
8 .  在现代工业生产中应用广泛,查阅资料得:无水
在现代工业生产中应用广泛,查阅资料得:无水 在空气中易潮解,加热易升华。
在空气中易潮解,加热易升华。
(1)用丁达尔效应鉴别 胶体和
胶体和 溶液的操作是
溶液的操作是____________ (写出具体实验操作、结论)。
(2)电子工业中用 溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出
溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:__________________ 。该反应的还原剂是______ 。
(3)硫化氢( )是一种有毒的气体,可用
)是一种有毒的气体,可用 溶液吸收,生成单质硫(S)沉淀。
溶液吸收,生成单质硫(S)沉淀。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为____________ 。该反应中氧化产物与还原产物的物质的量之比为______ 。
(4)某小组同学设计了制备无水) 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
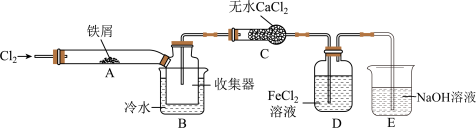
步骤Ⅰ.检验装置的气密性;
步骤Ⅱ.通入干燥的 ,赶尽装置中的空气;
,赶尽装置中的空气;
步骤Ⅲ.用酒精灯在铁屑下方加热至反应完成;
步骤Ⅳ.体系冷却后,停止通入 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。
①装置A中发生反应的化学方程式为__________________ 。
②装置B中冷水浴的作用为____________ 。
 在现代工业生产中应用广泛,查阅资料得:无水
在现代工业生产中应用广泛,查阅资料得:无水 在空气中易潮解,加热易升华。
在空气中易潮解,加热易升华。(1)用丁达尔效应鉴别
 胶体和
胶体和 溶液的操作是
溶液的操作是(2)电子工业中用
 溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出
溶液腐蚀敷在绝缘板上的铜,从而制造印刷电路板,写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(3)硫化氢(
 )是一种有毒的气体,可用
)是一种有毒的气体,可用 溶液吸收,生成单质硫(S)沉淀。
溶液吸收,生成单质硫(S)沉淀。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为(4)某小组同学设计了制备无水)
 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
步骤Ⅰ.检验装置的气密性;
步骤Ⅱ.通入干燥的
 ,赶尽装置中的空气;
,赶尽装置中的空气;步骤Ⅲ.用酒精灯在铁屑下方加热至反应完成;
步骤Ⅳ.体系冷却后,停止通入
 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。①装置A中发生反应的化学方程式为
②装置B中冷水浴的作用为
您最近半年使用:0次
9 . 工业上常用绿矾(FeSO4•7H2O)作还原剂。
(1)检验久置绿矾是否变质可用试剂______ 。
(2)①工业上常用FeCl3溶液刻蚀铜电路板,反应的离子方程式为_______ 。
腐蚀废液含FeCl2、FeCl3、CuCl2,某小组欲从腐蚀废液中回收铜及制绿矾,工艺流程如图:
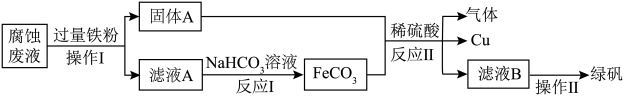
②操作I中使用的玻璃仪器除烧杯、玻璃棒外还有______ ;腐蚀废液中加入过量铁粉的目的______ 。
③固体A中含有______ 。
④反应I中生成FeCO3沉淀同时有CO2和水生成,反应的离子方程式为:_______ 。
(3)如何检验滤液A中含有Fe2+?______ 。
(1)检验久置绿矾是否变质可用试剂
(2)①工业上常用FeCl3溶液刻蚀铜电路板,反应的离子方程式为
腐蚀废液含FeCl2、FeCl3、CuCl2,某小组欲从腐蚀废液中回收铜及制绿矾,工艺流程如图:

②操作I中使用的玻璃仪器除烧杯、玻璃棒外还有
③固体A中含有
④反应I中生成FeCO3沉淀同时有CO2和水生成,反应的离子方程式为:
(3)如何检验滤液A中含有Fe2+?
您最近半年使用:0次
名校
10 . 学习元素周期律后,可以利用元素在周期表中位置解释及预测陌生元素的部分性质。
例如 、
、 、
、 是同族元素,性质有一定的相似性,存在多种价态的阳离子;
是同族元素,性质有一定的相似性,存在多种价态的阳离子; 元素原子半径与
元素原子半径与 元素原子半径很接近,因此它们的化学性质有一定的相似性。
元素原子半径很接近,因此它们的化学性质有一定的相似性。
在利用炼锌钴渣[主要含 、
、 、
、 和
和 、
、 单质]协同制备
单质]协同制备 和高纯
和高纯 的流程中,借助元素周期律分析其原理。流程如下:
的流程中,借助元素周期律分析其原理。流程如下:
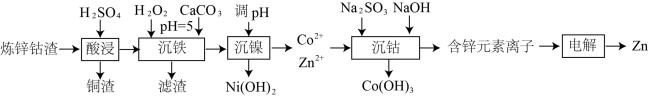
(1)“酸浸”过程产生的铜渣用 溶液溶解后回收利用,溶解时发生反应的离子方程式为
溶液溶解后回收利用,溶解时发生反应的离子方程式为_______ 。
(2)“酸浸”过程 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)“沉铁”过程, 时
时 、
、 、
、 不沉淀,
不沉淀, 的作用是
的作用是_______ 。
(4)“沉镍”过程 对溶液中
对溶液中 、
、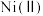 含量的影响如图。由图判断,应调节
含量的影响如图。由图判断,应调节
_______ 。
(5) 、
、 、
、 在周期表中位置是
在周期表中位置是_______ , ,
, 都具有氧化性,结合以上流程信息比较氧化性:
都具有氧化性,结合以上流程信息比较氧化性:
_______  (填“>”或“<”)。
(填“>”或“<”)。
(6)“沉钴”过程,加入 溶液,其中硫元素为+6价,生成
溶液,其中硫元素为+6价,生成 的离子方程式为
的离子方程式为_______ 。
(7)“沉钴”过程中, 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
例如
 、
、 、
、 是同族元素,性质有一定的相似性,存在多种价态的阳离子;
是同族元素,性质有一定的相似性,存在多种价态的阳离子; 元素原子半径与
元素原子半径与 元素原子半径很接近,因此它们的化学性质有一定的相似性。
元素原子半径很接近,因此它们的化学性质有一定的相似性。在利用炼锌钴渣[主要含
 、
、 、
、 和
和 、
、 单质]协同制备
单质]协同制备 和高纯
和高纯 的流程中,借助元素周期律分析其原理。流程如下:
的流程中,借助元素周期律分析其原理。流程如下:
(1)“酸浸”过程产生的铜渣用
 溶液溶解后回收利用,溶解时发生反应的离子方程式为
溶液溶解后回收利用,溶解时发生反应的离子方程式为(2)“酸浸”过程
 发生反应的离子方程式为
发生反应的离子方程式为(3)“沉铁”过程,
 时
时 、
、 、
、 不沉淀,
不沉淀, 的作用是
的作用是(4)“沉镍”过程
 对溶液中
对溶液中 、
、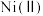 含量的影响如图。由图判断,应调节
含量的影响如图。由图判断,应调节

(5)
 、
、 、
、 在周期表中位置是
在周期表中位置是 ,
, 都具有氧化性,结合以上流程信息比较氧化性:
都具有氧化性,结合以上流程信息比较氧化性:
 (填“>”或“<”)。
(填“>”或“<”)。(6)“沉钴”过程,加入
 溶液,其中硫元素为+6价,生成
溶液,其中硫元素为+6价,生成 的离子方程式为
的离子方程式为(7)“沉钴”过程中,
 与
与 反应的离子方程式为
反应的离子方程式为
您最近半年使用:0次



