名校
1 . 氮元素是生命物质中重要的组成元素之一,氮气经过一系列的变化可以生成氨、氮的氧化物、硝酸等重要的化工原料。工业合成氨是人类科学技术的一项重大突破,其合成原理为
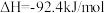 。实验室中可通过铵盐与强碱共热制取少量的
。实验室中可通过铵盐与强碱共热制取少量的 并验证其性质。下列离子方程式或化学方程式书写正确的是
并验证其性质。下列离子方程式或化学方程式书写正确的是

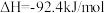 。实验室中可通过铵盐与强碱共热制取少量的
。实验室中可通过铵盐与强碱共热制取少量的 并验证其性质。下列离子方程式或化学方程式书写正确的是
并验证其性质。下列离子方程式或化学方程式书写正确的是A.印刷电路板: |
B.铁与稀硝酸: |
C. 溶液中通 溶液中通 : : |
D. 溶液吸收 溶液吸收 : : |
您最近半年使用:0次
名校
解题方法
2 . 组装如图实验装置,检验装置气密性后,添加药品,将铜丝插入浓硝酸中开始实验。下列说法错误的是
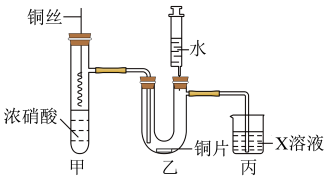
| A.实验中可以利用铜丝的上下移动来控制反应的发生和停止 |
| B.一段时间后抽出铜丝,向乙中注入水,气体颜色会变浅 |
C.注入水后装置乙中铜片表面产生气泡,说明反应生成 |
| D.丙中X溶液可以是NaOH溶液,以吸收尾气 |
您最近半年使用:0次
7日内更新
|
118次组卷
|
2卷引用:福建省晋江市养正中学2023-2024学年高一下学期3月第一次月考化学试题
名校
3 . 工业上利用图1流程制备的亚硝酸钠中常含有一定量的硝酸钠杂质,二者的溶解度随温度变化如图2所示。下列说法正确的是
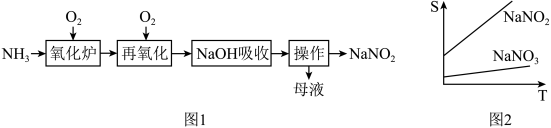

A.氧化炉中发生反应的化学方程式为: |
B.再氧化时氧气用量越多 产率越高 产率越高 |
| C.操作为蒸发浓缩、趁热过滤 |
D. 保护条件下,低温蒸干母液所得固体主要是 保护条件下,低温蒸干母液所得固体主要是 |
您最近半年使用:0次
解题方法
4 . 部分含氮物质的分类与相应化合价的关系如图所示。下列说法不正确的是
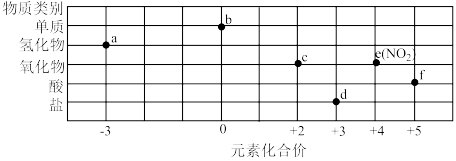
| A.实验室可用排水法收集e |
B. 属于人工固氮的过程 属于人工固氮的过程 |
| C.将c和e通入到强碱溶液中,可生成d |
| D.工业上可用气体a、空气和水为原料生产f |
您最近半年使用:0次
名校
解题方法
5 . 实验室可用如图所示装置(夹持、加热装置略去)制备一定量的草酸(H2C2O4)。其中制备原理为C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O。

| A.淀粉的分子式为(C6H12O6)n |
| B.装置A反应中每生成1molH2C2O4转移电子的物质的量为12mol |
| C.实验时在装置C中充入O2的目的是将NO2和NO充分转化为HNO3 |
| D.向反应后的装置A中滴加NaHCO3溶液,有气泡产生,说明酸性H2C2O4大于H2CO3 |
您最近半年使用:0次
名校
解题方法
6 . 低温等离子体(NTP)技术可有效脱除烟气中的NO,其原理是在高压放电条件下,O2产生自由基(O-),自由基将NO氧化为NO2,再用Na2CO3溶液吸收,实验装置如图所示。已知:
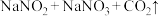 ,下列说法错误的是
,下列说法错误的是

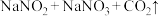 ,下列说法错误的是
,下列说法错误的是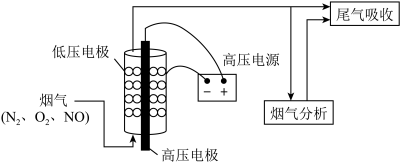
| A.增大烟气流速不可提高NO脱除率 |
| B.氮元素既有被氧化的过程又有被还原的过程 |
| C.高压电源的功率越大,烟气中NO的脱除效果一定越好 |
| D.单位时间内生成的自由基(O-)越多,越有利于NO的转化 |
您最近半年使用:0次
名校
7 . 下列离子方程式书写正确的是
A.向NaClO溶液中通入足量SO2气体:ClO-+SO2+H2O=Cl-+ +2H+ +2H+ |
B.NO2气体通入足量NaOH溶液中:NO2+2OH-= +H2O +H2O |
C.向氯化铝溶液中滴加过量氨水:4NH3•H2O+Al3+= +4 +4 +2H2O +2H2O |
| D.向Fe(OH)3加入氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O |
您最近半年使用:0次
8 . N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。
N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为___________ 。
(2)NO和NO2的处理。
已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应原理如下:
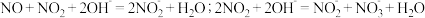
①下列措施一定能提高尾气中NO和NO2去除率的有___________ (填字母)。
A.采用气、液逆流的方式吸收尾气 B.提高吸收液的温度
C.加快通入尾气的速率 D.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,其中主要杂质是___________ (填化学式),吸收后排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示: ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(1)N2O的处理。
N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。
已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应原理如下:
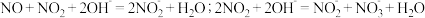
①下列措施一定能提高尾气中NO和NO2去除率的有
A.采用气、液逆流的方式吸收尾气 B.提高吸收液的温度
C.加快通入尾气的速率 D.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,其中主要杂质是
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近半年使用:0次
名校
9 . 铜和硝酸的反应实验是体现硝酸重要性质的实验,某教师设计了如图装置进行铜和稀硝酸的反应实验,步骤如下:
步骤ⅰ.将弹簧状细铜丝放入注射器 底部并固定,注射器
底部并固定,注射器 吸入少量蒸馏水后将活塞推至最低处;注射器
吸入少量蒸馏水后将活塞推至最低处;注射器 吸取
吸取 溶液(过量),注射器
溶液(过量),注射器 于烧杯中吸取
于烧杯中吸取 稀硝酸,注射器
稀硝酸,注射器 吸取
吸取 (过量)。
(过量)。
步骤ⅱ.按图连接好装置,打开止水夹 、
、 ,关闭
,关闭 、
、 ,将注射器
,将注射器 中的稀硝酸注入
中的稀硝酸注入 中。
中。
步骤ⅲ.关闭止水夹 ,打开止水夹
,打开止水夹 ,抽动注射器
,抽动注射器 的活塞,将注射器
的活塞,将注射器 中生成的
中生成的 气体全部抽入
气体全部抽入 中。
中。
步骤ⅳ.关闭止水夹 ,打开止水夹
,打开止水夹 ,将注射器
,将注射器 中气体全部抽入
中气体全部抽入 中。
中。 、
、 的容积为
的容积为 ,注射器
,注射器 、
、 的容积为
的容积为 ;②止水夹
;②止水夹 、
、 、
、 、
、 连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有
连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有 。
。
请回答下列问题:
(1)步骤ⅰ中注射器 吸入少量蒸馏水后将活塞推至最低处的目的是
吸入少量蒸馏水后将活塞推至最低处的目的是______ ;步骤ⅱ注射器 中的稀硝酸注入
中的稀硝酸注入 中时发生反应的化学方程式为
中时发生反应的化学方程式为______ ,观察到的现象为______ ,该反应中稀硝酸体现了______ (填化学性质)。
(2)步骤ⅲ将注射器 中生成的气体全部抽入
中生成的气体全部抽入 中,注射器
中,注射器 中能观察到的现象为
中能观察到的现象为______ ;该过程中, 发生了
发生了______ (填“氧化”或“还原”)反应。
(3)步骤ⅳ将注射器 中气体全部抽入
中气体全部抽入 中,
中, 和
和 的混合气体与
的混合气体与 溶液反应生成的盐只有
溶液反应生成的盐只有 ,该反应的离子方程式为
,该反应的离子方程式为______ ,该反应中氧化剂和氧化产物的物质的量之比为______ 。
(4)若反应过程中有 铜丝参与反应,要使注射器
铜丝参与反应,要使注射器 中产生的
中产生的 最终在注射器
最终在注射器 中全部转化为
中全部转化为 ,需要消耗
,需要消耗______  。
。
步骤ⅰ.将弹簧状细铜丝放入注射器
 底部并固定,注射器
底部并固定,注射器 吸入少量蒸馏水后将活塞推至最低处;注射器
吸入少量蒸馏水后将活塞推至最低处;注射器 吸取
吸取 溶液(过量),注射器
溶液(过量),注射器 于烧杯中吸取
于烧杯中吸取 稀硝酸,注射器
稀硝酸,注射器 吸取
吸取 (过量)。
(过量)。步骤ⅱ.按图连接好装置,打开止水夹
 、
、 ,关闭
,关闭 、
、 ,将注射器
,将注射器 中的稀硝酸注入
中的稀硝酸注入 中。
中。步骤ⅲ.关闭止水夹
 ,打开止水夹
,打开止水夹 ,抽动注射器
,抽动注射器 的活塞,将注射器
的活塞,将注射器 中生成的
中生成的 气体全部抽入
气体全部抽入 中。
中。步骤ⅳ.关闭止水夹
 ,打开止水夹
,打开止水夹 ,将注射器
,将注射器 中气体全部抽入
中气体全部抽入 中。
中。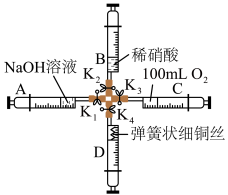
 、
、 的容积为
的容积为 ,注射器
,注射器 、
、 的容积为
的容积为 ;②止水夹
;②止水夹 、
、 、
、 、
、 连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有
连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有 。
。请回答下列问题:
(1)步骤ⅰ中注射器
 吸入少量蒸馏水后将活塞推至最低处的目的是
吸入少量蒸馏水后将活塞推至最低处的目的是 中的稀硝酸注入
中的稀硝酸注入 中时发生反应的化学方程式为
中时发生反应的化学方程式为(2)步骤ⅲ将注射器
 中生成的气体全部抽入
中生成的气体全部抽入 中,注射器
中,注射器 中能观察到的现象为
中能观察到的现象为 发生了
发生了(3)步骤ⅳ将注射器
 中气体全部抽入
中气体全部抽入 中,
中, 和
和 的混合气体与
的混合气体与 溶液反应生成的盐只有
溶液反应生成的盐只有 ,该反应的离子方程式为
,该反应的离子方程式为(4)若反应过程中有
 铜丝参与反应,要使注射器
铜丝参与反应,要使注射器 中产生的
中产生的 最终在注射器
最终在注射器 中全部转化为
中全部转化为 ,需要消耗
,需要消耗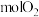 。
。
您最近半年使用:0次
2024-04-11更新
|
53次组卷
|
3卷引用:江西省部分地区2023-2024学年高一下学期3月月考化学试题
10 . “环境是民生,青山是美丽,蓝天也是幸福”。对生态环境污染问题,我们必须正视问题、着力解决问题。
Ⅰ.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体)污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是______ 。
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示:______ 。
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式______ 。
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: 。若反应时消耗了10L
。若反应时消耗了10L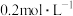 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量______ mol。
Ⅱ.硫有多种化合物,如H2S、SO2等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(5)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:______ 。
(6)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成 而实现SO2的回收利用,写出Fe3+将SO2氧化成
而实现SO2的回收利用,写出Fe3+将SO2氧化成 反应的离子方程式
反应的离子方程式______ 。
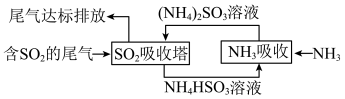
(7)某企业利用下列流程综合处理工厂排放的含;SO2的烟气,以减少其对环境造成的污染。“SO2吸收塔”中发生反应的化学方程式为______ ,该流程中可循环利用的物质为______ (填化学式)。
Ⅰ.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体)污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示:
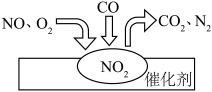
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 。若反应时消耗了10L
。若反应时消耗了10L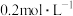 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量Ⅱ.硫有多种化合物,如H2S、SO2等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(5)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:

(6)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成
 而实现SO2的回收利用,写出Fe3+将SO2氧化成
而实现SO2的回收利用,写出Fe3+将SO2氧化成 反应的离子方程式
反应的离子方程式(7)某企业利用下列流程综合处理工厂排放的含;SO2的烟气,以减少其对环境造成的污染。“SO2吸收塔”中发生反应的化学方程式为
您最近半年使用:0次



