氮的化合物是化学研究的热点之一,请回答下列问题:
(1)汽车尾气中的 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式_______ ,并用双线桥法标出电子转移的方向和数目。
(2)氮氧化物是造成雾霾天气的主要原因之一,利用 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下:
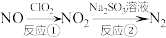
反应①的化学方程式是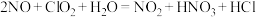 ,反应②的离子方程式是
,反应②的离子方程式是_______ ;若有1.4g 生成,需消耗
生成,需消耗
_______ g。
亚硝酸钠有咸味,有毒。已知: 。
。
(3)上述反应的还原剂为_______ (填化学式);若反应中有1分子 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为_______ 。
(4)在酸性条件下,高锰酸钾可将 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:_______ 。
(1)汽车尾气中的
 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式(2)氮氧化物是造成雾霾天气的主要原因之一,利用
 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下: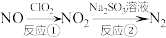
反应①的化学方程式是
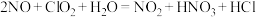 ,反应②的离子方程式是
,反应②的离子方程式是 生成,需消耗
生成,需消耗
亚硝酸钠有咸味,有毒。已知:
 。
。(3)上述反应的还原剂为
 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为(4)在酸性条件下,高锰酸钾可将
 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:
更新时间:2023-10-15 15:51:00
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】I.通过计算填写下列内容:
(1)在标准状况下,6.72LCO的物质的量为_______ ;
(2)在标准状况下,23gC2H5OH的氢原子数目为_______ NA;
(3)7.8 gNa2X中含有Na+0.2 mol,则Na2X的摩尔质量为_______ g/mol;
(4)100mLAl2(SO4)3和MgSO4的混合溶液中,含有Mg2+0.24g, SO 的物质的量浓度为0.7mol/L,则Al3+的物质的量浓度为
的物质的量浓度为0.7mol/L,则Al3+的物质的量浓度为_______ mol/L。
(5)配制500mL 1mol/L的稀硫酸,需取5 mol/L的硫酸_______ mL。
II.分类是学习化学的重要方法,以物质的元素组成和化学性质视角对物质进行科学分类,可体现化学学科独有的魅力。有下列物质:①SO2 ②水银 ③Na2O固体 ④稀硫酸 ⑤碳酸氢钠固体 ⑥酒精 ⑦熔融的KNO3 ⑧蔗糖 ⑨Fe(OH)3胶体
请回答下列问题:
(6)上述物质中属于电解质的是_______ ;
(7)将⑤中固体加热的反应化学方程式是_______ ;
(8)制备⑨的离子反应方程式是_______ 。
(1)在标准状况下,6.72LCO的物质的量为
(2)在标准状况下,23gC2H5OH的氢原子数目为
(3)7.8 gNa2X中含有Na+0.2 mol,则Na2X的摩尔质量为
(4)100mLAl2(SO4)3和MgSO4的混合溶液中,含有Mg2+0.24g, SO
 的物质的量浓度为0.7mol/L,则Al3+的物质的量浓度为
的物质的量浓度为0.7mol/L,则Al3+的物质的量浓度为(5)配制500mL 1mol/L的稀硫酸,需取5 mol/L的硫酸
II.分类是学习化学的重要方法,以物质的元素组成和化学性质视角对物质进行科学分类,可体现化学学科独有的魅力。有下列物质:①SO2 ②水银 ③Na2O固体 ④稀硫酸 ⑤碳酸氢钠固体 ⑥酒精 ⑦熔融的KNO3 ⑧蔗糖 ⑨Fe(OH)3胶体
请回答下列问题:
(6)上述物质中属于电解质的是
(7)将⑤中固体加热的反应化学方程式是
(8)制备⑨的离子反应方程式是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】根据所学知识填空
(1)1.0molH2O中,氢原子与氧原子个数之比为___________ 。
(2)1.204×1023个CO2分子的物质的量为___________ mol。
(3)1molOH-中含有___________ mol电子。
(4)在标准状况下,由CO和CO2组成的混合气体22.4L,质量是40g。此混合物中CO和CO2的物质的量比是___________ 。
(5)写出FeCl2溶液中通入Cl2的离子方程式___________ 。
(1)1.0molH2O中,氢原子与氧原子个数之比为
(2)1.204×1023个CO2分子的物质的量为
(3)1molOH-中含有
(4)在标准状况下,由CO和CO2组成的混合气体22.4L,质量是40g。此混合物中CO和CO2的物质的量比是
(5)写出FeCl2溶液中通入Cl2的离子方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题。
(1)工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

①由图可知SCR技术中的氧化剂为____ 。
②用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1:1时,写出该反应的化学方程式:_______ 。
(2)ClO2气体是一种常用的消毒剂,现在被广泛用于饮用水消毒。自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg/L。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样用微量的氢氧化钠溶液调至中性,然后加入一定量的碘化钾,并加入淀粉溶液,溶液变蓝
Ⅱ.加入一定量的Na2S2O3溶液(已知:2S2O32-+I2=S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1.3。
已知:ClO2在中性条件下还原产物为ClO2-,在酸性条件下还原产物为Cl-。请回答下列问题:
①确定操作Ⅱ完全反应的现象为________ 。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式为______ 。
③若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol/L的Na2S2O3溶液10 mL,则水样中ClO2的浓度是____ mg/L。
(1)工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

①由图可知SCR技术中的氧化剂为
②用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1:1时,写出该反应的化学方程式:
(2)ClO2气体是一种常用的消毒剂,现在被广泛用于饮用水消毒。自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg/L。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样用微量的氢氧化钠溶液调至中性,然后加入一定量的碘化钾,并加入淀粉溶液,溶液变蓝

Ⅱ.加入一定量的Na2S2O3溶液(已知:2S2O32-+I2=S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1.3。
已知:ClO2在中性条件下还原产物为ClO2-,在酸性条件下还原产物为Cl-。请回答下列问题:
①确定操作Ⅱ完全反应的现象为
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式为
③若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol/L的Na2S2O3溶液10 mL,则水样中ClO2的浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】已知 ,该反应常用于实验室常温下制氯气。
,该反应常用于实验室常温下制氯气。
(1)请用双线桥法标出该反应的电子转移的方向和数目_______________________________ 。
(2)该反应中,氧化剂是________ ,氧化产物是________ 。
(3)当反应中有3mol电子发生转移时,则参加反应的HCl的物质的量为________ mol。生成物中氧化产物的质量比还原产物的质量多________ g。
 ,该反应常用于实验室常温下制氯气。
,该反应常用于实验室常温下制氯气。(1)请用双线桥法标出该反应的电子转移的方向和数目
(2)该反应中,氧化剂是
(3)当反应中有3mol电子发生转移时,则参加反应的HCl的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】配平并完成方程式。
(1)_____ Pt+ _____ HNO3+ _____ HCl
_____ H2PtCl6+_____ NO↑+_____ ( )
(2)_____ Fe+ _____ HNO3(稀)
_____ Fe(NO3)3+ _____ NO↑+ _____ H2O,被还原与未被还原的氮元素质量之比__________ 。
(3)_____ Cu2S+_____ HNO3
_____ Cu(NO3)2+ _____ NO↑+_____ S↓+ _____ H2O,被还原与未被还原硝酸物质的量之比是_______ 被还原的元素是_____ 。
(1)

(2)

(3)

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】已知KMnO4与浓盐酸反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+8H2O+2KCl+5Cl2↑,回答下列问题:
(1)请用双线桥表示出该反应转移电子的方向和数目_______________________________
(2)被氧化的HCl占HCl总量的_______ 被还原的元素_________ (填元素符号)
(3)当标准状况下有0.5mol氯气生成时,该反应转移的电子数为_____ (设NA为阿伏加 德罗常数的值)
(4)15.8g KMnO4与含1.2molHCl的浓盐酸完全反应(假设HCl无挥发),在反应后的溶液中加入足量的AgNO3溶液,可生成_____ g沉淀.
(1)请用双线桥表示出该反应转移电子的方向和数目
(2)被氧化的HCl占HCl总量的
(3)当标准状况下有0.5mol氯气生成时,该反应转移的电子数为
(4)15.8g KMnO4与含1.2molHCl的浓盐酸完全反应(假设HCl无挥发),在反应后的溶液中加入足量的AgNO3溶液,可生成
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在加热条件下,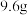 铜丝与
铜丝与 的硝酸恰好完全反应,产生一定量
的硝酸恰好完全反应,产生一定量 和
和 的混合气体(反应过程中溶液体积变化忽略不计)。
的混合气体(反应过程中溶液体积变化忽略不计)。
(1)硝酸铜物质的量浓度为_______  。
。
(2)整个过程中被还原的硝酸物质的量为_______  。
。
(3)混合气体中 的体积为
的体积为_______  。(标准状况下)
。(标准状况下)
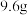 铜丝与
铜丝与 的硝酸恰好完全反应,产生一定量
的硝酸恰好完全反应,产生一定量 和
和 的混合气体(反应过程中溶液体积变化忽略不计)。
的混合气体(反应过程中溶液体积变化忽略不计)。(1)硝酸铜物质的量浓度为
 。
。(2)整个过程中被还原的硝酸物质的量为
 。
。(3)混合气体中
 的体积为
的体积为 。(标准状况下)
。(标准状况下)
您最近一年使用:0次
【推荐2】把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:_______ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:_______ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:
您最近一年使用:0次

 2MO+4NO2↑+O2↑,加热29.6gM(NO3)2使其完全分解,在标准状况下收集2.24L的O2,则M的摩尔质量是?
2MO+4NO2↑+O2↑,加热29.6gM(NO3)2使其完全分解,在标准状况下收集2.24L的O2,则M的摩尔质量是?

