广东北江实验学校2023—2024学年高一上学期10月月考化学试题
广东
高一
阶段练习
2024-03-16
23次
整体难度:
适中
考查范围:
认识化学科学、初中衔接知识点、常见无机物及其应用、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
| A.科学家成功将二氧化碳转化为淀粉 | B.切开的苹果放置一段时间后切面变色 |
| C.利用干冰制冷保冰棒 | D.厨余垃圾“变身”为沼气 |
| 选项 | 酸性氧化物 | 酸 | 盐 | 电解质 | 非电解质 |
| A | SiO2 | HCl | 纯碱 | Na2O | 液氯 |
| B | Mn2O7 | HNO3 | NaHCO3 | 硫酸铜溶液 | NH3 |
| C | SO3 | H2CO3 | Na2SiO3 | NaOH | 酒精 |
| D | CO | NaHSO4 | BaCO3 | AgCl | SO2 |
| A.A | B.B | C.C | D.D |
A.无色透明溶液中: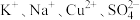 |
B.加入Mg能放出H2的溶液中: |
C.使酚酞变红色的溶液中: |
D.Fe2(SO4)3溶液: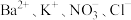 |
【知识点】 限定条件下的离子共存解读 碳酸氢钠与碱反应解读
A. |
B. |
C. |
D. |
【知识点】 单线桥、双线桥分析氧化还原反应解读
| A.反应过程中CCl4是氧化剂 | B.纳米级金刚石粉末属于胶体 |
| C.另一种化合物是NaCl | D.金刚石和石墨互为同素异形体 |
【知识点】 胶体的定义及分类解读 氧化还原反应基本概念 几组常见同素异形体解读
①根据酸分子中H原子个数分为一元酸、二元酸等
②酸性氧化物和水都能反应生成酸,碱性氧化物和水都能反应生成碱
③在电流作用下,盐酸中的
 电离成
电离成 和
和
④熔融态能导电的物质不一定是电解质
⑤食物腐败、植物光合作用都与氧化还原反应有关
⑥金属单质失电子越多,其还原性越强
| A.2个 | B.3个 | C.4个 | D.5个 |
【知识点】 酸、碱、盐、氧化物解读 非电解质、电解质物质类别判断解读
A.用醋酸除去水垢: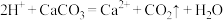 |
B.向硫酸氢钠溶液中滴加氢氧化钡溶液至溶液呈中性: |
C.铜与稀硫酸反应: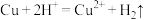 |
D.少量氢氧化钙溶液与过量碳酸氢钠溶液反应: |
【知识点】 离子方程式的正误判断解读
| A.2、2 | B.2、3 | C.3、3 | D.2、4 |
【知识点】 离子方程式的书写解读 氧化还原反应方程式的书写与配平解读
 溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图①所示。下列说法不正确的是
溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图①所示。下列说法不正确的是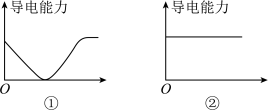
A.图①中导电能力接近0时,溶液中 恰好沉淀完全 恰好沉淀完全 |
| B.图①中导电能力接近0后又增强,主要是由于过量的稀硫酸是电解质溶液 |
| C.向氢氧化钠溶液中逐渐滴加盐酸时,溶液导电能力的变化满足图② |
D.澄清的石灰水中逐渐通入 ,溶液导电能力的变化满足图① ,溶液导电能力的变化满足图① |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
二、多选题 添加题型下试题
| A.HNO3和Na2CO3;HCl和NaHCO3 |
| B.BaCl2和(NH4)2SO4;Ba(OH)2和K2SO4 |
C.HCl和 ;H2S和KOH ;H2S和KOH |
| D.HNO3和NaOH;KHSO4和KOH |
【知识点】 离子方程式的正误判断解读
 。下列对此反应的说法中,不正确的是
。下列对此反应的说法中,不正确的是| A.方框中的物质为Na2SO4 |
| B.Na2O2既是氧化剂,又是还原剂 |
| C.氧化产物只有Na2FeO4 |
| D.2个FeSO4发生反应时,反应中共转移8个电子 |
【知识点】 氧化还原反应的几组概念解读 电子转移计算
三、单选题 添加题型下试题
| A.Na2CO3溶液(NaHCO3): 选用适量NaOH溶液 |
| B.NaHCO3溶液(Na2CO3): 通入过量的CO2气体 |
| C.CO2(HCl): 将混合气体通入 Na2CO3溶液中 |
| D.Na2SO4溶液(Na2CO3): 加入适量的稀硫酸 |
| A.用水来确定某Na2O粉末中是否含有Na2O2 |
| B.用碱石灰除去新制氯气中的水 |
| C.用无色酚酞试液检验某烧碱溶液是否变质 |
| D.用NaOH溶液来鉴别Na2CO3溶液和NaHCO3溶液 |
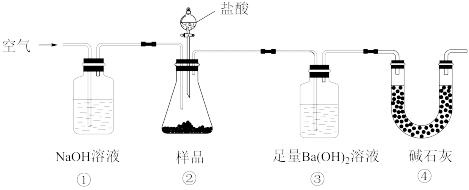
| A.必须在装置②、③间添加盛有饱和 NaHCO3溶液的洗气瓶 |
| B.装置①、④的作用是防止空气中的CO2进入装置③ |
| C.滴入盐酸前,应将装置中含有CO2的空气排尽 |
| D.反应结束时,应再通入空气将装置②中CO2转移到装置③中 |
四、填空题 添加题型下试题
 ;②液氨;③
;②液氨;③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑥铜;⑦
胶体;⑥铜;⑦ ;⑧
;⑧ ;⑨蔗糖;⑩矿泉水。请回答下列问题:
;⑨蔗糖;⑩矿泉水。请回答下列问题:(1)以上物质中属于混合物的是
(2)写出③和⑧反应的离子方程式
(3)写出
 在熔融状态下的电离方程式
在熔融状态下的电离方程式 在物质分类中属于
在物质分类中属于A.钾盐 B.含氧酸 C.酸式盐 D.氧化物
(4)在
 、
、 、
、 、
、 、
、 、S中,既有氧化性又有还原性的是
、S中,既有氧化性又有还原性的是五、解答题 添加题型下试题
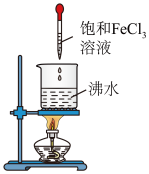
①向沸水中加入几滴饱和
 溶液,继续煮沸至液体呈红褐色停止加热。
溶液,继续煮沸至液体呈红褐色停止加热。②把盛有
 溶液和
溶液和 胶体的烧杯置于暗处,用红色激光笔照射两烧杯中的液体,观察现象。
胶体的烧杯置于暗处,用红色激光笔照射两烧杯中的液体,观察现象。(1)图中盛有饱和
 溶液的仪器名称为
溶液的仪器名称为(2)
 胶体
胶体 胶体的化学方程式:
胶体的化学方程式:(3)步骤②中能观察到的现象为
(4)若将实验改为向饱和
 溶液中加入
溶液中加入 溶液,则观察到的现象为
溶液,则观察到的现象为六、填空题 添加题型下试题
(1)亚氯酸钠
 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为__________(填标号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为__________(填标号)。A. 、 、 | B. 、 、 |
C. 、 、 | D. 、 、 |
 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,
,(3)工业上可利用
 制备亚氯酸钠
制备亚氯酸钠 ,反应体系中涉及下列物质:
,反应体系中涉及下列物质: 、
、 、
、 、
、 、
、 、
、 写出反应的化学方程式:
写出反应的化学方程式:(4)某温度下将
 通入
通入 溶液里,反应后得到
溶液里,反应后得到 、
、 、
、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为
的个数之比为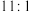 ,则
,则 与
与 反应时,被还原的氯原子和被氧化的氯原子的个数之比为
反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)已知氧化性:
 ,写出少量氯气通入到碘化亚铁溶液中的离子方程式:
,写出少量氯气通入到碘化亚铁溶液中的离子方程式:七、计算题 添加题型下试题
(1)汽车尾气中的
 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式(2)氮氧化物是造成雾霾天气的主要原因之一,利用
 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下: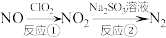
反应①的化学方程式是
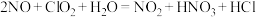 ,反应②的离子方程式是
,反应②的离子方程式是 生成,需消耗
生成,需消耗
亚硝酸钠有咸味,有毒。已知:
 。
。(3)上述反应的还原剂为
 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为(4)在酸性条件下,高锰酸钾可将
 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:试卷分析
试卷题型(共 20题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 物理变化与化学变化 物质的化学变化 | |
| 2 | 0.85 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 | |
| 3 | 0.85 | 酸、碱、盐、氧化物 非电解质、电解质物质类别判断 酸性氧化物通性 二氧化硅的化学性质 | |
| 4 | 0.85 | 限定条件下的离子共存 碳酸氢钠与碱反应 | |
| 5 | 0.85 | 单线桥、双线桥分析氧化还原反应 | |
| 6 | 0.94 | 物质的转化 酸、碱、盐、氧化物 身边的化学物质 | |
| 7 | 0.94 | 胶体的定义及分类 氧化还原反应基本概念 几组常见同素异形体 | |
| 8 | 0.65 | 酸、碱、盐、氧化物 非电解质、电解质物质类别判断 | |
| 9 | 0.85 | 离子方程式的正误判断 | |
| 10 | 0.85 | 离子方程式的书写 氧化还原反应方程式的书写与配平 | |
| 11 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 14 | 0.85 | 碳酸钠与碳酸氢钠的相互转化 物质分离、提纯的常见化学方法 | |
| 15 | 0.85 | 氯气与碱溶液反应 过氧化钠与水的反应 碳酸钠 碳酸钠与碳酸氢钠性质的比较 | |
| 16 | 0.4 | 碳酸钠与盐酸的反应 物质含量的测定 探究物质组成或测量物质的含量 化学实验方案的设计与评价 | |
| 二、多选题 | |||
| 12 | 0.65 | 离子方程式的正误判断 | |
| 13 | 0.65 | 氧化还原反应的几组概念 电子转移计算 | |
| 三、填空题 | |||
| 17 | 0.65 | 非电解质、电解质物质类别判断 电离方程式 离子方程式的书写 氧化还原反应的规律 | |
| 19 | 0.65 | 单线桥、双线桥分析氧化还原反应 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 四、解答题 | |||
| 18 | 0.65 | 胶体的定义及分类 胶体的性质和应用 胶体的制备 | 实验探究题 |
| 五、计算题 | |||
| 20 | 0.65 | 离子方程式的书写 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 | |







