解题方法
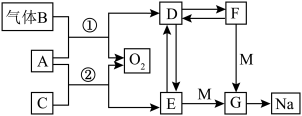
1 . A~G均代表常见化合物,且A、D、E、F、G均含同种金属阳离子,转化关系如图所示,C在常温下为液体,F俗称为小苏打,请回答下列问题:_______ ,F→D:_______ 。
(2)电解熔融G可得到钠和黄绿色气体,该反应的化学方程式为_______ 。
(3)请写出反应②的离子方程式:_____ ,该反应中的氧化剂与还原剂的质量之比为______ 。
(4)检验 溶液中是否存在
溶液中是否存在 的操作及现象为
的操作及现象为_______ 。
(5)取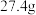 由
由 和
和 组成的某固体粉末充分加热,将产生的全部气体依次通过浓硫酸和碱石灰,碱石灰增重
组成的某固体粉末充分加热,将产生的全部气体依次通过浓硫酸和碱石灰,碱石灰增重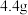 (不考虑气体的逸出),则加热时发生反应的化学方程式为
(不考虑气体的逸出),则加热时发生反应的化学方程式为_______ ,原固体粉末中 的质量分数为
的质量分数为_______ (保留三位有效数字)。
(2)电解熔融G可得到钠和黄绿色气体,该反应的化学方程式为
(3)请写出反应②的离子方程式:
(4)检验
 溶液中是否存在
溶液中是否存在 的操作及现象为
的操作及现象为(5)取
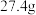 由
由 和
和 组成的某固体粉末充分加热,将产生的全部气体依次通过浓硫酸和碱石灰,碱石灰增重
组成的某固体粉末充分加热,将产生的全部气体依次通过浓硫酸和碱石灰,碱石灰增重 (不考虑气体的逸出),则加热时发生反应的化学方程式为
(不考虑气体的逸出),则加热时发生反应的化学方程式为 的质量分数为
的质量分数为
您最近半年使用:0次
2 . 在化学课上老师向NaOH溶液通入 后无明显现象。
后无明显现象。
(提出问题)如何通过实验证明 与NaOH发生了反应?
与NaOH发生了反应?
[查阅资料]①碳酸钠溶液中滴加少量的稀盐酸,会先反应生成碳酸氢钠(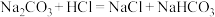 )
)
②碳酸钠在二氧化碳过量的条件继续与水和二氧化碳反应生成碱性较弱的碳酸氢钠。
(设计实验)
(1)反应物之-- 消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满
消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满 的瓶中滴入NaOH溶液,一会儿后观察到的现象是
的瓶中滴入NaOH溶液,一会儿后观察到的现象是________ 。据此现象判断NaOH与 发生了化学反应。
发生了化学反应。________ 。
(2)假设生成物为 ,分别设计了以下两个实验方案:
,分别设计了以下两个实验方案:
(实验拓展)该小组同学将过量的干冰放入氢氧化钠溶液中,利用数字化技术测定溶液pH变化,如图所示。请用化学方程式回答下列问题:________ ;
(4)CD段pH低于7的原因可能是________ 。
 后无明显现象。
后无明显现象。(提出问题)如何通过实验证明
 与NaOH发生了反应?
与NaOH发生了反应?[查阅资料]①碳酸钠溶液中滴加少量的稀盐酸,会先反应生成碳酸氢钠(
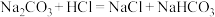 )
)②碳酸钠在二氧化碳过量的条件继续与水和二氧化碳反应生成碱性较弱的碳酸氢钠。
(设计实验)
(1)反应物之--
 消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满
消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满 的瓶中滴入NaOH溶液,一会儿后观察到的现象是
的瓶中滴入NaOH溶液,一会儿后观察到的现象是 发生了化学反应。
发生了化学反应。
(2)假设生成物为
 ,分别设计了以下两个实验方案:
,分别设计了以下两个实验方案:实验操作 | 实验现象 | 结论 |
| 方案一:向实验(1)所得的溶液中加入 | 有白色沉淀产生 | 有新物质 生成,发生反应。 生成,发生反应。 |
| 方案二:向实验(1)所得溶液中滴加过量稀盐酸 |
(实验拓展)该小组同学将过量的干冰放入氢氧化钠溶液中,利用数字化技术测定溶液pH变化,如图所示。请用化学方程式回答下列问题:
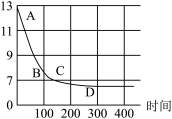
(4)CD段pH低于7的原因可能是
您最近半年使用:0次
名校
解题方法
3 . 科学家设计出烧碱溶液捕捉CO2法,原理如图所示:___________ 。
(2)上述流程中,被循环利用的物质有CaO和NaOH,请说明NaOH循环利用的途径。___________
(3)如下为产生CO2气体的体积与消耗HCl物质的量的关系图。现向流程中 和
和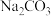 的混合液中逐滴加入稀盐酸,其中可能正确的是
的混合液中逐滴加入稀盐酸,其中可能正确的是___________ 。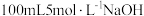 溶液,理论上最多可吸收CO2
溶液,理论上最多可吸收CO2_______ mol;此时溶液中的溶质的电离方程式为:___________ 。若喷洒完上述NaOH溶液后,测得吸收液中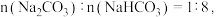 则被吸收的CO2在标准状况下的体积为
则被吸收的CO2在标准状况下的体积为___________ L。
(5)实验室中,有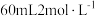 的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的
的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的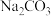 溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)
溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)___________ 。
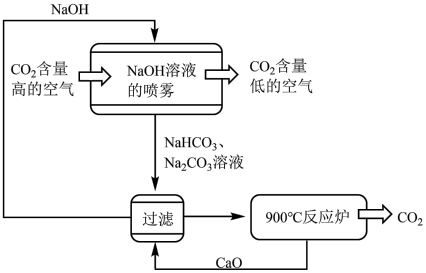
(2)上述流程中,被循环利用的物质有CaO和NaOH,请说明NaOH循环利用的途径。
(3)如下为产生CO2气体的体积与消耗HCl物质的量的关系图。现向流程中
 和
和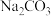 的混合液中逐滴加入稀盐酸,其中可能正确的是
的混合液中逐滴加入稀盐酸,其中可能正确的是
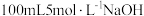 溶液,理论上最多可吸收CO2
溶液,理论上最多可吸收CO2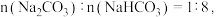 则被吸收的CO2在标准状况下的体积为
则被吸收的CO2在标准状况下的体积为(5)实验室中,有
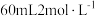 的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的
的NaOH溶液和盛有足量CO2的气体钢瓶,要制备得到纯度最大的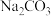 溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)
溶液,具体的实验步骤为:(实验可供选择仪器:烧杯、量筒、试管、胶头滴管、乳胶管、导管)
您最近半年使用:0次
名校
4 . 已知X、Y和Z为中学化学中的常见元素﹐根据如图所示转化关系(反应条件及部分产物已略去)。回答下列问题:

(1)若A、B、C、D均为含X的化合物。A常用作制冷剂,D是一种强酸,则
①反应I的化学方程式为___________ 。
②常温下,C的颜色为___________ 色。
③足量的铜与一定量的D的浓溶液充分反应,向所得溶液中加入100mL 4 NaOH溶液,
NaOH溶液, 恰好沉淀完全。则消耗铜的质量为
恰好沉淀完全。则消耗铜的质量为___________ g。
(2)若A、B、C、D均为含Y的化合物。A是一元强碱且焰色为黄色,E是“碳中和”的主角,则B的化学式为___________ ;C的用途有___________ (任写一种);E的空间结构为___________ 。
(3)若A、B、C、D均为含Z的化合物。A为黄铁矿的主要成分,D为强酸,则
①A在空气中煅烧生成氧化铁的化学方程式为___________ 。
②C→D的过程中选择用98.3%的浓硫酸吸收而不用 吸收的原因是
吸收的原因是___________ 。

(1)若A、B、C、D均为含X的化合物。A常用作制冷剂,D是一种强酸,则
①反应I的化学方程式为
②常温下,C的颜色为
③足量的铜与一定量的D的浓溶液充分反应,向所得溶液中加入100mL 4
 NaOH溶液,
NaOH溶液, 恰好沉淀完全。则消耗铜的质量为
恰好沉淀完全。则消耗铜的质量为(2)若A、B、C、D均为含Y的化合物。A是一元强碱且焰色为黄色,E是“碳中和”的主角,则B的化学式为
(3)若A、B、C、D均为含Z的化合物。A为黄铁矿的主要成分,D为强酸,则
①A在空气中煅烧生成氧化铁的化学方程式为
②C→D的过程中选择用98.3%的浓硫酸吸收而不用
 吸收的原因是
吸收的原因是
您最近半年使用:0次
解题方法
5 . 在给定条件下,下列选项中所示的物质间转化均能实现的是
A.饱和NaCl溶液制备纯碱:饱和NaCl溶液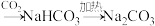 |
B.由S制备 : :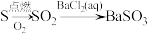 |
C.由 生成 生成 : : |
D. 的生成: 的生成: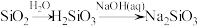 |
您最近半年使用:0次
名校
解题方法
6 . 在给定条件下,下列选项所示的物质间转化不能一步实现的
A. |
B.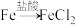 溶液 溶液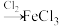 溶液 溶液 |
C.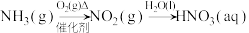 |
D.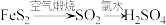 |
您最近半年使用:0次
解题方法
7 . 下列混合物分离(或除杂)的方法正确的是
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加入过量盐酸后,过滤、洗涤 |
| C.除去NaHCO3溶液中的Na2CO3:加入适量稀盐酸 |
| D.除去Al2O3中的少量Fe2O3:加入过量氢氧化钠溶液,过滤、洗涤 |
您最近半年使用:0次
解题方法
8 . 下列除杂方法或对应方程式错误的是
| 选项 | 物质(杂质) | 除杂方法或试剂 | 方程式 |
| A | 溶液 ( ( ) ) | 过量Fe,过滤 |  |
| B | 固体 ( ( ) ) | 水溶后通过量 ,结晶,过滤 ,结晶,过滤 | 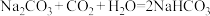 |
| C | 固体 ( ( ) ) | 水溶后加入过量NaOH |  |
| D |  ( ( ) ) | 过量Fe,过滤 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
9 . 侯德榜是我国近代著名的化学家,他提出的联合制碱法得到世界各国的认可,其工艺流程如图所示。下列说法正确的是
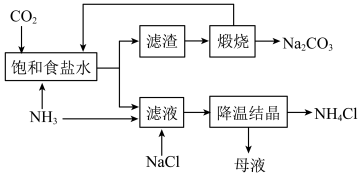
A.向“饱和食盐水”中先通入 ,后通入 ,后通入 |
| B.该工艺流程中涉及了氧化还原反应 |
| C.碳酸氢钠固体中若混有少量碳酸钠,可通过煅烧,除去碳酸钠 |
D.“母液”中溶质的主要成分是 ,可循环利用 ,可循环利用 |
您最近半年使用:0次
解题方法
10 . 焦亚硫酸钠(Na2S2O5)在化学工业中用途广泛。其一种制备流程如下:
(1)SO2分子的VSEPR模型为___________ 。
(2)“NaHCO3制备”所用实验装置(夹持仪器已省略)如下图:___________ 。
②饱和碳酸氢钠溶液的作用是___________ 。
③三颈烧瓶中生成NaHCO3反应的化学方程式为___________ (NaHCO3为沉淀物)。
(3)“Na2S2O5制备”反应过程分四步:
步骤I.在碳酸钠溶液中通入SO2至pH为4.1,生成NaHSO3溶液;
步骤Ⅱ.停止通SO2,向NaHSO3溶液中再加入Na2CO3溶液调至pH为7~8,转化为Na2SO3;
步骤Ⅲ.继续通入SO2至pH达4.1,又生成NaHSO3溶液;
步骤Ⅳ.当溶液中NaHSO3含量达到过饱和浓度时析出Na2S2O5。
①步骤I测量溶液的pH=4.1所用仪器是___________ 。
②写出步骤Ⅱ中反应的离子方程式:___________ 。
③写出I~Ⅳ步骤中总反应的化学方程式:___________ 。
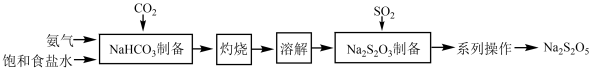
(1)SO2分子的VSEPR模型为
(2)“NaHCO3制备”所用实验装置(夹持仪器已省略)如下图:
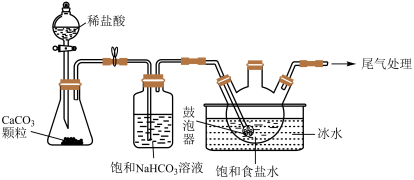
②饱和碳酸氢钠溶液的作用是
③三颈烧瓶中生成NaHCO3反应的化学方程式为
(3)“Na2S2O5制备”反应过程分四步:
步骤I.在碳酸钠溶液中通入SO2至pH为4.1,生成NaHSO3溶液;
步骤Ⅱ.停止通SO2,向NaHSO3溶液中再加入Na2CO3溶液调至pH为7~8,转化为Na2SO3;
步骤Ⅲ.继续通入SO2至pH达4.1,又生成NaHSO3溶液;
步骤Ⅳ.当溶液中NaHSO3含量达到过饱和浓度时析出Na2S2O5。
①步骤I测量溶液的pH=4.1所用仪器是
②写出步骤Ⅱ中反应的离子方程式:
③写出I~Ⅳ步骤中总反应的化学方程式:
您最近半年使用:0次



