名校
解题方法
1 . 回答下列问题。
(1)链状烷烃A在同温同压下蒸气的密度是 的43倍,A的分子式:
的43倍,A的分子式:___________ 。
(2)分子中含有26个电子的链状烷烃 的分子式:
的分子式:___________ 。
(3)一定质量的链状烷烃 完全燃烧后生成
完全燃烧后生成 和
和 ,D的分子式为
,D的分子式为___________ 。
(4)若要使1mol 完全和
完全和 发生取代反应,并生成相同物质的量的四种取代物,则需要
发生取代反应,并生成相同物质的量的四种取代物,则需要 的物质的量为
的物质的量为___________ 。
(1)链状烷烃A在同温同压下蒸气的密度是
 的43倍,A的分子式:
的43倍,A的分子式:(2)分子中含有26个电子的链状烷烃
 的分子式:
的分子式:(3)一定质量的链状烷烃
 完全燃烧后生成
完全燃烧后生成 和
和 ,D的分子式为
,D的分子式为(4)若要使1mol
 完全和
完全和 发生取代反应,并生成相同物质的量的四种取代物,则需要
发生取代反应,并生成相同物质的量的四种取代物,则需要 的物质的量为
的物质的量为
您最近一年使用:0次
解题方法
2 . 研究化学反应中的能量变化具有重要的意义。回答下列问题:
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
①由上述热化学方程式可知甲醇的燃烧热△H=____________ 。
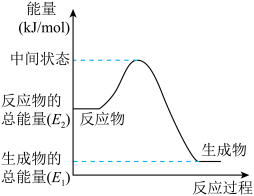
②上述第二个反应的能量变化如图所示,则△H2=___________ k/mol。(用E1、E2的相关式子表示)。.
(2)已知反应N2(g)+3H2(g) 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=________ 。
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是__________ (填化学式)。
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:_____________ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___________ 。
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol①由上述热化学方程式可知甲醇的燃烧热△H=
②上述第二个反应的能量变化如图所示,则△H2=

(2)已知反应N2(g)+3H2(g)
 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
名校
解题方法
3 . 生活无处不化学,运用所学知识,回答下列问题。
(1)节日燃放的五彩缤纷的烟花,就是锂、钠、钾、锶、钡等金属化合物所呈现的各种艳丽色彩。 、
、 在无色火焰上灼烧时,其焰色
在无色火焰上灼烧时,其焰色___________ (填“相同”或“不相同”),该原理是___________ (填“物理”或“化学”)变化。
(2)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:___________ 。
(3)高铁酸钠( )是一种新型的净水剂。其净水过程中发生的化学反应主要为
)是一种新型的净水剂。其净水过程中发生的化学反应主要为 ,证明有
,证明有 胶体生成的方法为:
胶体生成的方法为:___________ 。
(4)工业上常用绿矾( )做处理剂,处理废水中含有的重铬酸根离子(
)做处理剂,处理废水中含有的重铬酸根离子( ),反应的离子方程式如下:
),反应的离子方程式如下: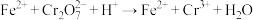 (未配平)。
(未配平)。
①在该反应中,氧化剂是___________ (填离子符号,下同),被氧化的是___________ 。
②该反应每消耗 离子,生成
离子,生成 的物质的量为
的物质的量为___________ mol,转移电子的物质的量为___________ mol。
(1)节日燃放的五彩缤纷的烟花,就是锂、钠、钾、锶、钡等金属化合物所呈现的各种艳丽色彩。
 、
、 在无色火焰上灼烧时,其焰色
在无色火焰上灼烧时,其焰色(2)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(3)高铁酸钠(
 )是一种新型的净水剂。其净水过程中发生的化学反应主要为
)是一种新型的净水剂。其净水过程中发生的化学反应主要为 ,证明有
,证明有 胶体生成的方法为:
胶体生成的方法为:(4)工业上常用绿矾(
 )做处理剂,处理废水中含有的重铬酸根离子(
)做处理剂,处理废水中含有的重铬酸根离子( ),反应的离子方程式如下:
),反应的离子方程式如下: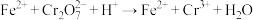 (未配平)。
(未配平)。①在该反应中,氧化剂是
②该反应每消耗
 离子,生成
离子,生成 的物质的量为
的物质的量为
您最近一年使用:0次
名校
4 . Ⅰ.某元素的核素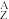 X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
(1)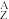 X的质量数A是
X的质量数A是___________ 。
(2)111g XCl2中所含质子数的物质的量为___________ 。
Ⅱ.向VmL 3mol L-1的NaOH溶液中,通入一定量CO2后,然后向该溶液中逐滴入1mol
L-1的NaOH溶液中,通入一定量CO2后,然后向该溶液中逐滴入1mol L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如图所示:
L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如图所示:
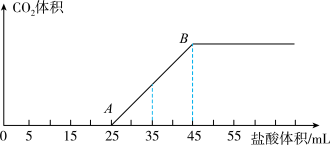
(3)所得溶液中的溶质是___________ ,其物质的量之比为___________ ;
(4)当加入35mL盐酸溶液时,产生二氧化碳的物质的量为___________ mol;
(5)计算所取氢氧化钠溶液的体积V=___________ mL。
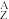 X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
X,1.11 g该核素的氯化物XCl2配成的溶液需用20 mL 1 mol·L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:(1)
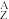 X的质量数A是
X的质量数A是(2)111g XCl2中所含质子数的物质的量为
Ⅱ.向VmL 3mol
 L-1的NaOH溶液中,通入一定量CO2后,然后向该溶液中逐滴入1mol
L-1的NaOH溶液中,通入一定量CO2后,然后向该溶液中逐滴入1mol L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如图所示:
L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如图所示: 
(3)所得溶液中的溶质是
(4)当加入35mL盐酸溶液时,产生二氧化碳的物质的量为
(5)计算所取氢氧化钠溶液的体积V=
您最近一年使用:0次
名校
解题方法
5 . 有关溶液中的计算
(1)某温度下测得0.01mol·L-1的NaOH溶液的pH为11,在该温度下,将pH=12的NaOH溶液VaL与pH=2的硫酸VbL混合。若所得混合液的pH=10,忽略体积变化,则Va∶Vb=___________ 。
(2)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c( )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=___________ 。
(3)常温下二元酸发生如下电离:H2A=H++HA-;HA-⇌H++A2-(Ka=1×10﹣2)。则常温下pH=10的Na2A溶液中c(A2-)是c(HA-)的___________ 倍。
(4)常温下Fe(OH)3的溶度积Ksp=1.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1.0×10-5mol·L-1时就沉淀完全,设溶液中CuSO4的浓度为3.0mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为___________ ,Fe3+完全沉淀时溶液的pH为___________ 。
(1)某温度下测得0.01mol·L-1的NaOH溶液的pH为11,在该温度下,将pH=12的NaOH溶液VaL与pH=2的硫酸VbL混合。若所得混合液的pH=10,忽略体积变化,则Va∶Vb=
(2)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(
 )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=(3)常温下二元酸发生如下电离:H2A=H++HA-;HA-⇌H++A2-(Ka=1×10﹣2)。则常温下pH=10的Na2A溶液中c(A2-)是c(HA-)的
(4)常温下Fe(OH)3的溶度积Ksp=1.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1.0×10-5mol·L-1时就沉淀完全,设溶液中CuSO4的浓度为3.0mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为
您最近一年使用:0次
名校
6 . 填空。
(1)常温常压下,相同体积的NH3和H2S所含N、S质量之比为___________ 。
(2)40.5 g某金属氯化物MCl2中含有0.6 mol C1—,则M的摩尔质量为___________ 。
(3)a mL Al2(SO4)3溶液中含 b g,则溶液中A13+的物质的量浓度为
b g,则溶液中A13+的物质的量浓度为___________ mol/L。
(4)用化学方法测量容器A的体积:把47.5 g MgC12放入500 mL烧杯中,加入150 mL蒸馏水;待MgCl2完全溶解后,将溶液全部转移到容器A中,用蒸馏水稀释至完全充满容器A;从中取出溶液50 mL,该溶液恰好与20 mL 0.20 mol·L-1 AgNO3溶液完全反应,通过计算可知该容器A的体积为___________ L。
(5)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为___________ 。
(1)常温常压下,相同体积的NH3和H2S所含N、S质量之比为
(2)40.5 g某金属氯化物MCl2中含有0.6 mol C1—,则M的摩尔质量为
(3)a mL Al2(SO4)3溶液中含
 b g,则溶液中A13+的物质的量浓度为
b g,则溶液中A13+的物质的量浓度为(4)用化学方法测量容器A的体积:把47.5 g MgC12放入500 mL烧杯中,加入150 mL蒸馏水;待MgCl2完全溶解后,将溶液全部转移到容器A中,用蒸馏水稀释至完全充满容器A;从中取出溶液50 mL,该溶液恰好与20 mL 0.20 mol·L-1 AgNO3溶液完全反应,通过计算可知该容器A的体积为
(5)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使
 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
您最近一年使用:0次
名校
7 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
(2)标准状况下有① ,②
,② 个
个 分子,③
分子,③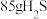 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是___________ (填序号)。
(3)某混合盐溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
___________  。
。
(4)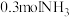 中含有质子数与
中含有质子数与___________ 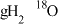 分子中所含质子数相等。
分子中所含质子数相等。
(5) 溶液中
溶液中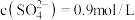 ,则
,则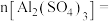
___________ 。
(1)某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(2)标准状况下有①
 ,②
,② 个
个 分子,③
分子,③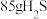 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是(3)某混合盐溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
 。
。(4)
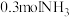 中含有质子数与
中含有质子数与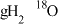 分子中所含质子数相等。
分子中所含质子数相等。(5)
 溶液中
溶液中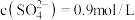 ,则
,则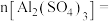
您最近一年使用:0次
名校
8 . 对碳及其氧化物的化学研究有助于人类充分利用化石燃料,消除碳氧化物对环境的负面影响。用 代替
代替 与燃料
与燃料 反应,既可以提高燃烧效率,又能得到高纯
反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①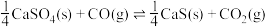
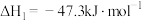
②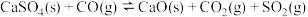
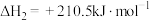
③
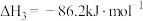
(1)反应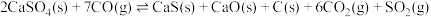 的
的
___________ (用 表示)。
表示)。
(2)向盛有 的真空恒容容器中充入
的真空恒容容器中充入 ,反应①于
,反应①于 达到平衡(
达到平衡( ),平衡时
),平衡时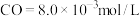 ,
, 的平衡转化率为
的平衡转化率为___________ 。(忽略副反应,结果保留2位有效数字)。
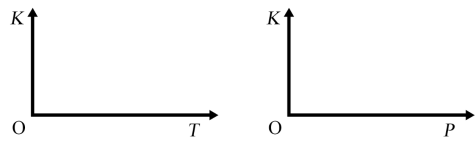
(3)其它条件不变时,升高温度戒缩小容器的体积,均能使反应②的平衡发生移动,请在下列坐标中作出该反应的平衡常数K随温度(T)、压强(P,缩小容器体积)变化而变化的示意图_______ :
(4)某温度下,测得 的
的 溶液的
溶液的 为11,将该温度下
为11,将该温度下 的
的 溶液
溶液 与
与 的
的 溶液,
溶液, 混合,通过计算填写以下不同情况时两溶液的体积比:
混合,通过计算填写以下不同情况时两溶液的体积比:
①若所得混合溶液为中性,且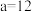 ,
,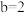 ,则
,则
___________ 。
②若所得混合溶液为中性,且 ,则
,则
___________ 。
③若所得混合溶液的 ,且
,且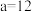 ,
,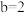 ,则
,则
___________ 。
 代替
代替 与燃料
与燃料 反应,既可以提高燃烧效率,又能得到高纯
反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。①
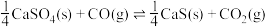
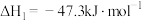
②
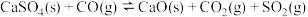
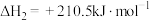
③

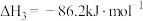
(1)反应
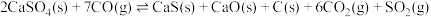 的
的
 表示)。
表示)。(2)向盛有
 的真空恒容容器中充入
的真空恒容容器中充入 ,反应①于
,反应①于 达到平衡(
达到平衡( ),平衡时
),平衡时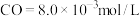 ,
, 的平衡转化率为
的平衡转化率为(3)其它条件不变时,升高温度戒缩小容器的体积,均能使反应②的平衡发生移动,请在下列坐标中作出该反应的平衡常数K随温度(T)、压强(P,缩小容器体积)变化而变化的示意图

(4)某温度下,测得
 的
的 溶液的
溶液的 为11,将该温度下
为11,将该温度下 的
的 溶液
溶液 与
与 的
的 溶液,
溶液, 混合,通过计算填写以下不同情况时两溶液的体积比:
混合,通过计算填写以下不同情况时两溶液的体积比:①若所得混合溶液为中性,且
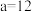 ,
,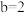 ,则
,则
②若所得混合溶液为中性,且
 ,则
,则
③若所得混合溶液的
 ,且
,且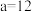 ,
,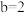 ,则
,则
您最近一年使用:0次
9 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积______ 。
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为______ 。
(3)标准状况下,1.7gNH3与______ LH2S气体含有的氢原子数相同,
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为______ ,该混合气体对氢气的相对密度为______ 。
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为
(3)标准状况下,1.7gNH3与
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为
您最近一年使用:0次
名校
解题方法
10 . 一定在条件下,容积为2L的密闭容器中,将2molL气体和3molM气体混合,发生如下反应: ,10s末平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。计算:
,10s末平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。计算:
(1)平衡时,L和M的转化率比值为___________ 。
(2)前10s内用M表示的化学反应速率为___________ 。
(3)化学方程式中x值为___________ 。
(4)在恒温恒容条件下,往容器中加入1mol氦气,反应速率___________ (填“增大”、“减小”或“不变”)。
(5)平衡时压强与初始压强之比为___________ (整数比)。
 ,10s末平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。计算:
,10s末平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。计算:(1)平衡时,L和M的转化率比值为
(2)前10s内用M表示的化学反应速率为
(3)化学方程式中x值为
(4)在恒温恒容条件下,往容器中加入1mol氦气,反应速率
(5)平衡时压强与初始压强之比为
您最近一年使用:0次
2023-10-26更新
|
103次组卷
|
2卷引用:天津市第四十七中学2023-2024学年高二上学期10月月考化学试题



