名校
1 . 按要求填空;
(1)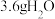 物质的量为
物质的量为_______ mol,约含有_______ 个原子;
(2)已知 个X气体的质量是
个X气体的质量是 ,则X气体的摩尔质量是
,则X气体的摩尔质量是_______ ;
(3)同温同压下,同体积的甲烷 和
和 质量之比为
质量之比为_______ ,质子数之比_______ ;
(4)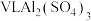 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为_______ ,取出V/2L再加入水稀释到4VL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是_______ 。
(5)某化合物由NaCl、 、
、 三种物质组成,已知钠、镁、铝三元素质量比为
三种物质组成,已知钠、镁、铝三元素质量比为 ,则NaCl、
,则NaCl、 、
、 三种物质的物质的量之比为
三种物质的物质的量之比为_______ ,当 的物质的量为1mol时,混合物的质量是
的物质的量为1mol时,混合物的质量是_______ g。
(6)用质量分数为36.5%的浓盐酸(密度为1.16 )配制成
)配制成 的稀盐酸250ml,浓盐酸的物质的量浓度是:
的稀盐酸250ml,浓盐酸的物质的量浓度是:_______ ;需要浓盐酸体积为:_______ mL(精确到小数点后1位)
(1)
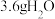 物质的量为
物质的量为(2)已知
 个X气体的质量是
个X气体的质量是 ,则X气体的摩尔质量是
,则X气体的摩尔质量是(3)同温同压下,同体积的甲烷
 和
和 质量之比为
质量之比为(4)
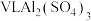 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为 的物质的量浓度是
的物质的量浓度是(5)某化合物由NaCl、
 、
、 三种物质组成,已知钠、镁、铝三元素质量比为
三种物质组成,已知钠、镁、铝三元素质量比为 ,则NaCl、
,则NaCl、 、
、 三种物质的物质的量之比为
三种物质的物质的量之比为 的物质的量为1mol时,混合物的质量是
的物质的量为1mol时,混合物的质量是(6)用质量分数为36.5%的浓盐酸(密度为1.16
 )配制成
)配制成 的稀盐酸250ml,浓盐酸的物质的量浓度是:
的稀盐酸250ml,浓盐酸的物质的量浓度是:
您最近一年使用:0次
名校
2 . (1)在质量分数为28%的 水溶液中,
水溶液中, 与
与 数目之比是
数目之比是_____ 。
(2)在 和
和 所组成的某混合物中,
所组成的某混合物中, 与
与 的物质的量之比为
的物质的量之比为 ,含1molCl-的该混合物的质量是
,含1molCl-的该混合物的质量是____ g。
 水溶液中,
水溶液中, 与
与 数目之比是
数目之比是(2)在
 和
和 所组成的某混合物中,
所组成的某混合物中, 与
与 的物质的量之比为
的物质的量之比为 ,含1molCl-的该混合物的质量是
,含1molCl-的该混合物的质量是
您最近一年使用:0次
名校
3 . 用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O。
(1)用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量)。用NaOH溶液吸收氮氧化物的最条件为:α=___ ,c(NaOH)=___ 。

(2)一定体积的NOx被250mL2mol•L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为___ 。
(1)用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量)。用NaOH溶液吸收氮氧化物的最条件为:α=

(2)一定体积的NOx被250mL2mol•L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为
您最近一年使用:0次
名校
4 . 方法规律提炼题组:物质的量浓度的计算
(1)50mL质量分数为49%、密度为1.24g·cm-3的硫酸中。
①此硫酸的物质的量浓度为___ mol·L-1。
②取此硫酸50mL,用蒸馏水稀释为200mL,稀释后硫酸的物质的量浓度为___ mol·L-1。
(2)在标准状况下,将aLA气体(摩尔质量是Mg/mol)溶于0.1L水中,所得溶液的密度为bg/cm3,则此溶液的物质的量浓度为___ mol·L-1。
(3)取等物质的量浓度的NaOH溶液A和B两份,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸体积之间的关系如图所示,请回答:

①原NaOH溶液的物质的量浓度为___ mol·L-1。
②A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是___ 。
③B曲线中当耗盐酸0<V(盐酸)<25mL时发生的离子反应为___ 。
④B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为___ mL。
(1)50mL质量分数为49%、密度为1.24g·cm-3的硫酸中。
①此硫酸的物质的量浓度为
②取此硫酸50mL,用蒸馏水稀释为200mL,稀释后硫酸的物质的量浓度为
(2)在标准状况下,将aLA气体(摩尔质量是Mg/mol)溶于0.1L水中,所得溶液的密度为bg/cm3,则此溶液的物质的量浓度为
(3)取等物质的量浓度的NaOH溶液A和B两份,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸体积之间的关系如图所示,请回答:

①原NaOH溶液的物质的量浓度为
②A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
③B曲线中当耗盐酸0<V(盐酸)<25mL时发生的离子反应为
④B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为
您最近一年使用:0次
5 . 某化工厂废水(pH=2.0,ρ≈1g•mL-1)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol•L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如表:
(1)你认为往废水中投入___ (填序号),Ag+、Pb2+沉淀效果最好。
a.KI b.NaOH c.Na2S
(2)常温下,如果用NaOH处理上述废水,使溶液的pH=9.0,处理后的废水中c(Pb2+)=___ 。
(3)如果用食盐处理只含Ag+的废水,测得处理后的废水(ρ≈1g•mL-1)中NaCl的质量分数为0.117%.若排放标准要求为c(Ag+)低于1.0×10-8mol•L-1,已知Ksp(AgCl)=1.8×10-10mol•L-2,问该工厂处理后的废水中c(Ag+)=__ ,是否符合排放标准___ (填“是”或“否”)。
| 难溶 电解质 | AgI | PbI2 | AgOH | Pb(OH)2 | Ag2S | PbS |
| Ksp | 8.3×10-17 | 7.1×10-9 | 5.6×10-8 | 1.2×10-15 | 6.3×10-50 | 3.4×10-28 |
a.KI b.NaOH c.Na2S
(2)常温下,如果用NaOH处理上述废水,使溶液的pH=9.0,处理后的废水中c(Pb2+)=
(3)如果用食盐处理只含Ag+的废水,测得处理后的废水(ρ≈1g•mL-1)中NaCl的质量分数为0.117%.若排放标准要求为c(Ag+)低于1.0×10-8mol•L-1,已知Ksp(AgCl)=1.8×10-10mol•L-2,问该工厂处理后的废水中c(Ag+)=
您最近一年使用:0次
2020-02-26更新
|
572次组卷
|
6卷引用:天津市部分区2020届高三上学期期末考试化学试题
天津市部分区2020届高三上学期期末考试化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)作业(二十) 沉淀溶解平衡与溶度积第三章 第四节 沉淀溶解平衡 第1课时 沉淀溶解平衡与溶度积
6 . 规律方法提炼题组:有关物质的量的计算
(1)在标准状况下,67.2LCO2是__________ mol,质量为_______ g,含有__________ 个CO2分子,其中含有__________ mol氧原子。
(2)在标准状况下,1.7g氨气所占的体积约为_________ L,它与同条件下_____ mol H2S含有相同的氢原子数。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为_______ ,R的相对原子质量为__________ 。
(4)实验室常用浓硫酸的质量分数为98%,密度为1.80g·mL-1,其物质的量浓度是_______ 。
(5)标准状况下,将V L A气体(摩尔质量为M g/mol)溶于0.1L水(密度1 g/cm3)中,所得溶液的密度为dg/mL,则此溶液的物质的量浓度为_______ mol/L。
A.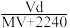 B.
B.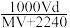 C.
C.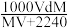 D.
D.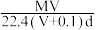
(6)学法题:通过以上训练思考,解决这些问题的关键是将其它量均先转化为____ 再计算。
(1)在标准状况下,67.2LCO2是
(2)在标准状况下,1.7g氨气所占的体积约为
(3)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为
(4)实验室常用浓硫酸的质量分数为98%,密度为1.80g·mL-1,其物质的量浓度是
(5)标准状况下,将V L A气体(摩尔质量为M g/mol)溶于0.1L水(密度1 g/cm3)中,所得溶液的密度为dg/mL,则此溶液的物质的量浓度为
A.
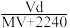 B.
B.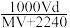 C.
C.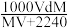 D.
D.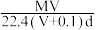
(6)学法题:通过以上训练思考,解决这些问题的关键是将其它量均先转化为
您最近一年使用:0次



