按要求填空;
(1)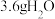 物质的量为
物质的量为_______ mol,约含有_______ 个原子;
(2)已知 个X气体的质量是
个X气体的质量是 ,则X气体的摩尔质量是
,则X气体的摩尔质量是_______ ;
(3)同温同压下,同体积的甲烷 和
和 质量之比为
质量之比为_______ ,质子数之比_______ ;
(4)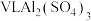 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为_______ ,取出V/2L再加入水稀释到4VL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是_______ 。
(5)某化合物由NaCl、 、
、 三种物质组成,已知钠、镁、铝三元素质量比为
三种物质组成,已知钠、镁、铝三元素质量比为 ,则NaCl、
,则NaCl、 、
、 三种物质的物质的量之比为
三种物质的物质的量之比为_______ ,当 的物质的量为1mol时,混合物的质量是
的物质的量为1mol时,混合物的质量是_______ g。
(6)用质量分数为36.5%的浓盐酸(密度为1.16 )配制成
)配制成 的稀盐酸250ml,浓盐酸的物质的量浓度是:
的稀盐酸250ml,浓盐酸的物质的量浓度是:_______ ;需要浓盐酸体积为:_______ mL(精确到小数点后1位)
(1)
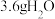 物质的量为
物质的量为(2)已知
 个X气体的质量是
个X气体的质量是 ,则X气体的摩尔质量是
,则X气体的摩尔质量是(3)同温同压下,同体积的甲烷
 和
和 质量之比为
质量之比为(4)
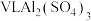 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为 的物质的量浓度是
的物质的量浓度是(5)某化合物由NaCl、
 、
、 三种物质组成,已知钠、镁、铝三元素质量比为
三种物质组成,已知钠、镁、铝三元素质量比为 ,则NaCl、
,则NaCl、 、
、 三种物质的物质的量之比为
三种物质的物质的量之比为 的物质的量为1mol时,混合物的质量是
的物质的量为1mol时,混合物的质量是(6)用质量分数为36.5%的浓盐酸(密度为1.16
 )配制成
)配制成 的稀盐酸250ml,浓盐酸的物质的量浓度是:
的稀盐酸250ml,浓盐酸的物质的量浓度是:
更新时间:2022-04-06 10:56:13
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】NH3和Cl2可快速反应:2NH3+3Cl2→N2+6HCl。有标况下100LNH3和Cl2混合气体,充分反应后的混合气体中N2占混合气体的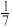 ,则N2的物质的量可能为
,则N2的物质的量可能为
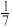 ,则N2的物质的量可能为
,则N2的物质的量可能为| A.0.263mol | B.0.483mol | C.0.526mol | D.0.663mol |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】通过计算,回答下列问题:
(1)标况下6.72 L CH4分子中所含原子数与_______ gH2O分子中所含原子数相等。
(2)一定条件下,l6g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为_____ g/mol。
(3)已知标况下11.2LCO和CO2的混合气体质量为15.6g,则混合气体中CO与CO2的体积之比为_______ 。
(4)在NaCl和AlCl3的混合溶液中,Na+和A13+的物质的量浓度之比为2:1,则2L含1mol Cl-的该溶液中,阳离子的总物质的量浓度为_______ mol/L。
(1)标况下6.72 L CH4分子中所含原子数与
(2)一定条件下,l6g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(3)已知标况下11.2LCO和CO2的混合气体质量为15.6g,则混合气体中CO与CO2的体积之比为
(4)在NaCl和AlCl3的混合溶液中,Na+和A13+的物质的量浓度之比为2:1,则2L含1mol Cl-的该溶液中,阳离子的总物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将Fe2O3、Al2O3两种固体混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:

(1)原混合物中Fe2O3的质量是____________ g。
(2)所用NaOH溶液物质的量浓度为___________ 。
(3)稀硫酸物质的量浓度为______________ 。

(1)原混合物中Fe2O3的质量是
(2)所用NaOH溶液物质的量浓度为
(3)稀硫酸物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】取1.43 g Na2CO3·10H2O溶于水配成100 mL溶液,求:
(1)Na2CO3物质的量浓度____________ Na+物质的量浓度_______________
(2)取出20 mL(1)溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.004 mol/L,求加入蒸馏水的体积_____________ (设稀释时,对溶液体积的影响忽略不计)。
(3)取10 mL(1)溶液,若通入HCl气体以后恰好将CO32-全部转化成CO2气体,则反应后该溶液中Cl-的物质的量浓度__________________ 。
(1)Na2CO3物质的量浓度
(2)取出20 mL(1)溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.004 mol/L,求加入蒸馏水的体积
(3)取10 mL(1)溶液,若通入HCl气体以后恰好将CO32-全部转化成CO2气体,则反应后该溶液中Cl-的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)标准状况下,4.48 L NH3所含分子数为____________ 。___ molCO2 中含有氧原子数与1.806×1024个H2O分子含有的氧原子数相同
(2) 1.7g H2O2中含有氧原子的物质的量为_________ mol,电子数目为 _____ ,已知ag H2O2中含原子数为b,则阿伏加 德罗常数为 _________ (用含a、b的代数式表示)
(3)8.4 g N2与9.6 g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是_______ ,x值为_______ 。并写出R原子的原子结构示意图_________
(4)标况下等质量的O2与O3的体积之比为______ ,氧原子个数之比为 ______ 。
(5)在一密闭容器中充入a molNO和b molO2,可发生如下反应 2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比__________
(2) 1.7g H2O2中含有氧原子的物质的量为
(3)8.4 g N2与9.6 g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是
(4)标况下等质量的O2与O3的体积之比为
(5)在一密闭容器中充入a molNO和b molO2,可发生如下反应 2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】下列物质中,物质的量最大的是________ ,含分子个数最多的是________ ,含原子个数最多的是________ ,质量最大的是________ 。
A.6 g H2;
B.0.5 mol CO2;
C.1.204×1024个HCl分子;
D.标准状况下33.6LCH4;
E.92 g乙醇(C2H5OH);
A.6 g H2;
B.0.5 mol CO2;
C.1.204×1024个HCl分子;
D.标准状况下33.6LCH4;
E.92 g乙醇(C2H5OH);
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)有以下四种物质 ①22g二氧化碳;②5g氢气;③1.204╳1024个氮气分子; ④4℃时18g水,它们所含分子数最多的是_________________ ;质量最大的是____________ ;常温时体积最大的是_______________ (填序号)。
(2)V L Fe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为________ mol·L-1
(3)标况下,mg 气体A和ng气体B具有相等的体积,则同温同压下的密度之比为________ , 同质量的A、B的分子数目之比为________ 。
(4)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为_____________ 、_________________ 。
(2)V L Fe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为
(3)标况下,mg 气体A和ng气体B具有相等的体积,则同温同压下的密度之比为
(4)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)配制500mL 3.6mol/L 的稀H2SO4所需18 mol/L的浓H2SO4的体积为________ mL。
(2)常温下,将0.1 mol/L的NH4Cl溶液与0.1 mol/L的氨水溶液等体积混合,所得混合液的pH=7,则c(NH4+)=________ mol/L,c(Cl-)=________ mol/L。
(2)常温下,将0.1 mol/L的NH4Cl溶液与0.1 mol/L的氨水溶液等体积混合,所得混合液的pH=7,则c(NH4+)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某研究性学习小组利用酸性 溶液测定护校河中溶解的
溶液测定护校河中溶解的 的含量。其测定反应原理:
的含量。其测定反应原理: 。现将
。现将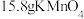 固体溶于水配成
固体溶于水配成 溶液,稀释100倍后,取稀释后的
溶液,稀释100倍后,取稀释后的 溶液
溶液 溶液与
溶液与 河水反应恰好褪色。请计算:
河水反应恰好褪色。请计算:
(1)稀释后的 溶液的物质的量浓度为
溶液的物质的量浓度为___________  。
。
(2)护校河中 的含量为
的含量为___________ 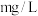 。
。
(3)城乡污水排放一级标准是: 的浓度不超过
的浓度不超过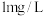 为合格,则该护校河中硫化氢含量
为合格,则该护校河中硫化氢含量___________ (填“合格”或“不合格”)。
 溶液测定护校河中溶解的
溶液测定护校河中溶解的 的含量。其测定反应原理:
的含量。其测定反应原理: 。现将
。现将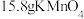 固体溶于水配成
固体溶于水配成 溶液,稀释100倍后,取稀释后的
溶液,稀释100倍后,取稀释后的 溶液
溶液 溶液与
溶液与 河水反应恰好褪色。请计算:
河水反应恰好褪色。请计算:(1)稀释后的
 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(2)护校河中
 的含量为
的含量为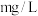 。
。(3)城乡污水排放一级标准是:
 的浓度不超过
的浓度不超过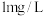 为合格,则该护校河中硫化氢含量
为合格,则该护校河中硫化氢含量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】将3.2gCu与足量的浓硫酸在加热条件下充分反应。
(1)请写出反应的方程式_________________ ;
(2)若把反应后的溶液稀释至500mL,取出50mL,向其中加入足量的BaCl2溶液,得到沉淀2.33g,则稀释后所得溶液中 的物质的量浓度为
的物质的量浓度为_______________ 。
(3)若把反应后的溶液稀释至500mL,加入铁粉。最多能溶解__________ g铁粉
(4)把产生的气体缓缓通入100mLamol/L的NaOH溶液中,若反应物均无剩余,则a的取值范围是___________________ 。
(5)若浓硫酸中含溶质b mol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的n(H2SO4)_______ 0.5b mol(填“>”、“<”或“=”)
(1)请写出反应的方程式
(2)若把反应后的溶液稀释至500mL,取出50mL,向其中加入足量的BaCl2溶液,得到沉淀2.33g,则稀释后所得溶液中
 的物质的量浓度为
的物质的量浓度为(3)若把反应后的溶液稀释至500mL,加入铁粉。最多能溶解
(4)把产生的气体缓缓通入100mLamol/L的NaOH溶液中,若反应物均无剩余,则a的取值范围是
(5)若浓硫酸中含溶质b mol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的n(H2SO4)
您最近一年使用:0次



