(1)标准状况下,4.48 L NH3所含分子数为____________ 。___ molCO2 中含有氧原子数与1.806×1024个H2O分子含有的氧原子数相同
(2) 1.7g H2O2中含有氧原子的物质的量为_________ mol,电子数目为 _____ ,已知ag H2O2中含原子数为b,则阿伏加 德罗常数为 _________ (用含a、b的代数式表示)
(3)8.4 g N2与9.6 g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是_______ ,x值为_______ 。并写出R原子的原子结构示意图_________
(4)标况下等质量的O2与O3的体积之比为______ ,氧原子个数之比为 ______ 。
(5)在一密闭容器中充入a molNO和b molO2,可发生如下反应 2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比__________
(2) 1.7g H2O2中含有氧原子的物质的量为
(3)8.4 g N2与9.6 g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是
(4)标况下等质量的O2与O3的体积之比为
(5)在一密闭容器中充入a molNO和b molO2,可发生如下反应 2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比
更新时间:2020-02-24 15:31:48
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】24.5g硫酸中所含的氧原子数目为________ ,48g的氧气在标准状况下的体积是________ .
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列计算:
(1)若ag CO2含b个原子,则阿伏加德罗常数为___________ mol-1。
(2)含0.6molCl-的氯化镁的质量是___________ g。
(3)已知4.8g CO2和CO混合气体中含分子数为0.15NA,该混合气体的平均摩尔质量为___________ ,CO2和CO的物质的量之比是___________ 。
(1)若ag CO2含b个原子,则阿伏加德罗常数为
(2)含0.6molCl-的氯化镁的质量是
(3)已知4.8g CO2和CO混合气体中含分子数为0.15NA,该混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】物质的量是化学中常用的物理量,请完成以下有关计算:
(1)0.2 g H2含有________ 个H原子。
(2)标准状况下,含有相同氧原子数的CO和CO2的体积之比为________ 。
(3)100 mL硫酸钠溶液中n(Na+)=0.20 mol,则其中c(SO42-)=________ 。
(4)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为________ ,该金属元素的相对原子质量为________ 。
(5)6.72 L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量___ g。
(1)0.2 g H2含有
(2)标准状况下,含有相同氧原子数的CO和CO2的体积之比为
(3)100 mL硫酸钠溶液中n(Na+)=0.20 mol,则其中c(SO42-)=
(4)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为
(5)6.72 L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现有5.1gNH3,则该气体的物质的量为____ mol,该气体所含分子数为____ 个,该气体在标准状况下的体积为____ L,将该气体完全溶于水配成2L溶液,所得溶液的物质的量浓度为_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】把15.6gNa2O2放入100mL水中,充分反应后,计算:(要求写出解题过程,按过程计分)
(1)生成O2在标准状况的体积_______ mL;
(2)反应后所得NaOH的物质的量浓度_______ 。(反应前后溶液体积变化忽略不计)。
(1)生成O2在标准状况的体积
(2)反应后所得NaOH的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】物质的量是高中化学计算的核心:
(1)相同物质的量的NH3和H2S的质量比___ ,分子个数比为____ ,同温同压下的体积比___ ,所含氢原子的个数比为_____ 。
(2)现有mg某气体,它的一个分子由四原子构成,它的摩尔质量为Mg·mol-1。设阿伏伽德罗常数为NA,则:①该气体的物质的量为____ mol。②该气体中所含的原子总数为_____ 个。
(1)相同物质的量的NH3和H2S的质量比
(2)现有mg某气体,它的一个分子由四原子构成,它的摩尔质量为Mg·mol-1。设阿伏伽德罗常数为NA,则:①该气体的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】计算题
(1)3.01×1023个H3O+含有电子的物质的量是_______ 。
(2)200mL2mol/L的Al2(SO4)3溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(3)标准状况下,36gH2和O2组成的混合气体的体积是67.2L,则混合气体中H2和O2的体积比为_______ 。
(4)已知1.505×1023个A气体分子的质量为31g,则62gA气体的摩尔质量是_______ 。
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为NA,则该原子的相对原子质量数值可表示为_______ 或_______ 。
(6)将19.5g锌粒投入250mL2mol·L-1的硫酸溶液中。
①产生的氢气在标准状况下的体积为_______ L。
②忽略溶液体积变化,反应后溶液中氢离子浓度是_______ 。
(1)3.01×1023个H3O+含有电子的物质的量是
(2)200mL2mol/L的Al2(SO4)3溶液中
 的物质的量浓度为
的物质的量浓度为(3)标准状况下,36gH2和O2组成的混合气体的体积是67.2L,则混合气体中H2和O2的体积比为
(4)已知1.505×1023个A气体分子的质量为31g,则62gA气体的摩尔质量是
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为NA,则该原子的相对原子质量数值可表示为
(6)将19.5g锌粒投入250mL2mol·L-1的硫酸溶液中。
①产生的氢气在标准状况下的体积为
②忽略溶液体积变化,反应后溶液中氢离子浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】已知NH3气体34 g,求:(注意书写单位)
(1)NH3的物质的量为__________________ 。
(2)NH3所含原子总数为__________________ 。
(3)这些NH3溶于150 mL水后形成溶液,密度为0.9281g/cm3,则其溶液的物质的量浓度为_______________ 。
(4)与___________ gOH-有相同的电子数。
(1)NH3的物质的量为
(2)NH3所含原子总数为
(3)这些NH3溶于150 mL水后形成溶液,密度为0.9281g/cm3,则其溶液的物质的量浓度为
(4)与
您最近一年使用:0次

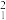 H和
H和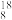 O组成的11克水中,含有中子数的物质的量为多少
O组成的11克水中,含有中子数的物质的量为多少

