24.5g硫酸中所含的氧原子数目为________ ,48g的氧气在标准状况下的体积是________ .
更新时间:2018-08-04 10:10:35
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)质量之比为16∶7∶6的三种气体SO2、CO、NO,分子数之比为________ ;氧原子数之比为________ ;相同条件下的体积之比为________ 。
(2)标准状况下,1.7 g NH3的体积为________ L,它与标准状况下________ L H2S含有相同数目的氢原子。
(3)某气态氧化物的化学式为RO2,标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为__________ ,R的相对原子质量为________ 。
(4)在同温同压下,2 g CO2的体积为120 mL,而2 g A气体的体积为165 mL,则气体A的摩尔质量为________ 。标准状况下,11.2 L CO2和CO的质量是18 g,则其中含CO2的质量为________ g,CO的体积为________ 。
(5)一储气瓶真空时质量为500 g。标准状况下,充满氧气后质量为508 g,装满某气体X后总质量为511 g。则该储气瓶的体积为________ L,X的相对分子质量为________ 。
(2)标准状况下,1.7 g NH3的体积为
(3)某气态氧化物的化学式为RO2,标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为
(4)在同温同压下,2 g CO2的体积为120 mL,而2 g A气体的体积为165 mL,则气体A的摩尔质量为
(5)一储气瓶真空时质量为500 g。标准状况下,充满氧气后质量为508 g,装满某气体X后总质量为511 g。则该储气瓶的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)区别溶液和胶体的一种常用的物理方法是______ 。
(2)分离两种相互溶解但沸点相差较大的液体常用的实验方法是______ 。
(3)0.1 mol/L Al2(SO4)3中Al3+的物质的量浓度是______ ;同温同压下,等体积的CO和CO2所含分子数之比为________ 。
(4)已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中的氧化剂是______ (写化学式),被氧化的元素是____ (写元素符号)。
(5)若该反应中生成标准状况下的Cl2为67.2 L,则转移的电子个数是_________ 。
(2)分离两种相互溶解但沸点相差较大的液体常用的实验方法是
(3)0.1 mol/L Al2(SO4)3中Al3+的物质的量浓度是
(4)已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中的氧化剂是
(5)若该反应中生成标准状况下的Cl2为67.2 L,则转移的电子个数是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】利用太阳能光解水,制备的H2用于还原CO2合成有机物甲醇(CH3OH),可实现资源的再利用。回答下列问题:
(1)CH3OH的摩尔质量是___________ g∙mol-1。
(2)2mol CO2中所含原子的物质的量为___________ mol。
(3)___________ g的氢气中所含H原子的数目与1mol CH3OH相同。
(4)含0.1NA个O的CO2中有___________ 个电子,标准状况下该CO2的体积为___________ L。
(5)在标准状况下,H2和CO2的混合气体共11.2 L,质量为13.6 g,其中H2为___________ mol。
(1)CH3OH的摩尔质量是
(2)2mol CO2中所含原子的物质的量为
(3)
(4)含0.1NA个O的CO2中有
(5)在标准状况下,H2和CO2的混合气体共11.2 L,质量为13.6 g,其中H2为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】利用相关知识填空。
(1)标准状况下11.2LNH3中含_______ 个氨分子,含_______ mol氢原子。
(2)等质量的SO2和SO3物质的量之比是_______ ;所含的氧原子个数之比是_______ 。
(3)4.8gCH4中所含氢原子数与_______ g水所含氢原子数相等。
(4)已知A是一种金属,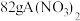 中含有
中含有 个硝酸根离子,则该硝酸盐的摩尔质量为
个硝酸根离子,则该硝酸盐的摩尔质量为_______ 。
(5)标况下,一定量的 与
与 CO所含电子的物质的量相等,
CO所含电子的物质的量相等, 的质量是
的质量是_______ 。
(6)在一定温度和压强下, 某气体的体积为
某气体的体积为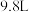 ,则该条件下的气体摩尔体积为
,则该条件下的气体摩尔体积为_______ 。若此时压强为 ,则温度
,则温度_______ 0℃(填>,<,=)。
(1)标准状况下11.2LNH3中含
(2)等质量的SO2和SO3物质的量之比是
(3)4.8gCH4中所含氢原子数与
(4)已知A是一种金属,
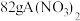 中含有
中含有 个硝酸根离子,则该硝酸盐的摩尔质量为
个硝酸根离子,则该硝酸盐的摩尔质量为(5)标况下,一定量的
 与
与 CO所含电子的物质的量相等,
CO所含电子的物质的量相等, 的质量是
的质量是(6)在一定温度和压强下,
 某气体的体积为
某气体的体积为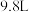 ,则该条件下的气体摩尔体积为
,则该条件下的气体摩尔体积为 ,则温度
,则温度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(MoleDay),这个时间的美式写法为6:0210/23,外观与阿伏加 德罗常数相似。
(1)amol H2SO4中含有b个氧原子,则阿伏加 德罗常数可以表示为________ mol-1
(2)4.5g水与__________ g硫酸所含的分子数相等。
(3)相同质量的SO2和SO3所含硫原子的个数之比为________
(4)已知agA和bgB恰好完全反应生成0.2 molC和dgD,则C的摩尔质量为____________
(5)含Na2SO4、MgSO4和NaNO3的1L混合溶液,已知其中c(Mg2+)=0.4 mol·L-1,c( )=0.7 mol·L-1,c(
)=0.7 mol·L-1,c( )=0.2 mol·L-1,则此溶液中c(Na+)为
)=0.2 mol·L-1,则此溶液中c(Na+)为________ mol·L-1。
(6)若mg密度为ρg·cm-3的Al2(SO4)3溶液中含 ng,则该Al2(SO4)3溶液的物质的量浓度是
ng,则该Al2(SO4)3溶液的物质的量浓度是____ mol·L-1
(1)amol H2SO4中含有b个氧原子,则阿伏加 德罗常数可以表示为
(2)4.5g水与
(3)相同质量的SO2和SO3所含硫原子的个数之比为
(4)已知agA和bgB恰好完全反应生成0.2 molC和dgD,则C的摩尔质量为
(5)含Na2SO4、MgSO4和NaNO3的1L混合溶液,已知其中c(Mg2+)=0.4 mol·L-1,c(
 )=0.7 mol·L-1,c(
)=0.7 mol·L-1,c( )=0.2 mol·L-1,则此溶液中c(Na+)为
)=0.2 mol·L-1,则此溶液中c(Na+)为(6)若mg密度为ρg·cm-3的Al2(SO4)3溶液中含
 ng,则该Al2(SO4)3溶液的物质的量浓度是
ng,则该Al2(SO4)3溶液的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】NA为阿伏加德罗常数的值,请完成以下有关计算。
(1)0.05 mol的硫酸钠中含有_______ 个氧原子;其所含Na+与_______ g NaCl中所含有的Na+数目相同。
(2)溶质质量分数为98%、密度为1.84 g·cm-3的某浓硫酸,溶质的物质的量浓度为_______ 。
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为_______ 。
(1)0.05 mol的硫酸钠中含有
(2)溶质质量分数为98%、密度为1.84 g·cm-3的某浓硫酸,溶质的物质的量浓度为
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某元素的一种核素X的质量数为A,含有N个中子,则a g 1HmX分子中所含质子数是________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)在标准状况下,CO 和 CO2 的混合气体共 39.2 L,质量为 61 g。则两种气体的物质的量之和为_________ mol,其中 CO2 _________ mol,CO 占总体积的_________ %。
(2)0.5 mol H2SO4的质量是_________ g,含_________ 个H2SO4分子,含_________ 个氧原子,能与_________ mol NaOH 完全反应,该硫酸所含氢元素的质量与_________ g H3PO4 或_________ mol HCl 中所含氢元素的质量相同。
(3)12.8g氧气与_________ L(标准状况)的CO气体所含氧原子数相同,与_________ mol SO2所含的分子数相同。
(4)2 mol SO3和3 mol SO2其原子数之比为_________ ;相同状况下(均为气体)体积之比为_________ ;氧原子数之比为_________ 。
(1)在标准状况下,CO 和 CO2 的混合气体共 39.2 L,质量为 61 g。则两种气体的物质的量之和为
(2)0.5 mol H2SO4的质量是
(3)12.8g氧气与
(4)2 mol SO3和3 mol SO2其原子数之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】状准状况下,22.4LHCl气体溶于250mL水中,配成密度为1.146g·cm-3的溶液,
(1)求所得盐酸中溶质的物质的量浓度?____________
(2)若将此溶液再稀释成1L溶液,求稀释后盐酸中溶质的物质的量浓度?_________
(1)求所得盐酸中溶质的物质的量浓度?
(2)若将此溶液再稀释成1L溶液,求稀释后盐酸中溶质的物质的量浓度?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】2.3g钠跟水反应后,得到100mL溶液,2Na+2H2O=2NaOH+H2↑
试计算:(1)生成的气体在标况下的体积是多少?___
(2)反应后所得溶液的物质的量浓度是多少?___
(3)在完全反应后转移的电子个数为多少?(用单线桥方法标出)___
试计算:(1)生成的气体在标况下的体积是多少?
(2)反应后所得溶液的物质的量浓度是多少?
(3)在完全反应后转移的电子个数为多少?(用单线桥方法标出)
您最近一年使用:0次

 )、H2和O2的混合气体,在标准状态下,若将H2、O2的混合气体点燃引爆.活塞先左弹,恢复原温度后,空气体积占整个容器的
)、H2和O2的混合气体,在标准状态下,若将H2、O2的混合气体点燃引爆.活塞先左弹,恢复原温度后,空气体积占整个容器的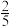 。则原来H2、O2的体积之比可能为
。则原来H2、O2的体积之比可能为


