每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(MoleDay),这个时间的美式写法为6:0210/23,外观与阿伏加 德罗常数相似。
(1)amol H2SO4中含有b个氧原子,则阿伏加 德罗常数可以表示为________ mol-1
(2)4.5g水与__________ g硫酸所含的分子数相等。
(3)相同质量的SO2和SO3所含硫原子的个数之比为________
(4)已知agA和bgB恰好完全反应生成0.2 molC和dgD,则C的摩尔质量为____________
(5)含Na2SO4、MgSO4和NaNO3的1L混合溶液,已知其中c(Mg2+)=0.4 mol·L-1,c( )=0.7 mol·L-1,c(
)=0.7 mol·L-1,c( )=0.2 mol·L-1,则此溶液中c(Na+)为
)=0.2 mol·L-1,则此溶液中c(Na+)为________ mol·L-1。
(6)若mg密度为ρg·cm-3的Al2(SO4)3溶液中含 ng,则该Al2(SO4)3溶液的物质的量浓度是
ng,则该Al2(SO4)3溶液的物质的量浓度是____ mol·L-1
(1)amol H2SO4中含有b个氧原子,则阿伏加 德罗常数可以表示为
(2)4.5g水与
(3)相同质量的SO2和SO3所含硫原子的个数之比为
(4)已知agA和bgB恰好完全反应生成0.2 molC和dgD,则C的摩尔质量为
(5)含Na2SO4、MgSO4和NaNO3的1L混合溶液,已知其中c(Mg2+)=0.4 mol·L-1,c(
 )=0.7 mol·L-1,c(
)=0.7 mol·L-1,c( )=0.2 mol·L-1,则此溶液中c(Na+)为
)=0.2 mol·L-1,则此溶液中c(Na+)为(6)若mg密度为ρg·cm-3的Al2(SO4)3溶液中含
 ng,则该Al2(SO4)3溶液的物质的量浓度是
ng,则该Al2(SO4)3溶液的物质的量浓度是
更新时间:2020-10-17 08:59:53
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)标准状况下,4.48 L NH3所含分子数为____________ 。___ molCO2 中含有氧原子数与1.806×1024个H2O分子含有的氧原子数相同
(2) 1.7g H2O2中含有氧原子的物质的量为_________ mol,电子数目为 _____ ,已知ag H2O2中含原子数为b,则阿伏加 德罗常数为 _________ (用含a、b的代数式表示)
(3)8.4 g N2与9.6 g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是_______ ,x值为_______ 。并写出R原子的原子结构示意图_________
(4)标况下等质量的O2与O3的体积之比为______ ,氧原子个数之比为 ______ 。
(5)在一密闭容器中充入a molNO和b molO2,可发生如下反应 2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比__________
(2) 1.7g H2O2中含有氧原子的物质的量为
(3)8.4 g N2与9.6 g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是
(4)标况下等质量的O2与O3的体积之比为
(5)在一密闭容器中充入a molNO和b molO2,可发生如下反应 2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】完成下列填空
(1)8gCH4中含有的质子总数为___________
(2)0.25molCH4中所含原子数为a,则阿伏加德罗常数可表示为NA=___________
(3)相同质量的CO和CO2所含氧元素的质量之比为___________
(4)已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是___________
(5)把1000mL含有BaCl2、KCl的混合溶液分成10等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完沉淀。则该混合溶液中钾离子浓度为___________
(1)8gCH4中含有的质子总数为
(2)0.25molCH4中所含原子数为a,则阿伏加德罗常数可表示为NA=
(3)相同质量的CO和CO2所含氧元素的质量之比为
(4)已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
(5)把1000mL含有BaCl2、KCl的混合溶液分成10等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完沉淀。则该混合溶液中钾离子浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)在臭氧发生器中装入100mLO2,经反应3O2=2 O3,最后气体体积变为95mL(体积均为标准状况下测定),则反应后混合气体的密度为____________ 。
(2)将溶质质量分数为a%NaOH溶液蒸发掉m g水后,变成VmL 2a%的NaOH不饱和溶液,则蒸发后的溶液的物质的量浓度是__________ 。
(3)amolH2SO4中含有b个氧原子,则阿伏伽德罗常数可以表示为_______ 。
(4)现有CO、CO2、O3(臭氧)三种气体,它们分别都含有1mol氧原子,则三种气体的质量之比为________ (最简整数比)。
(5)标准状况下,密度为0.75g/L 的NH3与CH4组成的混合气体中,NH3的体积分数为__________ ,该混合气体对氢气的相对密度为_____________ 。
(2)将溶质质量分数为a%NaOH溶液蒸发掉m g水后,变成VmL 2a%的NaOH不饱和溶液,则蒸发后的溶液的物质的量浓度是
(3)amolH2SO4中含有b个氧原子,则阿伏伽德罗常数可以表示为
(4)现有CO、CO2、O3(臭氧)三种气体,它们分别都含有1mol氧原子,则三种气体的质量之比为
(5)标准状况下,密度为0.75g/L 的NH3与CH4组成的混合气体中,NH3的体积分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)相同质量的O2和O3的物质的量比为_________ ;所含氧原子的个数比为_________ 。
(2)在标准状况下,1.7 NH3所占的体积约为_________ L,含有的N原子数目为___________ ,它与标准状况________ L H2S含有相同数目的氢原子。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________________ 。
(4)同温同压下,SO2与氦气的密度之比为________ ,若质量相同,两种气体的体积比为_____ 。
(2)在标准状况下,1.7 NH3所占的体积约为
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为
(4)同温同压下,SO2与氦气的密度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】按照要求填空:
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是___________ ,属于强电解质的是___________ ,属于非电解质的是___________ ,能导电的是___________ 。
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为___________ ;它与盐酸反应的化学方程式为___________ 。
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是___________ 。
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目___________ 。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为___________ 。
(5)19.6克硫酸中含有___________ 个原子,将其溶于水配成500mL溶液则溶液的物质的量浓度为___________ ,从中取出100mL可以消耗1mol/L的NaOH溶液___________ mL。
(6)物质的量相等的SO2和SO3,其质量之比为________ ,所含原子数之比为________ ,所含质子数之比为________ ,质量相等的SO2和SO3,所含氧原子数之比为___________ 。
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为___________ 。36g 中质子数为
中质子数为___________ ,电子数为___________ (用NA表示)。
(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是___________ ,混合气体的平均摩尔质量为___________ ,混合气体中CO2在标准状况下的体积是___________ ,混合气体在标准状况下的密度是___________ ,该混合气体对氢气的相对密度为___________ 。
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(5)19.6克硫酸中含有
(6)物质的量相等的SO2和SO3,其质量之比为
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为
 中质子数为
中质子数为(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】把铝、铁混合物1.1g溶于200mL5mol/L盐酸中,反应后盐酸的浓度变为4.6mol/L(溶液体积变化忽略不计)。
求:该混合物中铝的物质的量为___ mol,铁的物质的量为___ mol。
求:该混合物中铝的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某溶液含 Mg2+、Al3+,向其中滴加a mLC1mol·L—1NaOH之后,改成滴加C2mol·L—1H2SO4溶液,所得沉淀Y(mol)与所加试剂总体积V(mL)间的关系如下图所示。据此,回答下列问题:
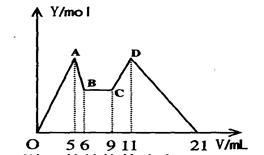
(1)C-D过程中的离子方程式________________________ ;
(2)n(Mg2+)/ n(Al3+) =______________ ;
(3)C1/C2=______________ ;
(4)所加入NaOH溶液的体积a=______________ mL。

(1)C-D过程中的离子方程式
(2)n(Mg2+)/ n(Al3+) =
(3)C1/C2=
(4)所加入NaOH溶液的体积a=
您最近一年使用:0次



