按照要求填空:
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是___________ ,属于强电解质的是___________ ,属于非电解质的是___________ ,能导电的是___________ 。
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为___________ ;它与盐酸反应的化学方程式为___________ 。
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是___________ 。
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目___________ 。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为___________ 。
(5)19.6克硫酸中含有___________ 个原子,将其溶于水配成500mL溶液则溶液的物质的量浓度为___________ ,从中取出100mL可以消耗1mol/L的NaOH溶液___________ mL。
(6)物质的量相等的SO2和SO3,其质量之比为________ ,所含原子数之比为________ ,所含质子数之比为________ ,质量相等的SO2和SO3,所含氧原子数之比为___________ 。
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为___________ 。36g 中质子数为
中质子数为___________ ,电子数为___________ (用NA表示)。
(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是___________ ,混合气体的平均摩尔质量为___________ ,混合气体中CO2在标准状况下的体积是___________ ,混合气体在标准状况下的密度是___________ ,该混合气体对氢气的相对密度为___________ 。
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(5)19.6克硫酸中含有
(6)物质的量相等的SO2和SO3,其质量之比为
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为
 中质子数为
中质子数为(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是
更新时间:2023-09-16 21:00:42
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】臭氧层是地球生命的保护神,其中的臭氧(O3)和氧气(O2)是氧元素的两种单质。
(1)含有相同氧原子数的臭氧和氧气的物质的量之比为__________ 。
(2)同温同压时,相等质量的臭氧和氧气的密度之比为________ ,所占有的体积之比为__________ ,所含有的原子个数之比为_________ 。
(3)已知反应:O3 + 2KI + H2O = 2KOH + I2 + O2 。标准状况下的2.24L臭氧完全反应,生成的KOH的质量为_____ 克。
(1)含有相同氧原子数的臭氧和氧气的物质的量之比为
(2)同温同压时,相等质量的臭氧和氧气的密度之比为
(3)已知反应:O3 + 2KI + H2O = 2KOH + I2 + O2 。标准状况下的2.24L臭氧完全反应,生成的KOH的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在标准状况下,25gH2和CO2的混合气体含有1.204×1024个分子。
求(1)该混合物中CO2的物质的量_____ ;
(2)混合物中H2的体积_____ 。
求(1)该混合物中CO2的物质的量
(2)混合物中H2的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】以物质的量为中心的相关计算,已知阿状伽德罗常数为NA.
(1)相同物质的量的CO2和O2其分子数之比为_______________ ,原子数之比为_____________ 氧原子数之比为____________________ 。
(2)73.0g HCl气体中含有_______________ 个原子,标况下体积约为___________ L。
(3)23.75g某+2价金属的氯化物(MCl2)中含有3.01 ×1023个Cl-,则M的摩尔质量为______________ 。
(1)相同物质的量的CO2和O2其分子数之比为
(2)73.0g HCl气体中含有
(3)23.75g某+2价金属的氯化物(MCl2)中含有3.01 ×1023个Cl-,则M的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)同温同压下的两个相同容器中分别装有N0和NO2气体,则两瓶气体中,原子数之比是______ ,质量之比是______ ,密度之比是______ ,分子数之比是________ 。
(2)下列所给出的几组物质中:含有分子数最少的是_______ ;含有原子数最多的是________ ;标准状况下体积最小的是________ 。
① 1gH2; ② 2.408×1023个CH4;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)设NA表示阿伏伽德罗常数,如果X g某气体含有的分子数是Y,则Z g该气体在标准状况下的体积是_______ (用含NA的式子表示)。
(4)配制500 mL 0.1mol/L的的稀H2SO4溶液,需要用量筒量取质量分数为98%的浓H2SO4(密度为1.84g/cm3)的体积为_______ 。
(2)下列所给出的几组物质中:含有分子数最少的是
① 1gH2; ② 2.408×1023个CH4;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)设NA表示阿伏伽德罗常数,如果X g某气体含有的分子数是Y,则Z g该气体在标准状况下的体积是
(4)配制500 mL 0.1mol/L的的稀H2SO4溶液,需要用量筒量取质量分数为98%的浓H2SO4(密度为1.84g/cm3)的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)填写关于物质的量计算的四个恒等式:n=___________ =___________ =___________ =___________ 。
(2)0.5molO3(臭氧)中含有的分子数是___________ 个、原子数是___________ 个。
(3)0.5mol的Fe含___________ 个铁原子,质量是___________ g;2.107×1024个铁原子是___________ molFe,质量为___________ g。
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。
(1)填写关于物质的量计算的四个恒等式:n=
(2)0.5molO3(臭氧)中含有的分子数是
(3)0.5mol的Fe含
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】某元素的一种核素X的质量数为A,含有N个中子,则a g 1HmX分子中所含质子数是________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15 g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80 g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半。试计算(计算结果精确到0.1%):
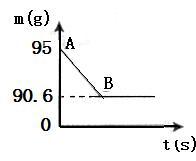
(1)产生CO2的质量为__________ g;
(2)该鸡蛋壳中CaCO3的质量分数__________ 。
(3)所用稀盐酸中溶质的质量分数__________ 。

(1)产生CO2的质量为
(2)该鸡蛋壳中CaCO3的质量分数
(3)所用稀盐酸中溶质的质量分数
您最近一年使用:0次
【推荐2】为测定某石灰石中CaCO3的质量分数,称取W g石灰石样品,加入过量的浓度为6 mol/L的盐酸,使它完全溶解,加热煮沸,除去溶解的CO2,再加入足量的草酸铵[(NH4)2C2O4]溶液后,慢慢加入氨水降低溶液的酸度,则析出草酸钙沉淀,离子方程式为:C2O42-+Ca2+=CaC2O4↓,过滤出CaC2O4后,用稀硫酸溶解:CaC2O4+H2SO4=H2C2O4 +CaSO4,再用蒸馏水稀释溶液至V0 mL。取出V1 mL用a mol/L的KMnO4酸性溶液滴定,此时发生反应:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,若滴定终点时消耗a mol/L的KMnO4 V2 mL,样品中CaCO3的质量分数为_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】同温同压同体积的O3和O2的分子数之比为_______ ,质量之比为_______ ,密度之比_______ ,含原子数之比为_______ ,所含电子数之比为_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是_____________ ;R的相对原子质量约是______________ 。
您最近一年使用:0次



