解题方法
1 . 我国科学家首次在实验室实现 到淀粉的合成,其路线如下,设
到淀粉的合成,其路线如下,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 到淀粉的合成,其路线如下,设
到淀粉的合成,其路线如下,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是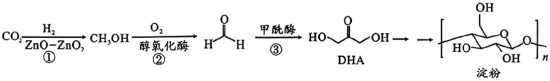
A.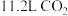 含有的 含有的 键数目为 键数目为 |
B.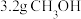 经醇氧化酶氧化为 经醇氧化酶氧化为 ,转移电子数目为 ,转移电子数目为 |
C.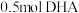 含有的羧基数目为 含有的羧基数目为 |
D. 淀粉与乙酸酯化,最多可消耗的乙酸分子数目为 淀粉与乙酸酯化,最多可消耗的乙酸分子数目为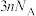 |
您最近半年使用:0次
2 . 设 为阿伏加德罗常数的值。制备莫尔盐[
为阿伏加德罗常数的值。制备莫尔盐[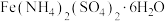 ]用到Fe、
]用到Fe、 、
、 、
、 等物质,下列说法正确的是
等物质,下列说法正确的是
 为阿伏加德罗常数的值。制备莫尔盐[
为阿伏加德罗常数的值。制备莫尔盐[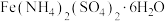 ]用到Fe、
]用到Fe、 、
、 、
、 等物质,下列说法正确的是
等物质,下列说法正确的是A.1L pH=1的 溶液中阳离子总数为0.1 溶液中阳离子总数为0.1 |
B.标准状况下,2.24L  所含共价键数为0.2 所含共价键数为0.2 |
C.0.1  溶液中, 溶液中, 的数目为0.2 的数目为0.2 |
D.5.6g Fe与足量的浓硫酸反应制备 ,转移的电子数为0.2 ,转移的电子数为0.2 |
您最近半年使用:0次
名校
3 . 溴蒸气与氨气相遇产生“白烟”,化学方程式为 。用
。用 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是
 。用
。用 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是A.生成14gN2时,反应中还原剂的分子数目为 |
B.标准状况下,11.2LBr2参与反应时转移的电子数为 |
C.1L 的NH4Br溶液中含有 的NH4Br溶液中含有 的数目小于 的数目小于 |
D.当生成29.4gNH4Br时,消耗NH3分子的数目为 |
您最近半年使用:0次
昨日更新
|
215次组卷
|
3卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
2024高三·全国·专题练习
4 . 工业合成氨常选择反应:N2+3H2 2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
 2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是| A.28 g N2完全反应,转移的电子数为3NA |
| B.混合气中物质的沸点:NH3>N2>H2 |
| C.在一定温度的固定容器中进行反应,通入氦气,能提高氢气的转化率 |
| D.反应物断裂NA个σ键的同时生成物断裂NA个σ键,反应达到平衡状态 |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
5 . 氨基钠(NaNH2)是重要的化学试剂,其与氧气反应的方程式为:4NaNH2+3O2=2NaOH+2NaNO2+2NH3。下列说法正确的是
A.NH3的电子式为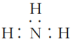 |
| B.n(氧化剂)∶n(还原剂)=3∶2 |
| C.NH3是氧化产物 |
| D.每消耗0.3 mol O2,转移电子数约为2.4×6.02×1023 |
您最近半年使用:0次
6 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.2.4 g Mg与足量稀硫酸反应,转移的电子数为0.1NA |
| B.3.2 g O2和O3混合气体中的氧原子数为0.3NA |
| C.1.6 g CH4含有的共价键数为0.4NA |
| D.5.6 L CO中含有的分子数为0.25NA |
您最近半年使用:0次
7 . 设NA表示阿伏加德罗常数,下列说法中不正确的是
| A.一定量的Fe与含1mol HNO3的稀硝酸恰好反应,如还原产物为NO,则被还原的氮原子数小于NA |
| B.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 |
| C.常温常压下,NA个臭氧分子的体积大于22.4L |
| D.1.8g水中含有的电子总数为NA |
您最近半年使用:0次
8 . 设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是
 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A.标准状况下,22.4L正丙醇( )分子中含有 )分子中含有 的数目为8 的数目为8 |
B.24g质量分数为25%的甲醛水溶液中含有氢原子数目为2.4 |
C.pH=1的 溶液与足量的Zn反应产生的氢气分子数目为0.05 溶液与足量的Zn反应产生的氢气分子数目为0.05 |
D.0.1mol  与0.1mol 与0.1mol  反应时,转移电子的数目为0.3 反应时,转移电子的数目为0.3 |
您最近半年使用:0次
9 . 每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(MoleDay),这个时间的美式写法为6:0210/23,外观与阿伏加德罗常数近似值 相似。设NA代表阿伏加德罗常数的值。下列说法正确的是
相似。设NA代表阿伏加德罗常数的值。下列说法正确的是
 相似。设NA代表阿伏加德罗常数的值。下列说法正确的是
相似。设NA代表阿伏加德罗常数的值。下列说法正确的是A.常温常压下,2.24L  含有的分子数目为0.1NA 含有的分子数目为0.1NA |
B.标准状况下,3.2g由 和 和 组成的混合气体所含原子数目为0.2NA 组成的混合气体所含原子数目为0.2NA |
C.5.6g铁在足量的 中燃烧,转移的电子数为0.2NA 中燃烧,转移的电子数为0.2NA |
D.0.1 的 的 溶液中, 溶液中, 的数目为0.2NA 的数目为0.2NA |
您最近半年使用:0次
名校
10 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1mol铁单质与足量的硫单质充分反应,转移电子的数目为 |
B.常温下,22.4L 与足量的 与足量的 反应,生成的 反应,生成的 分子数为 分子数为 |
C.常温下,将5.6g铁片投入足量的浓硫酸中,铁失去的电子数为 |
D.1mol 与足量 与足量 反应,转移的电子数为 反应,转移的电子数为 |
您最近半年使用:0次



