1 . 已知:K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,按要求完成下列空格。
(1)用单线桥标明电子转移方向和数目______ 。
(2)该反应中氧化剂是______ 。
(3)该反应在标况下生成2.24L氯气时,转移电子______ 个。
(1)用单线桥标明电子转移方向和数目
(2)该反应中氧化剂是
(3)该反应在标况下生成2.24L氯气时,转移电子
您最近一年使用:0次
名校
解题方法
2 . 有个成语叫“物以类聚”,本意就是物质的分类。对物质进行分类,我们不仅能够根据类别通性预测物质的性质,还能探索各类物质的共性和特性。化学家根据需要将众多物质进行分类,现有下列几种物质:①冰水混合物 ②N2 ③CO ④Fe(OH)3胶体 ⑤Mg ⑥熔融Ca(OH)2 ⑦漂白粉 ⑧乙醇 ⑨盐酸。
(1)属于非电解质的是_______ (填序号,下同);属于强电解质的是_______ ;上述物质中弱电解质的电离方程式:_______ 。
(2)写出实验室制取④的化学方程式:_______ 。
(3)生活中“84”消毒液(有效成分为NaClO)和洁厕灵(主要成分是⑨ )不能混合使用,原因是_______ (用离子方程式表示)。
(4)新型陶瓷氮化铝可用氧化铝高温还原法制备: (未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
(未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为_______ mol。
(1)属于非电解质的是
(2)写出实验室制取④的化学方程式:
(3)生活中“84”消毒液(有效成分为NaClO)和洁厕灵(主要成分是⑨ )不能混合使用,原因是
(4)新型陶瓷氮化铝可用氧化铝高温还原法制备:
 (未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
(未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
您最近一年使用:0次
名校
解题方法
3 . 现有下列物质:
①熔融NaCl;② 溶液;③氯气;④
溶液;③氯气;④ ;⑤NaOH溶液;⑥氢氧化铁胶体;⑦
;⑤NaOH溶液;⑥氢氧化铁胶体;⑦ ;⑧铜; ⑨ 过氧化钠; ⑩
;⑧铜; ⑨ 过氧化钠; ⑩
(1)上述物质中属于电解质的是___________ (填标号)。
(2)将②逐滴加入⑥中的现象是___________ 。
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为___________ 。
(4)③通入石灰乳中,发生反应的化学方程式为___________ 。
(5)⑦与⑨反应的化学方程式为:___________ ,该反应生成标准状况下22.4L氧气,转移的电子数目为___________ 。
①熔融NaCl;②
 溶液;③氯气;④
溶液;③氯气;④ ;⑤NaOH溶液;⑥氢氧化铁胶体;⑦
;⑤NaOH溶液;⑥氢氧化铁胶体;⑦ ;⑧铜; ⑨ 过氧化钠; ⑩
;⑧铜; ⑨ 过氧化钠; ⑩
(1)上述物质中属于电解质的是
(2)将②逐滴加入⑥中的现象是
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为
(4)③通入石灰乳中,发生反应的化学方程式为
(5)⑦与⑨反应的化学方程式为:
您最近一年使用:0次
2024高三·全国·专题练习
4 . 设NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2022·全国卷) 溶液中,
溶液中, 的数目为
的数目为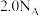
B.(2022·全国卷)电解熔融 ,阴极增重
,阴极增重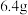 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
C.(2022·浙江卷) 和
和 于密闭容器中充分反应后,
于密闭容器中充分反应后, 分子总数为
分子总数为
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
E.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
F.(2021·广东卷)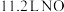 与
与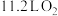 混合后的分子数目为
混合后的分子数目为
G.(2021·浙江卷)0.1 mol CH3COOH与足量CH3CH2OH充分反应生成的CH3COOCH2CH3分子数目为0.1NA
A.(2022·全国卷)
 溶液中,
溶液中, 的数目为
的数目为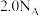
B.(2022·全国卷)电解熔融
 ,阴极增重
,阴极增重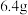 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
C.(2022·浙江卷)
 和
和 于密闭容器中充分反应后,
于密闭容器中充分反应后, 分子总数为
分子总数为
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
E.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
F.(2021·广东卷)
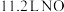 与
与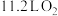 混合后的分子数目为
混合后的分子数目为
G.(2021·浙江卷)0.1 mol CH3COOH与足量CH3CH2OH充分反应生成的CH3COOCH2CH3分子数目为0.1NA
您最近一年使用:0次
名校
5 . 二氧化氯在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯化物。制备ClO2的方法是:
_____NaClO3+_______HCl=______ClO2↑+______Cl2↑+______NaCl+_______H2O
(1)试配平上述化学方程式,并用标出电子转移的方向和数目___________ 。
(2)该反应中HCl体现的性质是___________。
(3)在标准状况下,每生成10.08L气体,转移的电子数为___________ 。
(4)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒无害的两种气体,自身被还原为Cl-。处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的___________ 倍。
_____NaClO3+_______HCl=______ClO2↑+______Cl2↑+______NaCl+_______H2O
(1)试配平上述化学方程式,并用标出电子转移的方向和数目
(2)该反应中HCl体现的性质是___________。
| A.氧化性 | B.还原性 | C.酸性 | D.挥发性 |
(4)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒无害的两种气体,自身被还原为Cl-。处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的
您最近一年使用:0次
名校
解题方法
6 . 北京时间2022年12月4日20时09分,神舟十四号载人飞船返回舱在东风着陆场成功着陆。搭载神舟十四号载人飞船的是长征二号F遥十四运载火箭。
燃料主要有:①煤油 ②液氢 ③肼( ) ④固态铝粉
) ④固态铝粉
氧化剂主要有:⑤液氧 ⑥ ⑦高氯酸铵(
⑦高氯酸铵( )
)
(1)16g肼中含有H原子数目约为___________ 个。
(2)同温同压下,氧气与氢气的密度之比为___________ 。
(3)飞船以铝粉与高氨酸铵的混合物为固体燃料,其中高氯酸铵发生分解反应生成: 、
、 、
、 、和
、和 。请写出该反应的化学方程式:
。请写出该反应的化学方程式:___________ ,其中被氧化的元素是______ ,还原产物是______ 。
(4)空间站中可利用过氧化钠与人体代谢的 、
、 反应制备呼吸必需的
反应制备呼吸必需的 。过氧化钠的颜色为
。过氧化钠的颜色为_______ ,其中阴离子与阳离子的个数比为______ 。写出 与
与 反应的化学方程式
反应的化学方程式_______ 。在25℃和101 的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为_______ L,转移电子数目为_______ 个。
燃料主要有:①煤油 ②液氢 ③肼(
 ) ④固态铝粉
) ④固态铝粉氧化剂主要有:⑤液氧 ⑥
 ⑦高氯酸铵(
⑦高氯酸铵( )
)(1)16g肼中含有H原子数目约为
(2)同温同压下,氧气与氢气的密度之比为
(3)飞船以铝粉与高氨酸铵的混合物为固体燃料,其中高氯酸铵发生分解反应生成:
 、
、 、
、 、和
、和 。请写出该反应的化学方程式:
。请写出该反应的化学方程式:(4)空间站中可利用过氧化钠与人体代谢的
 、
、 反应制备呼吸必需的
反应制备呼吸必需的 。过氧化钠的颜色为
。过氧化钠的颜色为 与
与 反应的化学方程式
反应的化学方程式 的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
您最近一年使用:0次
7 . 请按要求回答下列问题:
(1)氯气和水反应的化学方程式:___________ 。
(2)长期置于空气中的钠,最后形成的物质与氢氧化钡溶液混合后,发生反应的离子方程式为:___________ 。
(3)现有8种物质:①熔融 ②氯气③
②氯气③ ④葡萄糖⑤
④葡萄糖⑤ ⑥稀硫酸⑦
⑥稀硫酸⑦ ⑧
⑧ 。属于电解质的是
。属于电解质的是___________ ,能导电是___________ 。
(4)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
①该反应的还原剂是___________ ;
②若生成1
 ,则反应转移的电子数为
,则反应转移的电子数为___________  。
。
(1)氯气和水反应的化学方程式:
(2)长期置于空气中的钠,最后形成的物质与氢氧化钡溶液混合后,发生反应的离子方程式为:
(3)现有8种物质:①熔融
 ②氯气③
②氯气③ ④葡萄糖⑤
④葡萄糖⑤ ⑥稀硫酸⑦
⑥稀硫酸⑦ ⑧
⑧ 。属于电解质的是
。属于电解质的是(4)高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
①该反应的还原剂是
②若生成1

 ,则反应转移的电子数为
,则反应转移的电子数为 。
。
您最近一年使用:0次
解题方法
8 . 请同学们仔细思考并回答下列问题:
(1)过氧化钠与二氧化碳反应的化学方程式为___________ ;39g过氧化钠完全反应,转移的电子数为___________ ,生成___________ L(换算成标准状况下)氧气。
(2) 与
与___________  所含的原子数目相等。
所含的原子数目相等。
(3)如图所示,将等质量的气体m和气体n充入带有活塞(可自由移动且厚度不计)的密闭容器中,最终活塞停留在图示位置,则m与n的摩尔质量之比为___________ 。

(4)实验室可用 固体与浓盐酸常温下反应制备氯气。
固体与浓盐酸常温下反应制备氯气。

该反应的氧化剂为___________ ,写出配平后的上述反应的化学方程式:___________ 。
(1)过氧化钠与二氧化碳反应的化学方程式为
(2)
 与
与 所含的原子数目相等。
所含的原子数目相等。(3)如图所示,将等质量的气体m和气体n充入带有活塞(可自由移动且厚度不计)的密闭容器中,最终活塞停留在图示位置,则m与n的摩尔质量之比为

(4)实验室可用
 固体与浓盐酸常温下反应制备氯气。
固体与浓盐酸常温下反应制备氯气。
该反应的氧化剂为
您最近一年使用:0次
23-24高三上·上海浦东新·阶段练习
名校
解题方法
9 . 业内人士预测,2023年对中国汽车的出口量将历史性的超过日本,成为世界第一、中国电动汽车技术处于世界领先地位。比亚迪公司充电电池全线搭载了刀片电池,刀片电池具有续航里程高,安全性好的优点。刀片电池的正极材料使用了磷酸铁锂(LiFePO4)。磷酸铁锂(LiFePO4)由Li2CO3、C6H12O6和FePO4在高温条件下制备。
(1)LiFePO4中的化合物态的铁价电子排布式为___________ ,铁元素在元素周期表中的位置为___________ 。
(2)C6H12O6在反应中表现出___________ (填氧化性、还原性),每生成27 g C6H12O6参与反应,转移电子数目为___________ 。
(3)CO2的电子式为___________ ,Li2CO3中负离子的立体结构为___________ 。
(4)电动汽车相对于燃油动力汽车更加环保,原因是___________ 。

(1)LiFePO4中的化合物态的铁价电子排布式为
(2)C6H12O6在反应中表现出
(3)CO2的电子式为
(4)电动汽车相对于燃油动力汽车更加环保,原因是
您最近一年使用:0次
2023高三上·全国·专题练习
解题方法
10 . 请完成下列填空:
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量_______ mol。
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作_______ (填“氧化”“还原”)剂,每有1 mol H2O2参加反应,转移电子的物质的量为_______ 。
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为_______ mol。
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为_______ g。
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_______ mol。
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1 mol K2FeO4转移的电子的物质的量
(2)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作
(3)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L的H2(标准状况)时,转移电子的物质的量为
(4)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50 mol/L的高锰酸钾溶液40.00 mL,则此双氧水溶液中溶质的质量为
(5)取300 mL0.2 mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是
您最近一年使用:0次



