业内人士预测,2023年对中国汽车的出口量将历史性的超过日本,成为世界第一、中国电动汽车技术处于世界领先地位。比亚迪公司充电电池全线搭载了刀片电池,刀片电池具有续航里程高,安全性好的优点。刀片电池的正极材料使用了磷酸铁锂(LiFePO4)。磷酸铁锂(LiFePO4)由Li2CO3、C6H12O6和FePO4在高温条件下制备。
(1)LiFePO4中的化合物态的铁价电子排布式为___________ ,铁元素在元素周期表中的位置为___________ 。
(2)C6H12O6在反应中表现出___________ (填氧化性、还原性),每生成27 g C6H12O6参与反应,转移电子数目为___________ 。
(3)CO2的电子式为___________ ,Li2CO3中负离子的立体结构为___________ 。
(4)电动汽车相对于燃油动力汽车更加环保,原因是___________ 。

(1)LiFePO4中的化合物态的铁价电子排布式为
(2)C6H12O6在反应中表现出
(3)CO2的电子式为
(4)电动汽车相对于燃油动力汽车更加环保,原因是
23-24高三上·上海浦东新·阶段练习 查看更多[1]
(已下线)上海市华东师范大学第二附属中学2023-2024学年高三上学期10月月考化学试题
更新时间:2023-11-06 20:16:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】实验室里用软锰矿(含MnO2质量分数为60%)与浓盐酸反应来制取适量的氯气,反应方程式如下: (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。
(1)用双线桥标出该反应中电子转移的方向和数目_______ 。
(2)若生成5个Cl2分子,计算转移电子总数_______ 。
(3)产生7.1g氯气时,计算所需软锰矿的质量_______ ,被氧化的HCl的质量_______ 。
 (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。(1)用双线桥标出该反应中电子转移的方向和数目
(2)若生成5个Cl2分子,计算转移电子总数
(3)产生7.1g氯气时,计算所需软锰矿的质量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________ ;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________ ;
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:
(2)该反应中氧化剂和还原剂的物质的量之比为
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】第四周期过渡元素单质及其化合物在生活、生产中有广泛应用。回答下列问题:
(1)基态Cr原子的价层电子排布式为___________ 。
(2)过渡金属单质及其化合物是有机合成反应的重要催化剂。
例如,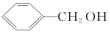 (苯甲醇)
(苯甲醇)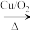
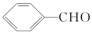 (苯甲醛)
(苯甲醛)
①苯甲醇分子中C原子的杂化类型是___________ 。
②苯甲醇、苯甲醛的沸点依次为205.7 ℃、179 ℃,造成二者沸点差异的主要原因是___________ 。
(3)多数过渡金属的配离子在水溶液中有颜色,其显色与配合物分裂能有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,用Δ表示,中心离子电荷数越大,中心与配体距离越近,则作用越强,Δ越大。分裂能(Δ):[Co(H2O)6]2+___________ (填“>”“<”或“=”)[Co(H2O)6]2+,理由是___________ 。
(1)基态Cr原子的价层电子排布式为
(2)过渡金属单质及其化合物是有机合成反应的重要催化剂。
例如,
 (苯甲醇)
(苯甲醇)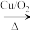
 (苯甲醛)
(苯甲醛)①苯甲醇分子中C原子的杂化类型是
②苯甲醇、苯甲醛的沸点依次为205.7 ℃、179 ℃,造成二者沸点差异的主要原因是
(3)多数过渡金属的配离子在水溶液中有颜色,其显色与配合物分裂能有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,用Δ表示,中心离子电荷数越大,中心与配体距离越近,则作用越强,Δ越大。分裂能(Δ):[Co(H2O)6]2+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、C、D、E都是元素周期表中前36号的元素,它们的原子序数依次增大。A原子基态时未成对电子数是第二周期元素中最多的,C的单质是一种黄色晶体,易研成粉末,D的基态原子核外有6个能级且全部充满电子,E的基态原子内层均排满电子,最外层有1个电子。
(1)基态A原子外围电子的轨道表示式为_______ 。
(2)C的原子结构示意图为_______ 。
(3)基态D原子的电子排布式为_______ 。
(4)基态E2+离子的价电子排布式为_______ 。
(1)基态A原子外围电子的轨道表示式为
(2)C的原子结构示意图为
(3)基态D原子的电子排布式为
(4)基态E2+离子的价电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)X元素是非金属元素,其原子中有3个未成对电子,轨道的最高能级是3p,则该原子的核外电子排布式是________________________ 。
(2)某元素的原子基态时有6个电子处于3d轨道上,则该元素的原子序数为________ ,该元素原子的d轨道上的未成对电子有________ 个。
(3)某元素的基态原子失去3个电子后,它的3d轨道上的电子恰好半满,则该元素的原子序数为________ ,其离子的电子排布式为______________________________________ 。
(2)某元素的原子基态时有6个电子处于3d轨道上,则该元素的原子序数为
(3)某元素的基态原子失去3个电子后,它的3d轨道上的电子恰好半满,则该元素的原子序数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题。
(1)现有下列各组物质: 和
和
⑦ 和
和
互为同分异构体的是_______ ,属于同一种物质的是______ ,互为同系物的是_______ 。 (填序号)
(2)请按照官能团的种类不同将下列有机化合物进行分类:_____ ,属于醛的是_____ ,属于酯的是_____ 。
(3)有机物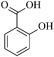 中官能团的名称为
中官能团的名称为_____ 、_____ 。
(4)某新型有机物M的结构如图所示。有关M的说法错误的是______。
(1)现有下列各组物质:
① 和
和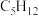 ②
② 和
和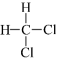 ③
③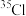 和
和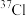 ④石墨和金刚石
④石墨和金刚石
⑤ 和
和
 和
和
⑦
 和
和
互为同分异构体的是
(2)请按照官能团的种类不同将下列有机化合物进行分类:
A.HC≡C—CH2CH3 B.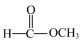 C.
C.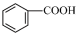 D.
D. E.
E. F.
F.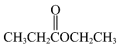 G.
G. H.
H.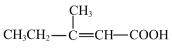
(3)有机物
 中官能团的名称为
中官能团的名称为(4)某新型有机物M的结构如图所示。有关M的说法错误的是______。
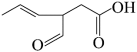
A.M的分子式为 C7H12O3 C7H12O3 | B.M中含有三种官能团 |
| C.M分子中含有手性碳原子 | D.M中碳原子杂化方式有两种 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】H2SeO3的中心原子杂化类型是___________ ;SeO 的立体构型是
的立体构型是___________
 的立体构型是
的立体构型是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:___________ 。
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为___________ 。
(3)O和S处于同一主族,第一电离能较大的是___________ 。 和
和 分子中的键角较大的是
分子中的键角较大的是___________ ,键长较短的是___________ 。单质硫与热的 浓溶液反应的产物之一为
浓溶液反应的产物之一为 ,
,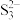 的空间构型为
的空间构型为___________ 。
(4)已知多个相邻且平行的p轨道重叠则形成大 键,分子中的大
键,分子中的大 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子的大
键的电子数(如苯分子的大 键可表示为
键可表示为 )。吡咯(
)。吡咯(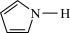 )中所有原子共平面。则吡咯分子中的大
)中所有原子共平面。则吡咯分子中的大 键应表示为
键应表示为___________ 。吡咯分子中N原子的杂化类型为___________ ,1mol吡咯分子中含有___________  键,
键,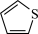 噻吩的沸点为84℃,吡咯(
噻吩的沸点为84℃,吡咯(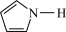 )的沸点在129-131℃之间,吡洛沸点较高,其原因是
)的沸点在129-131℃之间,吡洛沸点较高,其原因是___________ 。
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度: ,则下列物质酸性由强到弱的顺序是___________(填序号)。
,则下列物质酸性由强到弱的顺序是___________(填序号)。
(6) 是离子晶体,其形成过程中的能量变化如图(a)所示。
是离子晶体,其形成过程中的能量变化如图(a)所示。
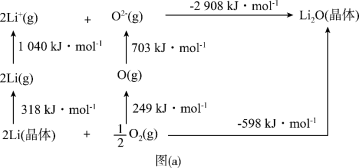
可知,Li原子的第一电离能为_______  ,
, 键键能为
键键能为_______  。
。
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为(3)O和S处于同一主族,第一电离能较大的是
 和
和 分子中的键角较大的是
分子中的键角较大的是 浓溶液反应的产物之一为
浓溶液反应的产物之一为 ,
,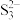 的空间构型为
的空间构型为(4)已知多个相邻且平行的p轨道重叠则形成大
 键,分子中的大
键,分子中的大 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子的大
键的电子数(如苯分子的大 键可表示为
键可表示为 )。吡咯(
)。吡咯(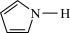 )中所有原子共平面。则吡咯分子中的大
)中所有原子共平面。则吡咯分子中的大 键应表示为
键应表示为 键,
键, 噻吩的沸点为84℃,吡咯(
噻吩的沸点为84℃,吡咯(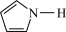 )的沸点在129-131℃之间,吡洛沸点较高,其原因是
)的沸点在129-131℃之间,吡洛沸点较高,其原因是(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:
 ,则下列物质酸性由强到弱的顺序是___________(填序号)。
,则下列物质酸性由强到弱的顺序是___________(填序号)。A. | B. |
C. | D.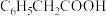 |
 是离子晶体,其形成过程中的能量变化如图(a)所示。
是离子晶体,其形成过程中的能量变化如图(a)所示。
可知,Li原子的第一电离能为
 ,
, 键键能为
键键能为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】 “碳捕捉技术”是指通过一定的方法将工业生产中产生的 分离出来并利用。某兴趣小组对于现有碳捕捉技术进行了研究学习。
分离出来并利用。某兴趣小组对于现有碳捕捉技术进行了研究学习。
(1)利用NaOH溶液来“捕捉” 的基本过程如图所示(部分条件及物质未标出)。在流程中可以循环利用的物质有
的基本过程如图所示(部分条件及物质未标出)。在流程中可以循环利用的物质有______ 、______ (均填化学式)。

(2)地球上最高效的碳捕捉过程就是叶绿素催化的光合作用,请写出光合作用合成葡萄糖( )的化学方程式
)的化学方程式______ 。葡萄糖是生物体内的主要供能物质,具有良好的水溶性。20℃时,甲、乙两份葡萄糖饱和溶液的质量分别为200 g和300 g,在下列条件中,析出晶体质量相同的为______ (填选项)。
A.两份溶液都降温至10℃ B.甲溶液降温至10℃,乙液降温至0℃
C.两份溶液都蒸发掉20 g水 D.甲溶液蒸发掉30 g水,乙液蒸发掉20 g
 分离出来并利用。某兴趣小组对于现有碳捕捉技术进行了研究学习。
分离出来并利用。某兴趣小组对于现有碳捕捉技术进行了研究学习。(1)利用NaOH溶液来“捕捉”
 的基本过程如图所示(部分条件及物质未标出)。在流程中可以循环利用的物质有
的基本过程如图所示(部分条件及物质未标出)。在流程中可以循环利用的物质有
(2)地球上最高效的碳捕捉过程就是叶绿素催化的光合作用,请写出光合作用合成葡萄糖(
 )的化学方程式
)的化学方程式A.两份溶液都降温至10℃ B.甲溶液降温至10℃,乙液降温至0℃
C.两份溶液都蒸发掉20 g水 D.甲溶液蒸发掉30 g水,乙液蒸发掉20 g
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)化学用语是学习化学的重要工具。请按要求用化学用语填空:
①2个铜原子___________ 。
②5个氢氧根离子______________ 。
③最理想能源的气体单质_________________ 。
④氧化铝中铝元素的化合价为+3价________ 。
⑤可用于人工降雨的干冰______________ 。
(2)生活处处有化学,请联系学过的化学知识。回答下列问题:
①包饺子的食材有面粉、韭草、瘦肉、植物油、食盐等。其中富含糖类的是_________ 。
②人体缺____ 元素能导致儿童发育不良或佝偻病,老年人会导致骨质疏松。
③加了洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的__________ 作用。
④铁锅容易生锈的主要原因是铁与空气中的________ 、水蒸气发生了化学反应。
⑤玻璃杯、塑料盆、不锈钢餐具等是生活中常见的日用品,其中属于有机合成材料制成的是____________ .
①2个铜原子
②5个氢氧根离子
③最理想能源的气体单质
④氧化铝中铝元素的化合价为+3价
⑤可用于人工降雨的干冰
(2)生活处处有化学,请联系学过的化学知识。回答下列问题:
①包饺子的食材有面粉、韭草、瘦肉、植物油、食盐等。其中富含糖类的是
②人体缺
③加了洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的
④铁锅容易生锈的主要原因是铁与空气中的
⑤玻璃杯、塑料盆、不锈钢餐具等是生活中常见的日用品,其中属于有机合成材料制成的是
您最近一年使用:0次



