我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________ ;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________ ;
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:
(2)该反应中氧化剂和还原剂的物质的量之比为
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为
更新时间:2017-11-19 14:42:42
|
相似题推荐
【推荐1】航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
I.“天宫”中水和氧气最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。
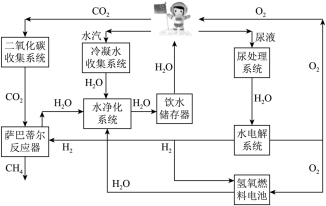
(1)“水电解系统”中产生氧气发生反应的化学方程式为_______ ,每转移8mol电子,生成_______ g的 O2。
(2)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为_______ ,该反应_______ (填“是”或“否”)氧化还原反应。
(3)一定条件 “萨巴蒂尔反应器”可除去CO2,该反应化学方程式为_______ 。
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不逸出,使水球越来越大。
(4)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3_______ (补全化学方程式)。
(5)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的_______ (填序号)。
A. B.
B. C.
C.
I.“天宫”中水和氧气最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“水电解系统”中产生氧气发生反应的化学方程式为
(2)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为
(3)一定条件 “萨巴蒂尔反应器”可除去CO2,该反应化学方程式为
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不逸出,使水球越来越大。
(4)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3
(5)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的
A.
 B.
B. C.
C.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一定质量的Na2O2投入到足量的水中,得到1L的溶液,同时生成的气体在标准状况时体积为2.24L。求:
(1)该反应转移的电子数目为_______ 。
(2)生成的NaOH物质的量浓度_______ 。
(3)参与该反应的物质Na2O2的质量_______ 。
(1)该反应转移的电子数目为
(2)生成的NaOH物质的量浓度
(3)参与该反应的物质Na2O2的质量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:将SO2通入FeCl3溶液中,溶液颜色会变为浅绿色,其原理可表示为:
□Fe3++ □SO2+ □H2O —— □Fe2++ □SO42-+ □H+
(1)在上述方框内填上配平后的系数,并用单线桥法标出电子转移的方向和数目_____ 。
(2)若参加反应的SO2体积为1.12 L(标准状况下),则反应中转移电子的物质的量为______ mol;
(3)已知向Fe2+溶液中滴加少量硝酸时,溶液由浅绿色变为黄色。则Fe3+、SO42-、HNO3的氧化性由强到弱的顺序为________________________ 。
□Fe3++ □SO2+ □H2O —— □Fe2++ □SO42-+ □H+
(1)在上述方框内填上配平后的系数,并用单线桥法标出电子转移的方向和数目
(2)若参加反应的SO2体积为1.12 L(标准状况下),则反应中转移电子的物质的量为
(3)已知向Fe2+溶液中滴加少量硝酸时,溶液由浅绿色变为黄色。则Fe3+、SO42-、HNO3的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据反应8NH3+3Cl2==6NH4Cl+N2,回答下列问题:
(1)用单线桥表示出该反应电子转移的数目和方向_____________ 。
(2)氧化剂是_______ 。
(3)当有34gNH3参加反应时,被氧化的物质的质量为_____ g,生成的还原产物的质量为_______ g。
(1)用单线桥表示出该反应电子转移的数目和方向
(2)氧化剂是
(3)当有34gNH3参加反应时,被氧化的物质的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平离子方程式(将化学计量数填于空白处)____ I-+____ IO3—+____ H+ =____ I2+____ H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的化学方程式是:____________________________ 。
②某学生设计回收四氯化碳的操作为:a.加入适量Na2SO3稀溶液; b.分离出下层液体;c.将碘的四氯化碳溶液置于分液漏斗中; d.将分液漏斗充分振荡后静置。其中分液漏斗使用前须进行的操作是_______ ,上述操作正确的顺序是:_______ (填序号)
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:a.准确称取ag食盐,加适量蒸馏水使其完全溶解;b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;c.以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是_______________________ 。
②b中反应所消耗的KI的物质的量是____________ mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含a的代数式表示)_____ mg/kg。
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
| 分装时期 | |
| 分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平离子方程式(将化学计量数填于空白处)
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的化学方程式是:
②某学生设计回收四氯化碳的操作为:a.加入适量Na2SO3稀溶液; b.分离出下层液体;c.将碘的四氯化碳溶液置于分液漏斗中; d.将分液漏斗充分振荡后静置。其中分液漏斗使用前须进行的操作是
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:a.准确称取ag食盐,加适量蒸馏水使其完全溶解;b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;c.以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是
②b中反应所消耗的KI的物质的量是
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含a的代数式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.人们对酸碱的认识,已有几百年的历史。1923年丹麦化学家布朗斯特和英国化学家劳莱提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论,下列水溶液既可看作酸又可看作碱的是__________ (填字母序号)。
A.H2O B. NH4+ C. OH- D. HCO3- E. CH3COOO- F. Cl-
Ⅱ.建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
□NaNO2+□HI→□NO↑+□I2+□NaI+□H2O
(1)配平上面方程式______________ 。
(2)上述反应的氧化剂是__________ ;若有1mol的还原剂被氧化,则反应中转移电子的数目是_______________ 。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为_________________ 。
A.H2O B. NH4+ C. OH- D. HCO3- E. CH3COOO- F. Cl-
Ⅱ.建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
□NaNO2+□HI→□NO↑+□I2+□NaI+□H2O
(1)配平上面方程式
(2)上述反应的氧化剂是
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)在S2﹣、Fe2+、Fe3+、Mg2+、S、I﹣、H+中,只有氧化性的是_____________ ,只有还原性的是_____ ,既有氧化性又有还原性的是__________ .
(2)火药是中国古代“四大发明”之一.黑火药爆炸时发生如下反应:2KNO3+C+S═K2S+2NO2↑+CO2↑.其中被还原的元素是____ ,被氧化的元素是____ ,氧化剂是_______ ,还原剂是________ .
(3)配平氧化还原反应方程式:_____________

(2)火药是中国古代“四大发明”之一.黑火药爆炸时发生如下反应:2KNO3+C+S═K2S+2NO2↑+CO2↑.其中被还原的元素是
(3)配平氧化还原反应方程式:

您最近一年使用:0次

 ,其中
,其中 的物质的量分数为b,将其全部投入
的物质的量分数为b,将其全部投入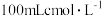 的稀硝酸中,加热使其充分反应(假设
的稀硝酸中,加热使其充分反应(假设 是唯一的还原产物)。
是唯一的还原产物)。 。
。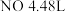 ,则反应转移的电子总数为
,则反应转移的电子总数为 。
。 时,则c≥
时,则c≥

