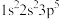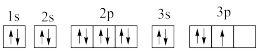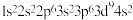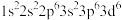(1)X元素是非金属元素,其原子中有3个未成对电子,轨道的最高能级是3p,则该原子的核外电子排布式是________________________ 。
(2)某元素的原子基态时有6个电子处于3d轨道上,则该元素的原子序数为________ ,该元素原子的d轨道上的未成对电子有________ 个。
(3)某元素的基态原子失去3个电子后,它的3d轨道上的电子恰好半满,则该元素的原子序数为________ ,其离子的电子排布式为______________________________________ 。
(2)某元素的原子基态时有6个电子处于3d轨道上,则该元素的原子序数为
(3)某元素的基态原子失去3个电子后,它的3d轨道上的电子恰好半满,则该元素的原子序数为
更新时间:2019/06/23 19:07:39
|
相似题推荐
【推荐1】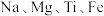 等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(2) 原子的核外电子,有
原子的核外电子,有___________ 种空间运动状态。
(3) 元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
(4) 原子位于元素周期表中的
原子位于元素周期表中的___________ 区,其价电子排布式为___________ 。与 同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为___________ 。
(5) 与
与 的离子半径大小关系为
的离子半径大小关系为
___________  (填“大于”或“小于)。
(填“大于”或“小于)。
(6)下列各组多电子原子的能级能量比较不正确的是___________。
① ②
② ③
③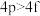 ④
④
(7)很多金属及其化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识解释产生此现象的原因是___________ 。
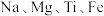 等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:(1)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(2)
 原子的核外电子,有
原子的核外电子,有(3)
 元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。A.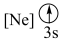 | B.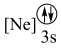 | C.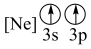 | D.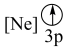 |
(4)
 原子位于元素周期表中的
原子位于元素周期表中的 同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为(5)
 与
与 的离子半径大小关系为
的离子半径大小关系为
 (填“大于”或“小于)。
(填“大于”或“小于)。(6)下列各组多电子原子的能级能量比较不正确的是___________。
①
 ②
② ③
③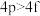 ④
④
| A.①④ | B.③④ | C.①③ | D.②③ |
(7)很多金属及其化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识解释产生此现象的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)Co基态原子核外电子排布式为___________ ;
(2)Zn2+基态核外电子排布式为____________ ;
(3)Cr3+基态核外电子排布式为____________ ;
(4)N的基态原子核外电子排布式为__________ ;Cu的基态原子最外层有_____ 个电子。
(5)Si元素基态原子的电子排布式是____________ 。
(2)Zn2+基态核外电子排布式为
(3)Cr3+基态核外电子排布式为
(4)N的基态原子核外电子排布式为
(5)Si元素基态原子的电子排布式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)Ag的核外电子排布式是[Kr]4d105s1,则Ag在元素周期表中的位置是_______ 。下列属于基态Ag+的电子排布式的是_______ 。(填标号)
A.[Kr]4d95s2 B.[Kr]4d10 C.[Kr]4d95s1
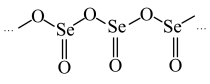
(2)硒所在的主族中,简单气态氢化物沸点最低的是________ (填化学式);硒的某种氧化物为链状聚合结构(如图所示),该氧化物的化学式为_______ 。
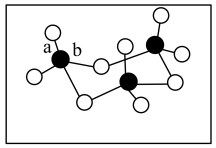
(3)固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ ,该结构中S-O键长有两类,一类键长约140pm,另一类键长约160pm,较短的键为_______ (填图中字母)。
(4)FeSO4•H2O结构如图所示。
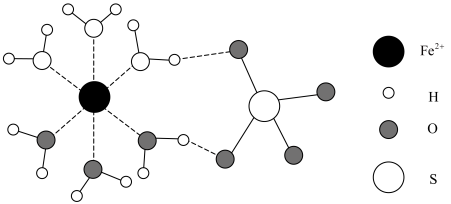
Fe2+价层电子排布式为________ 。比较SO 和H2O分子中的键角大小并给出相应解释:
和H2O分子中的键角大小并给出相应解释:_______ 。
(1)Ag的核外电子排布式是[Kr]4d105s1,则Ag在元素周期表中的位置是
A.[Kr]4d95s2 B.[Kr]4d10 C.[Kr]4d95s1
(2)硒所在的主族中,简单气态氢化物沸点最低的是

(3)固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为

(4)FeSO4•H2O结构如图所示。

Fe2+价层电子排布式为
 和H2O分子中的键角大小并给出相应解释:
和H2O分子中的键角大小并给出相应解释:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Na、Mg、C、N、O、S、Cl等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种___________ 光谱(填“发射”或“吸收”)。
(2)基态碳原子核外电子排布式为___________ ,共有___________ 种能量不同的轨道,其原子核外未成对电子数为___________ 。
(3)N、O、Mg元素的前3级电离能如下表所示:
①、②、③中为氮元素的是___________ (填序号),判断理由是___________ 。
(4)用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:___________ 。
(1)钠在火焰上灼烧产生的黄光是一种
(2)基态碳原子核外电子排布式为
(3)N、O、Mg元素的前3级电离能如下表所示:
| 元素 | 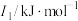 | 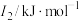 | 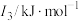 |
| ① | 737.7 | 1450.7 | 7732.7 |
| ② | 1313.9 | 3388.3 | 5300.5 |
| ③ | 1402.3 | 2856.0 | 4578.1 |
(4)用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)2p轨道上最多只能排布6个电子,其依据的规律是__________________ 。
(2)氧元素基态原子核外未成对电子数为________ 个,第三周期中有两个成单电子的元素符号________ (填一种即可),M层上有2对成对电子的原子最外层共有________ 种不同运动状态的电子。
(3)1~36号元素原子中未成对电子数为2的元素符号及价电子排布式________________ 。
(4)X元素的价电子排布式是4s24p5,X元素的符号是________ 。
(5)某元素的原子序数为33,该元素原子的价电子排布式为________ ,该元素原子核外有________ 个电子层,________ 个能级,________ 个原子轨道。
(2)氧元素基态原子核外未成对电子数为
(3)1~36号元素原子中未成对电子数为2的元素符号及价电子排布式
(4)X元素的价电子排布式是4s24p5,X元素的符号是
(5)某元素的原子序数为33,该元素原子的价电子排布式为
您最近半年使用:0次