1 . 根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)已知铬是24号元素,画出Cr的价层电子排布图:_______ 。
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序是_______ 。
(5)Zn2+的核外电子排布式为_______ 。
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)已知铬是24号元素,画出Cr的价层电子排布图:
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(5)Zn2+的核外电子排布式为
您最近半年使用:0次
2 . 过渡金属元素在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是______ 和______ 。
(2)基态钒原子核外电子的运动状态有_____ 种。
(3)A元素M层电子数是N电子数7倍,其价层电子轨道表示式________ 。
(4)C元素基态原子的轨道表示式是下图中的_____ (填“①”或“②”),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合_____ (填“A”“B”或“C”)。
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为I1)。如图所示:_____ 。
②根据图中提供的信息,可推断出I1(N)_____ I1(O)(填“>”“<”或“=”);原因是_____ 。
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是
(2)基态钒原子核外电子的运动状态有
(3)A元素M层电子数是N电子数7倍,其价层电子轨道表示式
(4)C元素基态原子的轨道表示式是下图中的
①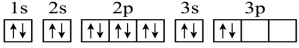
②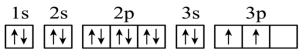
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为I1)。如图所示:
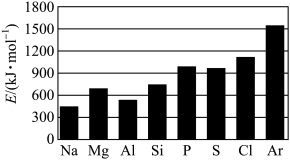
②根据图中提供的信息,可推断出I1(N)
您最近半年使用:0次
名校
解题方法
3 . 复旦大学某课题组首次实现了以芳基磺酰氯(ArSO2Cl)为引发剂的有机催化光调控活性聚合,如图所示。图中R1、R2为烷基,Ar为芳基。下列说法正确的是
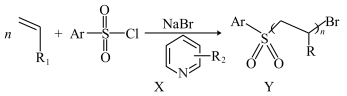
| A.基态S原子的价电子有4种运动状态 |
| B.磺酰氯(SO2Cl2)的分子构型为正四面体形 |
| C.X分子中的C、N原子均只采取sp2杂化 |
| D.Y分子属于线性高分子材料,具有热塑性 |
您最近半年使用:0次
名校
解题方法
4 . 硼和氮的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态N原子电子自旋量子数和为___________ ,其价电子中成对电子数与未成对电子数之比是___________ 。
(2)硼烷-吡啶(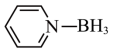 )是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是
)是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是___________ 。硼烷-吡啶组成元素属于第二周期的电负性从大到小的顺序是___________ 。
(3)吡啶(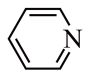 )和吡咯(
)和吡咯(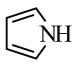 )均含有大
)均含有大 健,相同条件下,熔点吡啶
健,相同条件下,熔点吡啶___________ 吡咯(填“大于”或“小于”),其原因是___________ 。
(4)Ca与B组成的金属硼化物结构如图所示,硼原子全部组成B6正八面体,各个顶点通过B-B键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如M点原子的分数坐标为( ,
, ,
, ),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为
),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为 ___________ ,Ca与 B 原子间的最短距离d=___________ pm(列出计算式即可)。
(1)基态N原子电子自旋量子数和为
(2)硼烷-吡啶(
 )是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是
)是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是(3)吡啶(
 )和吡咯(
)和吡咯( )均含有大
)均含有大 健,相同条件下,熔点吡啶
健,相同条件下,熔点吡啶(4)Ca与B组成的金属硼化物结构如图所示,硼原子全部组成B6正八面体,各个顶点通过B-B键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为
 ,
, ,
, ),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为
),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为 
您最近半年使用:0次
5 . 根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素原子次外层电子数是最外层电子数的 ,其最外层电子的轨道表示式为
,其最外层电子的轨道表示式为___________ 。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是___________ ,在元素周期表中的位置是___________ 。
(3)C元素基态原子的轨道表示式是下图中的___________ (填序号),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合___________ (填序号)。
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量称为第一电离能(设为E)。如图所示:___________ 。
②根据图中提供的信息,可推断出E(氧)___________ (填“>”“<”或“=”,下同)E(氟)。
③根据第一电离能的含义和元素周期律可推断出E(镁)___________ E(钙)。
(1)A元素原子次外层电子数是最外层电子数的
 ,其最外层电子的轨道表示式为
,其最外层电子的轨道表示式为(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是
(3)C元素基态原子的轨道表示式是下图中的
①
②
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量称为第一电离能(设为E)。如图所示:
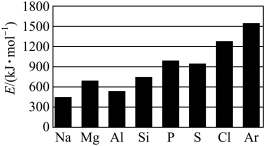
②根据图中提供的信息,可推断出E(氧)
③根据第一电离能的含义和元素周期律可推断出E(镁)
您最近半年使用:0次
名校
6 . 元素周期表前四周期W、X、Y、Z、E五种元素,W元素的原子最外层电子排布式为 ;X元素的原子价电子排布式为
;X元素的原子价电子排布式为 ;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子;
;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子; 中有5个未成对电子。
中有5个未成对电子。
(1)写出元素名称:Z___________ ;E___________ 。
(2)Y基态原子的电子排布图为___________ 。
(3)当 时,
时, 分子中,两共价键的键角为
分子中,两共价键的键角为___________ 度;当 时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是
时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是___________ 。
(4)E元素原子的价电子排布式是___________ ,在元素周期表中的位置是___________ ,按照核外电子排布,可以把元素周期表分为5个区,E元素位于周期表的___________ 区。
 ;X元素的原子价电子排布式为
;X元素的原子价电子排布式为 ;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子;
;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子; 中有5个未成对电子。
中有5个未成对电子。(1)写出元素名称:Z
(2)Y基态原子的电子排布图为
(3)当
 时,
时, 分子中,两共价键的键角为
分子中,两共价键的键角为 时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是
时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是(4)E元素原子的价电子排布式是
您最近半年使用:0次
名校
7 . 下列各项中,前面的能级先填入电子的为
①3p和4s ②2s和3s ③3d和3p ④3d和4s
①3p和4s ②2s和3s ③3d和3p ④3d和4s
| A.①③ | B.①② | C.②④ | D.①④ |
您最近半年使用:0次
名校
解题方法
8 . 下列各微粒的电子排布式或电子排布图不符合能量最低原理的是
| A.Fe2+ 1s22s22p63s23p63d6 | B.Cu 1s22s22p63s23p63d94s2 |
C.F 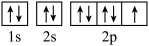 | D.Na+ 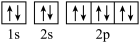 |
您最近半年使用:0次
9 . 某课题组发展了可控的 键形成策略,实现了
键形成策略,实现了 硅杂哌啶的高效合成,其反应原理如下:
硅杂哌啶的高效合成,其反应原理如下:
(1)下面B原子的电子排布图中,属于基态电子排布图的为___________ (填标号,下同),激发态电子排布图中能量最高的是___________ 。___________ (用元素符号表示)。晶体硅的熔点低于晶体硼,试解释其原因:___________ 。
(3)已知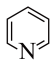 为平面结构,则合成的4-硅杂哌啶分子中,有
为平面结构,则合成的4-硅杂哌啶分子中,有 和
和 两种杂化方式的元素为
两种杂化方式的元素为___________ (填元素符号)。
(4)氮和硼可形成新型半导体材料 ,其晶胞结构如图所示,晶胞中每个
,其晶胞结构如图所示,晶胞中每个 周围最近的
周围最近的 原子个数为
原子个数为___________ 。若晶胞边长为 ,用
,用 表示阿伏加德罗常数的值,则最近的硼原子间的距离为
表示阿伏加德罗常数的值,则最近的硼原子间的距离为___________  (用含
(用含 的代数式表示),晶体密度为
的代数式表示),晶体密度为___________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
 键形成策略,实现了
键形成策略,实现了 硅杂哌啶的高效合成,其反应原理如下:
硅杂哌啶的高效合成,其反应原理如下: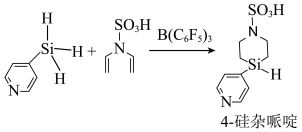
(1)下面B原子的电子排布图中,属于基态电子排布图的为
a.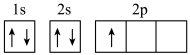 b.
b.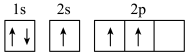
c. d.
d.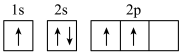
(3)已知
 为平面结构,则合成的4-硅杂哌啶分子中,有
为平面结构,则合成的4-硅杂哌啶分子中,有 和
和 两种杂化方式的元素为
两种杂化方式的元素为(4)氮和硼可形成新型半导体材料
 ,其晶胞结构如图所示,晶胞中每个
,其晶胞结构如图所示,晶胞中每个 周围最近的
周围最近的 原子个数为
原子个数为 ,用
,用 表示阿伏加德罗常数的值,则最近的硼原子间的距离为
表示阿伏加德罗常数的值,则最近的硼原子间的距离为 (用含
(用含 的代数式表示),晶体密度为
的代数式表示),晶体密度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
解题方法
10 . 下面是第二周期部分元素基态原子的轨道表示式,据此判断下列说法错误的是
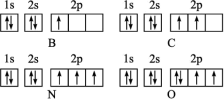
| A.每个原子轨道里最多只能容纳2个电子 |
| B.电子排在同一能级时,总是优先单独占据一个轨道 |
| C.每个能层所具有的能级数等于能层的序数(n) |
| D.若一个能级中有2个电子,则其自旋一定相反 |
您最近半年使用:0次



