23-24高一下·全国·课前预习
1 . 构造原理
随着原子_____ 的递增,绝大多数元素的原子核外电子将遵循以下顺序填充到各能级中:1s、2s、2p、3s、3p、4s、_____ 、4p、5s、_____ 、5p、6s、_____ 、_____ 、6p、7s……这个排列顺序被称为构造原理。(见教材P6构造原理示意图)
随着原子
您最近半年使用:0次
23-24高一下·全国·课前预习
2 . 电子排布式
(1)元素原子的电子排布式中能级符号右上角的数字是该能级上_____ 。钾原子的电子排布式为_____ 。
(2)为了书写方便,通常还会将电子排布式进行简化,用稀有气体结构代替已经充满的电子层。示例:Fe1s22s22p63s23p63d64s2,简化电子排布式是_____ 。
(3)写出Na、Cl、Ca的电子排布式:
Na:_____ 、Cl:_____ 、Ca:_____ 。
或者简写为:
Na:_____ 、Cl:_____ 、Ca:_____ 。
(1)元素原子的电子排布式中能级符号右上角的数字是该能级上
(2)为了书写方便,通常还会将电子排布式进行简化,用稀有气体结构代替已经充满的电子层。示例:Fe1s22s22p63s23p63d64s2,简化电子排布式是
(3)写出Na、Cl、Ca的电子排布式:
Na:
或者简写为:
Na:
您最近半年使用:0次
名校
3 . 下列说法中一定错误的是
| A.某原子K层上只有一个电子 |
| B.某阳离子的核电荷数与最外层电子数相等 |
| C.某原子M层上电子数为L层上电子数的4倍 |
| D.某离子M层上和L层上的电子数均为K层的4倍 |
您最近半年使用:0次
4 .  最稳定的价态为+3价,因为符合了
最稳定的价态为+3价,因为符合了___________ (填规则名称)
 最稳定的价态为+3价,因为符合了
最稳定的价态为+3价,因为符合了
您最近半年使用:0次
名校
解题方法
5 . 下列有关构造原理的说法错误的是
| A.原子核外电子填充3p、3d、4s能级的顺序为3p→4s→3d |
| B.某基态原子部分核外电子的排布式为3d64s2 |
| C.所有基态原子的核外电子排布都遵循构造原理 |
| D.构造原理中的电子排布能级顺序,源于光谱学事实 |
您最近半年使用:0次
2023-12-25更新
|
325次组卷
|
5卷引用:山东省潍坊市临朐县第一中学2023-2024学年高一上学期12月月考化学试题
山东省潍坊市临朐县第一中学2023-2024学年高一上学期12月月考化学试题陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题(已下线)1.1.2 构造原理与电子排布式 电子云与原子轨道(巩固)(已下线)名校期中好题汇编-原子结构与性质(选择题)名校期中好题汇编-原子结构与性质(选择题)
名校
6 . M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法不正确 的是
A.基态原子未成对电子数: |
B.电负性: |
C.基态原子的第一电离能: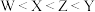 |
| D.W基态原子的电子的空间运动状态有5种 |
您最近半年使用:0次
名校
7 . 下列说法中正确的是
| A.原子的核外电子都是先排满前一个电子层,才能排进下一个电子层 |
| B.核外电子层结构相同的原子,一定属于同种元素 |
| C.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| D.非金属元素原子最外层电子数不一定都大于4 |
您最近半年使用:0次
名校
8 . 下列叙述错误的是
①热稳定性:
②熔点: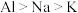
③IA,ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤多电子原子中,在离核较近的区域内运动的电子能量较高
⑥盐酸可以与碳酸钠溶液反应生成 气体,说明盐酸比碳酸酸性强,Cl比C的非金属性强
气体,说明盐酸比碳酸酸性强,Cl比C的非金属性强
⑦ 、
、 分子中各原子最外层均达到8电子稳定结构。
分子中各原子最外层均达到8电子稳定结构。
①热稳定性:

②熔点:
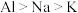
③IA,ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤多电子原子中,在离核较近的区域内运动的电子能量较高
⑥盐酸可以与碳酸钠溶液反应生成
 气体,说明盐酸比碳酸酸性强,Cl比C的非金属性强
气体,说明盐酸比碳酸酸性强,Cl比C的非金属性强⑦
 、
、 分子中各原子最外层均达到8电子稳定结构。
分子中各原子最外层均达到8电子稳定结构。| A.①③⑤⑥ | B.②④⑥ | C.②③④⑦ | D.①⑤⑥ |
您最近半年使用:0次
9 . 下列有关原子核外电子排布的说法错误的是
| A.电子总是优先排布在能量最低的电子层里 |
| B.每个电子层最多能容纳的电子数为2n2 |
| C.最外层电子数不超过8个(K层为最外层时不超过2个) |
| D.S2-的M层电子数有6个电子 |
您最近半年使用:0次
10 . 下列有关说法错误的是
| A.处于最低能量状态的原子叫作基态原子 |
| B.价电子层有2个未成对电子的原子一定属于主族元素 |
| C.玻尔原子结构模型可以较好地解释氢原子的可见光谱线 |
| D.利用电负性可判断化合物中元素化合价的正负及化学键的性质 |
您最近半年使用:0次



