解题方法
1 . 下列化学用语或图示表达不正确 的是
A.反-2-丁烯的分子结构模型: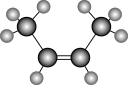 |
B.质量数为2的 ,其核素符号是: ,其核素符号是: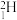 |
C. 的 的 模型: 模型: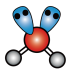 |
D. 价层电子轨道表示式为: 价层电子轨道表示式为: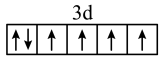 |
您最近一年使用:0次
2 . 锰酸锂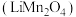 是较有前景的锂离子正极材料之一,相比钴酸锂等传统正极材料,锰酸锂具有资源丰富、成本低、无污染、安全性好、倍率性能好等优点,是理想的动力电池正极材料。一种以废旧电池正极材料(主要成分为
是较有前景的锂离子正极材料之一,相比钴酸锂等传统正极材料,锰酸锂具有资源丰富、成本低、无污染、安全性好、倍率性能好等优点,是理想的动力电池正极材料。一种以废旧电池正极材料(主要成分为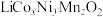 ,含少量铝箔、炭黑和有机黏合剂)为原料制备
,含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
(1)基态Mn原子的价层电子排布图为_______ ;由排布图可知Mn位于元素周期表中的_______ 区。
(2)“灼烧”时通入足量空气,目的是_______ 。
(3)“碱浸”的目的是_______ 。
(4)“酸浸”中双氧水作还原剂的优点是_______ ,_______ (填“能”或“不能”)用 代替双氧水。
代替双氧水。
(5)“沉锰”过程中生成 的离子方程式为
的离子方程式为_______ {已知: 的结构为
的结构为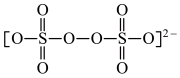 }。
}。
(6) 热失重图像如图所示。c点得到的固体的化学式为
热失重图像如图所示。c点得到的固体的化学式为_______ 。
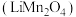 是较有前景的锂离子正极材料之一,相比钴酸锂等传统正极材料,锰酸锂具有资源丰富、成本低、无污染、安全性好、倍率性能好等优点,是理想的动力电池正极材料。一种以废旧电池正极材料(主要成分为
是较有前景的锂离子正极材料之一,相比钴酸锂等传统正极材料,锰酸锂具有资源丰富、成本低、无污染、安全性好、倍率性能好等优点,是理想的动力电池正极材料。一种以废旧电池正极材料(主要成分为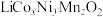 ,含少量铝箔、炭黑和有机黏合剂)为原料制备
,含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
(1)基态Mn原子的价层电子排布图为
(2)“灼烧”时通入足量空气,目的是
(3)“碱浸”的目的是
(4)“酸浸”中双氧水作还原剂的优点是
 代替双氧水。
代替双氧水。(5)“沉锰”过程中生成
 的离子方程式为
的离子方程式为 的结构为
的结构为 }。
}。(6)
 热失重图像如图所示。c点得到的固体的化学式为
热失重图像如图所示。c点得到的固体的化学式为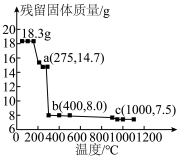
您最近一年使用:0次
解题方法
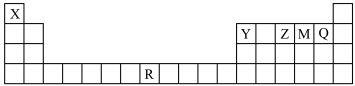
3 . 下表为元素周期表的一部分,每个字母分别代表一种元素。
(1)元素Y、Z、M、Q中,原子半径最大的是_______ (填元素名称)。
(2)基态Q原子中,其占据的最高能层的符号是_______ ,其最高能级的原子轨道的形状是_______ 。
(3)下列关于R的说法正确的是_______ (填序号)。
①R的原子序数为26
②依据核外电子排布,把元素周期表划分为5个区,R位于ds区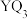 的中心原子杂化轨道类型为
的中心原子杂化轨道类型为_______ ,键角为_______ 。 的空间结构名称为
的空间结构名称为_______ 。
(1)元素Y、Z、M、Q中,原子半径最大的是
(2)基态Q原子中,其占据的最高能层的符号是
(3)下列关于R的说法正确的是
①R的原子序数为26
②依据核外电子排布,把元素周期表划分为5个区,R位于ds区
③基态 的价层电子轨道表示式为
的价层电子轨道表示式为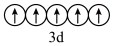
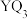 的中心原子杂化轨道类型为
的中心原子杂化轨道类型为 的空间结构名称为
的空间结构名称为
您最近一年使用:0次
4 . 宋代《千里江山图》历经千年色彩依然,所用颜料由石绿、雌黄、赭石、碎碟、朱砂等绘制而成,其中含有硅、铜、锌、铁等元素。
(1)基态铁原子的核外电子排布式为_______ ;基态Fe2+核外电子的空间运动状态有_______ 种,其电子占据的最高能层符号为_______ 。
(2)研究发现,阳离子的颜色与未成对电子数有关,例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色的原因是_______ 。
(3)铜、锌两种元素的第一电离能、第二电离能如下表所示。元素2在周期表中位于第四周期第_______ 族,解释元素2的 远远大于
远远大于 的主要原因是
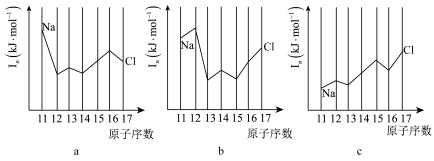
的主要原因是_______ 。用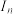 表示元素的第n电离能,则图中的a、b、c分别代表第三周期元素的
表示元素的第n电离能,则图中的a、b、c分别代表第三周期元素的_______ (填“ ”、“
”、“ ”或“
”或“ ”)随原子序数递增的变化。
”)随原子序数递增的变化。
_______ 。已知电负性Cl>H>Si,则SiHCl3中H的化合价为_______ ,SiHCl3在浓NaOH溶液中发生反应的化学方程式为_______ 。
(1)基态铁原子的核外电子排布式为
(2)研究发现,阳离子的颜色与未成对电子数有关,例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色的原因是
(3)铜、锌两种元素的第一电离能、第二电离能如下表所示。元素2在周期表中位于第四周期第
 远远大于
远远大于 的主要原因是
的主要原因是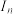 表示元素的第n电离能,则图中的a、b、c分别代表第三周期元素的
表示元素的第n电离能,则图中的a、b、c分别代表第三周期元素的 ”、“
”、“ ”或“
”或“ ”)随原子序数递增的变化。
”)随原子序数递增的变化。电离能 |  |  |
| 元素1 | 906 | 1733 |
| 元素2 | 746 | 1958 |
您最近一年使用:0次
名校
5 . 下列化学用语表述正确的是
A. 的电子式: 的电子式: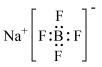 |
B.基态Si原子的价层电子轨道表示式: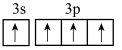 |
C.HCl分子中 键的电子云轮廓图: 键的电子云轮廓图: |
D. 的VSEPR模型: 的VSEPR模型: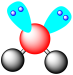 |
您最近一年使用:0次
7日内更新
|
228次组卷
|
3卷引用:陕西省渭南高级中学2025届高三上学期9月份联考化学试题
6 . 乙二醇(结构如图所示)可用于生产汽车的防冻液,下列说法正确的是
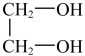
| A.乙二醇中既含有非极性共价键,又含有极性共价键 |
B. 的电子式为 的电子式为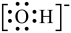 |
| C.基态碳原子核外有5种不同运动状态的电子 |
D.基态氧原子的轨道表示式为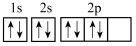 |
您最近一年使用:0次
7日内更新
|
13次组卷
|
2卷引用:广东省部分学校2023-2024学年高二上学期期末教学质量监测化学试卷
7 . 化学反应中常伴随着能量的变化。回答下列问题:
(1)S8分子可形成单斜硫和斜方硫,转化过程为: ,则S(单斜)与S(斜方)相比,较稳定的是
,则S(单斜)与S(斜方)相比,较稳定的是______ ,基态S原子的原子核外电子有___ 种空间运动状态,其能量最高的电子电子云轮廓图为____ 形。
(2)Cu的价层电子排布式为_____ ,位于在周期表______ 区(填s、p、d或ds)。
(3)下列属于氧原子激发态的轨道表示式的有_____ (填字母)。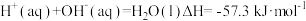 ,则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量
,则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量_____ (填“>”“<”或“=”)57.3kJ。
(5)1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化如图所示:_____ (填“增大”“减小”或“不变”)。
②写出NO2和CO反应的热化学方程式____ 。
(6)标准摩尔生成焓是指在25℃和101kPa时,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa时下列反应:
①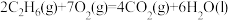
 ;
;
②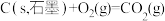
 ;
;
③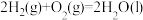
 。
。
写出乙烷(C2H6)标准摩尔生成焓的焓变
____ (用含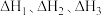 的式子表示)。
的式子表示)。
(1)S8分子可形成单斜硫和斜方硫,转化过程为:
 ,则S(单斜)与S(斜方)相比,较稳定的是
,则S(单斜)与S(斜方)相比,较稳定的是(2)Cu的价层电子排布式为
(3)下列属于氧原子激发态的轨道表示式的有
a.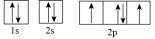 b.
b.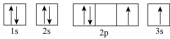
c.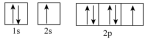 d.
d.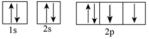
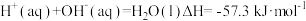 ,则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量
,则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量(5)1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化如图所示:
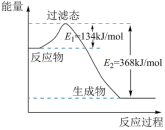
②写出NO2和CO反应的热化学方程式
(6)标准摩尔生成焓是指在25℃和101kPa时,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa时下列反应:
①
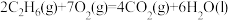
 ;
;②
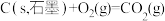
 ;
;③
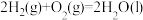
 。
。写出乙烷(C2H6)标准摩尔生成焓的焓变

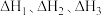 的式子表示)。
的式子表示)。
您最近一年使用:0次
名校
解题方法
8 . 下列化学用语或图示表达正确的是
A.基态C原子价电子排布图: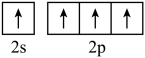 |
B.邻羟基苯甲醛的分子内氢键: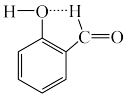 |
C.顺-2-丁烯的球棍模型: |
D.丙炔的键线式: |
您最近一年使用:0次
9 . 钛(Ti)被称为继铁、铝之后的第三金属,金属钛素有“太空金属”、“海洋金属”、“未来金属”等美誉,钛合金与骨骼具有很好的兼容性,因此钛是最好的人造骨材料。我国某高校科研团队设计在1150℃时电解 制备金属钛的装置如图所示,回答以下问题:
制备金属钛的装置如图所示,回答以下问题:_______ ,基态钛原子的价层电子轨道表示式为_______ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有_______ 种。
(2)下列状态的钛元素形成的微粒中,电离其最外层的一个电子所需能量最小的是_______(填序号)
(3) 直接电解法生产钛是一种较先进的方法。X接电源
直接电解法生产钛是一种较先进的方法。X接电源_______ 极,Y极主要产生一氧化碳气体,写出生成一氧化碳的电极反应式_______ 。
(4)当由 制得4.8g金属Ti时,理论上外电路转移
制得4.8g金属Ti时,理论上外电路转移_______ mol电子。
(5)若以二甲醚( )、空气、氢氧化钾溶液为原料,多孔石墨为电极构成的燃料电池提供上述电解的电源,则该电池工作时负极的电极反应式为
)、空气、氢氧化钾溶液为原料,多孔石墨为电极构成的燃料电池提供上述电解的电源,则该电池工作时负极的电极反应式为_______ 。
 制备金属钛的装置如图所示,回答以下问题:
制备金属钛的装置如图所示,回答以下问题: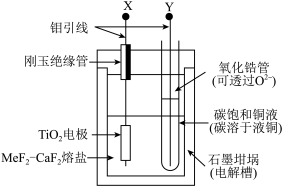
(2)下列状态的钛元素形成的微粒中,电离其最外层的一个电子所需能量最小的是_______(填序号)
A.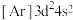 | B. | C.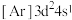 | D.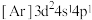 |
(3)
 直接电解法生产钛是一种较先进的方法。X接电源
直接电解法生产钛是一种较先进的方法。X接电源(4)当由
 制得4.8g金属Ti时,理论上外电路转移
制得4.8g金属Ti时,理论上外电路转移(5)若以二甲醚(
 )、空气、氢氧化钾溶液为原料,多孔石墨为电极构成的燃料电池提供上述电解的电源,则该电池工作时负极的电极反应式为
)、空气、氢氧化钾溶液为原料,多孔石墨为电极构成的燃料电池提供上述电解的电源,则该电池工作时负极的电极反应式为
您最近一年使用:0次
10 . 下列化学用语正确的是
A.乙烯的球棍模型: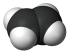 |
B.基态 的价层电子排布式: 的价层电子排布式: |
C.HClO的电子式: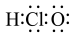 |
D.基态 电子排布的轨道表示式: 电子排布的轨道表示式: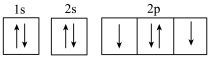 |
您最近一年使用:0次



