1 . 以邻硝基苯甲醛合成吲哚的反应如下,下列说法正确的是
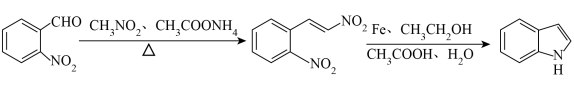
A.基态 的价电子排布图: 的价电子排布图: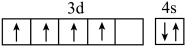 |
B.基态原子未成对电子数: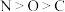 |
C. 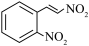 分子中有手性碳原子 分子中有手性碳原子 |
D. 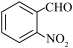 分子中 分子中 和 和 原子均是 原子均是 杂化 杂化 |
您最近半年使用:0次
2 . 按要求回答下列问题:
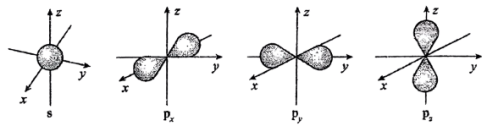
(1)如图是s能级和p能级的电子云轮廓图,试回答问题。______ 形,每个p能级有______ 个原子轨道。
(2)按要求作答:
①画出氯原子结构示意图______ ;
②写出基态O核外电子排布式为:______ ;
③写出基态N的原子轨道表示式:______ ;
(3)Sm的价层电子排布式为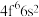 ,则
,则 价层电子排布式为
价层电子排布式为______ 。
(1)如图是s能级和p能级的电子云轮廓图,试回答问题。
(2)按要求作答:
①画出氯原子结构示意图
②写出基态O核外电子排布式为:
③写出基态N的原子轨道表示式:
(3)Sm的价层电子排布式为
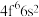 ,则
,则 价层电子排布式为
价层电子排布式为
您最近半年使用:0次
名校
解题方法
3 . 下列化学用语表达不正确的是
A.H2O的电子式: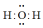 |
B.基态氧原子的轨道表示式: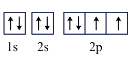 |
C.H2O中心原子的VSEPR模型: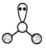 |
| D.H2O分子的空间结构:V形 |
您最近半年使用:0次
2024·浙江·模拟预测
解题方法
4 . 下列说法不正确 的是
A.Fe2+的价层电子轨道表示式为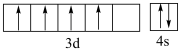 |
B.用电子式表示K2S的形成: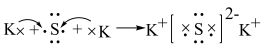 |
| C.HClO的分子的VSEPR模型为四面体形 |
D.聚已二酰己二胺的结构简式: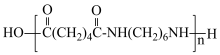 |
您最近半年使用:0次
名校
5 . 铜及其化合物在生活、生产中用途广泛。以黄铜矿为原料冶炼铜涉及多个反应,其中一个反应为
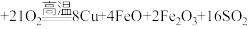 。回答下列问题:
。回答下列问题:
(1)基态铜原子的价层电子的轨道表示式(电子排布图)为___________ ,基态铜原子核外电子的空间运动状态(原子轨道)有___________ 种。
(2)高温下CuO能转化为 的原因是
的原因是___________ (从原子结构角度分析)。
(3) 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是___________ ,属于极性分子的是___________ 。
(4) 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是___________ ,1360℃是___________ 的熔点。
(5) 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为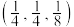 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为___________ 。晶胞参数分别为a pm,a pm、2a pm, 晶体的密度为
晶体的密度为___________  (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。

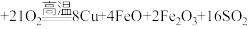 。回答下列问题:
。回答下列问题:(1)基态铜原子的价层电子的轨道表示式(电子排布图)为
(2)高温下CuO能转化为
 的原因是
的原因是(3)
 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是(4)
 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是(5)
 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为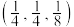 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为 晶体的密度为
晶体的密度为 (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。
您最近半年使用:0次
名校
解题方法
6 . 硼、氮、镁、铝是重要的短周期元素,它们能形成多种重要的化合物。请回答下列问题:
(1)基态Al原子处于最高能级的电子云轮廓图为_______ 形,基态 的核外电子的轨道表达式为
的核外电子的轨道表达式为_______ 。
(2)硼的氢化物叫硼烷( ),如
),如 (乙硼烷)。
(乙硼烷)。 与
与 反应生成
反应生成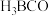 ,
,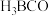 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为_______ 。
(3)离子化合物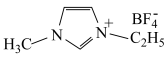 是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。
是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。
①图A、B、C分别表示C、N、O、F的逐级电离能I的变化趋势(纵坐标的标度不同),第一电离能 的变化图是
的变化图是_______ (填序号,下同);第三电离能 的变化图是
的变化图是_______ 。 、
、 和
和 在小立方体中的分布如图2、图3所示。
在小立方体中的分布如图2、图3所示。 的配位数为
的配位数为_______ ,晶体的化学式为_______ 。
②已知 之间的最小间距apm,晶体的密度为d
之间的最小间距apm,晶体的密度为d ,则阿伏加德罗常数的表达式为
,则阿伏加德罗常数的表达式为_______  (用含a、d的式子表示)。
(用含a、d的式子表示)。
(1)基态Al原子处于最高能级的电子云轮廓图为
 的核外电子的轨道表达式为
的核外电子的轨道表达式为(2)硼的氢化物叫硼烷(
 ),如
),如 (乙硼烷)。
(乙硼烷)。 与
与 反应生成
反应生成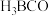 ,
,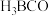 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为(3)离子化合物
 是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。
是离子液体。离子液体是在室温和接近室温时呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。①图A、B、C分别表示C、N、O、F的逐级电离能I的变化趋势(纵坐标的标度不同),第一电离能
 的变化图是
的变化图是 的变化图是
的变化图是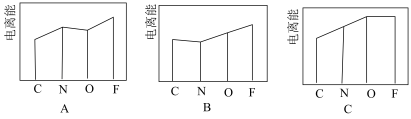
②离子化合物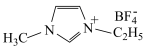 中阳离子存在大
中阳离子存在大 键
键 ,该化合物中杂化方式为
,该化合物中杂化方式为 的原子共有
的原子共有
 、
、 和
和 在小立方体中的分布如图2、图3所示。
在小立方体中的分布如图2、图3所示。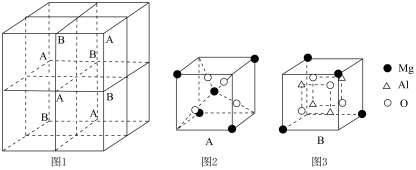
 的配位数为
的配位数为②已知
 之间的最小间距apm,晶体的密度为d
之间的最小间距apm,晶体的密度为d ,则阿伏加德罗常数的表达式为
,则阿伏加德罗常数的表达式为 (用含a、d的式子表示)。
(用含a、d的式子表示)。
您最近半年使用:0次
2024高三·全国·专题练习
7 . 《天工开物》记载,ZnCO3与木炭共热制得倭铅(锌)。下列说法错误的是
| A.Zn元素位于ds区 |
| B.制备锌的过程可能发生置换反应 |
C.基态碳原子的轨道表示式为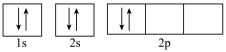 |
D. 为平面正三角形结构 为平面正三角形结构 |
您最近半年使用:0次
8 . 请回答下列问题:
(1)基态氟原子核外9个电子,这些电子的电子云形状有___________ 种;氟原子有___________ 种不同能量的电子,价层电子的轨道表示式为___________ 。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:___________ ;Cl-中有___________ 种运动状态不同的电子。
(3)某元素简化电子排布式为[Xe]4f46s2,其应在___________ 区。
(4)Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为___________ ,外围电子排布为3d104s2的元素在周期表中的位置是 ___________ 。
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列___________ 。
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
(1)基态氟原子核外9个电子,这些电子的电子云形状有
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:
(3)某元素简化电子排布式为[Xe]4f46s2,其应在
(4)Li、B、H元素的电负性由大到小的排列顺序为
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
您最近半年使用:0次
7日内更新
|
57次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
9 . 下列化学用语表示正确的是
A.用电子式表示HCl的形成过程: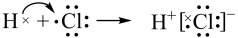 |
B.2-丁烯的键线式: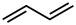 |
C.邻羟基苯甲醛分子内氢键示意图: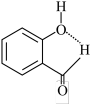 |
D.基态氧原子核外电子轨道表示式: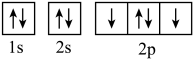 |
您最近半年使用:0次
7日内更新
|
508次组卷
|
3卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
名校
解题方法
10 . 下列化学用语不正确的是
A.基态 的价电子轨道表示式: 的价电子轨道表示式: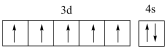 |
B.中子数为143的U原子: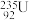 |
C.基态Ca原子核外电子占据的最高能级原子轨道示意图: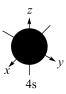 |
D.HCl分子中 键的形成: 键的形成: |
您最近半年使用:0次



