2024·北京·模拟预测
1 . 下列有关物质结构与性质的说法正确的是
| A.雪花是天空中的水汽经凝华而来的一种晶体,其六角形形状与氢键的方向性有关 |
| B.某基态原子的价层电子排布为4d25s2,该原子N层上有3个空轨道 |
| C.C=C键的键能比C—C键的大,所以碳碳双键的化学性质比碳碳单键稳定 |
| D.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
您最近半年使用:0次
名校
2 . 科学家合成了一种含硼阴离子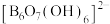 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是
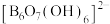 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是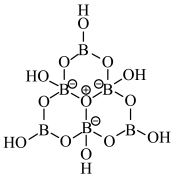
| A.基态硼原子的核外电子的空间运动状态有3种 |
| B.电负性大小为:O>B>H |
| C.该结构中硼原子的杂化方式为sp2、sp3 |
| D.该结构中共有4种不同化学环境的氧原子 |
您最近半年使用:0次
今日更新
|
214次组卷
|
2卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
3 . 硅材料在生产、生活中占有重有地位。回答下列问题:
(1)基态 原子的电子排布式
原子的电子排布式___________ 。
(2)某含硅化合物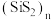 的长链状结构(片段)截取部分如图所示。该化合物的晶体类型是
的长链状结构(片段)截取部分如图所示。该化合物的晶体类型是___________ 。
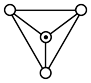
(4)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中。硅酸盐中的阴离子结构丰富多样,既有有限数目的硅氧四面体构成的简单阴离子 (图a),也有以硅氧四面体结构单元构成的
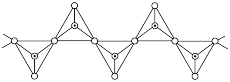
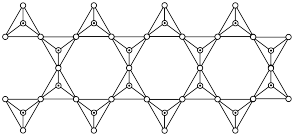
(图a),也有以硅氧四面体结构单元构成的无限 延长的单链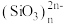 (图b)、双链(图c)等更复杂的结构。
(图b)、双链(图c)等更复杂的结构。
写出图c所示阴离子的化学式___________ 。
(5)碳和硅的有关化学键键能、键长如下所示:
硅与碳同族,也有系列含氢化合物,但硅的含氢化合物在种类和数量上都远不如碳的含氢化合物多,试从共价键的成键角度解释原因___________ 。
(6)已知 晶体的密度为
晶体的密度为 ,其晶胞结构如图所示。阿伏加德罗常数值为
,其晶胞结构如图所示。阿伏加德罗常数值为 ,则晶胞中两个
,则晶胞中两个 原子之间的距离为
原子之间的距离为___________  。
。
(1)基态
 原子的电子排布式
原子的电子排布式(2)某含硅化合物
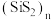 的长链状结构(片段)截取部分如图所示。该化合物的晶体类型是
的长链状结构(片段)截取部分如图所示。该化合物的晶体类型是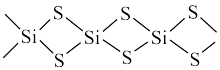
A.在晶体 和晶体 和晶体 结构中 结构中 均是 均是 杂化 杂化 |
B.常温下粗硅与盐酸反应制取 ,再以 ,再以 高温还原得到高纯硅 高温还原得到高纯硅 |
C. 比 比 易水解原因之一是 易水解原因之一是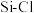 键能弱于 键能弱于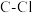 |
D. 晶体的X射线图谱显示有明锐的衍射峰 晶体的X射线图谱显示有明锐的衍射峰 |
(4)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中。硅酸盐中的阴离子结构丰富多样,既有有限数目的硅氧四面体构成的简单阴离子
 (图a),也有以硅氧四面体结构单元构成的
(图a),也有以硅氧四面体结构单元构成的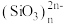 (图b)、双链(图c)等更复杂的结构。
(图b)、双链(图c)等更复杂的结构。
|
|
|
| 图a | 图b | 图c |
(5)碳和硅的有关化学键键能、键长如下所示:
| 化学键 |  | 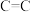 |  |  |  | 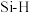 |
键能/ | 348 | 615 | 812 | 413 | 226 | 318 |
键长/ | 154 | 133 | 120 | 109 | 235 | 150 |
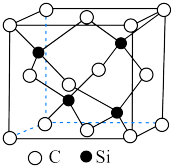
(6)已知
 晶体的密度为
晶体的密度为 ,其晶胞结构如图所示。阿伏加德罗常数值为
,其晶胞结构如图所示。阿伏加德罗常数值为 ,则晶胞中两个
,则晶胞中两个 原子之间的距离为
原子之间的距离为 。
。
您最近半年使用:0次
4 . 请回答下列问题:
(1)基态氟原子核外9个电子,这些电子的电子云形状有___________ 种;氟原子有___________ 种不同能量的电子,价层电子的轨道表示式为___________ 。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:___________ ;Cl-中有___________ 种运动状态不同的电子。
(3)某元素简化电子排布式为[Xe]4f46s2,其应在___________ 区。
(4)Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为___________ ,外围电子排布为3d104s2的元素在周期表中的位置是 ___________ 。
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列___________ 。
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
(1)基态氟原子核外9个电子,这些电子的电子云形状有
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:
(3)某元素简化电子排布式为[Xe]4f46s2,其应在
(4)Li、B、H元素的电负性由大到小的排列顺序为
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
5 . 从铜阳极泥(含有Se、Cu2S、Ag2Se及少量Au等)中分批提取硒、银、铜、金的过程如下:_______ 。
①Se的价层电子排布图为_______ 。
②SeO2蒸气中存在二聚态的SeO2,二聚态的SeO2结构中存在四元环结构。写出该二聚态的结构式:_______ 。
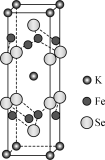
③某铁硒基电极材料晶胞结构如图所示,其化学式为_______ 。
(3)测定某粗硒样品中硒的含量:准确称量0.2000g粗硒样品,用浓硫酸将样品中的Se氧化得到SeO2;生成的SeO2加入硫酸酸化的KI溶液中充分反应。用0.4000mol·L-1的Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液20.00mL。计算粗硒样品中硒的质量分数为_______ 。
实验测定原理为SeO2+I-+H+→Se+I2+H2O;I2+ =I-+
=I-+ (未配平)。
(未配平)。
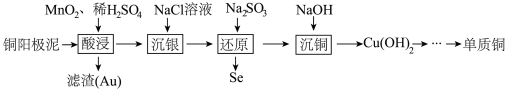
①Se的价层电子排布图为
②SeO2蒸气中存在二聚态的SeO2,二聚态的SeO2结构中存在四元环结构。写出该二聚态的结构式:
③某铁硒基电极材料晶胞结构如图所示,其化学式为
(3)测定某粗硒样品中硒的含量:准确称量0.2000g粗硒样品,用浓硫酸将样品中的Se氧化得到SeO2;生成的SeO2加入硫酸酸化的KI溶液中充分反应。用0.4000mol·L-1的Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液20.00mL。计算粗硒样品中硒的质量分数为
实验测定原理为SeO2+I-+H+→Se+I2+H2O;I2+
 =I-+
=I-+ (未配平)。
(未配平)。
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
6 . 以镉铁矿(主要成分为CdO2)为原料制备Cd(BrO3)2的部分工艺流程如下:
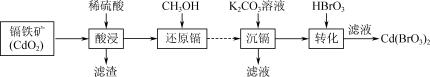
| A.已知Cd在周期表中位于第五周期IIB族,则Cd的价层电子排布式是4d105s2 |
| B.还原镉时可产生CO2,该反应中氧化剂与还原剂的物质的量之比为1∶3 |
C.“沉镉”所得滤液中的 ,其空间构型是正四面体形 ,其空间构型是正四面体形 |
| D.“转化”中发生的反应为CdCO3+2HBrO3=Cd(BrO3)2+CO2↑+H2O |
您最近半年使用:0次
2024高三·全国·专题练习
7 . THPC即四羟甲基氯化磷[P(CH2OH)4Cl],主要用于织物阻燃剂,制取THPC反应的化学方程式为4HCHO+HCl+PH3=P(CH2OH)4Cl,下列有关说法正确的是
| A.基态P原子核外电子的空间运动状态有9种 |
| B.PH3属于非极性分子 |
C.Cl-的结构示意图为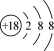 |
D.羟基的电子式为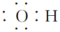 |
您最近半年使用:0次
解题方法
8 . 镧镍合金是一种储氢材料,其晶胞可认为由两种结构不同的层交替堆积而成,如下图所示,该合金的密度为p g·cm-3.已知该合金的晶胞中最多可容纳9个氢原子。下列叙述错误的是
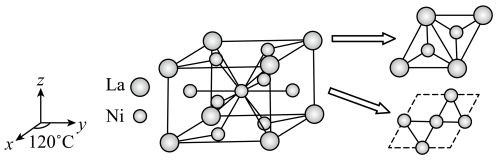
| A.基态Ni原子的价电子排布式为3d84s2 |
| B.该合金的化学式为LaNi5 |
C.设La的原子坐标为(0,0,0),则晶胞底面上Ni的原子坐标为系( , ,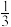 ,0)或( ,0)或( , , ,0) ,0) |
D.假定吸氢后体积不变,则合金中氢的最大密度为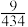 ρg·cm-3 ρg·cm-3 |
您最近半年使用:0次
名校
9 . Ⅰ.原子序数依次递增的短周期Q、W、X、Y、Z五种元素,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。(涉及元素时用对应的元素符号表示)
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是___________ 。
(2) 与
与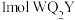 所含
所含 键的比值为
键的比值为___________ 。
(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为___________ 。
①该化合物的化学式为:___________ 。
②预测该化合物熔点应___________ 金刚石(填“高于”或“低于”)。
Ⅱ.铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(5) 可以与
可以与 、
、 、有机分子等形成配合物。基态
、有机分子等形成配合物。基态 的外围电子排布式为
的外围电子排布式为___________ 。
(6)普鲁士蓝俗称铁蓝,结构如图甲所示( 未画出),平均每两个立方体中含有一个
未画出),平均每两个立方体中含有一个 ,该晶体的化学式为
,该晶体的化学式为___________ 。又知该晶体中铁元素有 价和
价和 价两种,则
价两种,则 与
与 的个数比为
的个数比为___________ 。
(7)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为___________ ,两种晶体中空间利用率较高的是___________ 。(填“图乙”或“图丙”)
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是
(2)
 与
与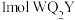 所含
所含 键的比值为
键的比值为(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为

①该化合物的化学式为:
②预测该化合物熔点应
Ⅱ.铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(5)
 可以与
可以与 、
、 、有机分子等形成配合物。基态
、有机分子等形成配合物。基态 的外围电子排布式为
的外围电子排布式为(6)普鲁士蓝俗称铁蓝,结构如图甲所示(
 未画出),平均每两个立方体中含有一个
未画出),平均每两个立方体中含有一个 ,该晶体的化学式为
,该晶体的化学式为 价和
价和 价两种,则
价两种,则 与
与 的个数比为
的个数比为(7)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为

您最近半年使用:0次
10 . 铜氨溶液含有 ,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。
,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。
(1) 溶液呈蓝色是因为含有水合铜离子
溶液呈蓝色是因为含有水合铜离子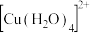 ,结构示意图如图所示:基态
,结构示意图如图所示:基态 原子核外电子排布式为
原子核外电子排布式为_______ 。
向 溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含
溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含 的铜氨溶液。
的铜氨溶液。
①比较键角:NH3_______ NH (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
②该实验中, 与
与 结合能力
结合能力_______ (填“大于”“小于”或“等于”) 与
与 结合能力,解释原因:
结合能力,解释原因:_______ 。
③经实验发现:金属铜与氨水和过氧化氢的混合溶液反应也可得到 。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是_______ ,反应的离子方应程式为_______ 。
(3)某种铜的氯化物晶胞形状为立方体,结构如图所示。
已知该晶胞的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则该晶胞的边长为
。则该晶胞的边长为_______  (列出计算式)。
(列出计算式)。
 ,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。
,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。(1)
 溶液呈蓝色是因为含有水合铜离子
溶液呈蓝色是因为含有水合铜离子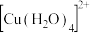 ,结构示意图如图所示:基态
,结构示意图如图所示:基态 原子核外电子排布式为
原子核外电子排布式为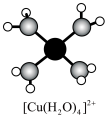
向
 溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含
溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含 的铜氨溶液。
的铜氨溶液。①比较键角:NH3
 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。②该实验中,
 与
与 结合能力
结合能力 与
与 结合能力,解释原因:
结合能力,解释原因:③经实验发现:金属铜与氨水和过氧化氢的混合溶液反应也可得到
 。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是(3)某种铜的氯化物晶胞形状为立方体,结构如图所示。
已知该晶胞的密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则该晶胞的边长为
。则该晶胞的边长为 (列出计算式)。
(列出计算式)。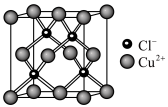
您最近半年使用:0次