1 . 核外电子排布与元素周期表的分区
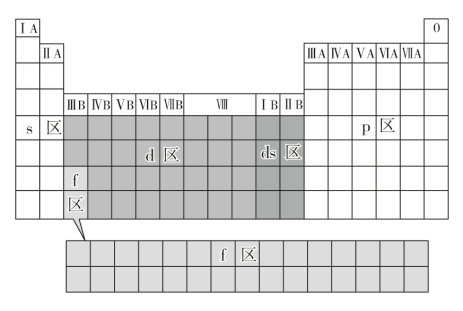
按电子排布式中最后填入电子的_______ 可将元素周期表分为s、p、d、f4个区,而IB、IIB族这2个纵行的元素的核外电子可理解为先填满了_______ 能级而后再填充_______ 能级而得名ds区。5个区的位置关系如下图所示:
按电子排布式中最后填入电子的

您最近半年使用:0次
23-24高二下·全国·课前预习
2 . 电子排布式
用数字在能级符号右上角标明该能级上排布的电子数,这就是电子排布式。写出下列基态原子的电子排布式:
(1)16S:_______ ;
(2)20Ca:_______ ;
(3)26Fe:_______ ;
(4)29Cu:_______ 。
用数字在能级符号右上角标明该能级上排布的电子数,这就是电子排布式。写出下列基态原子的电子排布式:
(1)16S:
(2)20Ca:
(3)26Fe:
(4)29Cu:
您最近半年使用:0次
23-24高一下·全国·课前预习
3 . 电子排布式
(1)元素原子的电子排布式中能级符号右上角的数字是该能级上_____ 。钾原子的电子排布式为_____ 。
(2)为了书写方便,通常还会将电子排布式进行简化,用稀有气体结构代替已经充满的电子层。示例:Fe1s22s22p63s23p63d64s2,简化电子排布式是_____ 。
(3)写出Na、Cl、Ca的电子排布式:
Na:_____ 、Cl:_____ 、Ca:_____ 。
或者简写为:
Na:_____ 、Cl:_____ 、Ca:_____ 。
(1)元素原子的电子排布式中能级符号右上角的数字是该能级上
(2)为了书写方便,通常还会将电子排布式进行简化,用稀有气体结构代替已经充满的电子层。示例:Fe1s22s22p63s23p63d64s2,简化电子排布式是
(3)写出Na、Cl、Ca的电子排布式:
Na:
或者简写为:
Na:
您最近半年使用:0次
4 . 填空。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ ;
(2)基态Ti原子的核外电子排布式为___________ ;
(3)Fe基态核外电子排布式为___________ 。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)基态Ti原子的核外电子排布式为
(3)Fe基态核外电子排布式为
您最近半年使用:0次
5 . 最外层电子排布式为ns2的基态原子对应元素一定位于ⅡA族吗_____ ?
您最近半年使用:0次
6 . 填空
(1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第_____ 周期_____ 族;最高价氧化物的化学式为_____ ,砷酸钠的化学式是_____ 。
(2)已知下列元素在周期表中的位置,写出它们的价电子排布式和元素符号:
①第4周期ⅣB族_____ ;
②第5周期ⅦA族_____ 。
(1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第
(2)已知下列元素在周期表中的位置,写出它们的价电子排布式和元素符号:
①第4周期ⅣB族
②第5周期ⅦA族
您最近半年使用:0次
7 . 某元素M2+的3d轨道上有5个电子,则
(1)M原子的核外电子排布式为_____ 。
(2)M元素在元素周期表中的位置为第_____ 周期。
(1)M原子的核外电子排布式为
(2)M元素在元素周期表中的位置为第
您最近半年使用:0次
解题方法
8 . 请根据1~36号元素原子的电子排布,参照鲍林近似能级图,尝试分析原子中电子排布与元素周期表中周期划分的内在联系。完成表格
| 周期序数 | 对应能级 | 原子轨道数 | 最多容纳电子数 | 价电子排布式 | 元素种数 | |
| ⅠA族 | 0族 | |||||
| 1 | ||||||
| 2 | ||||||
| 3 | ||||||
| 4 | ||||||
| 5 | ||||||
| 6 | ||||||
| 7 | ||||||
您最近半年使用:0次
9 . 某原子的一种激发态为1s22s12p1,则该元素在周期表中的位置为
| A.第2周期ⅡA族 | B.第2周期ⅢA族 |
| C.第1周期ⅠA族 | D.第1周期ⅡA族 |
您最近半年使用:0次
10 . 现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5。有关原子半径大小的顺序正确的是
| A.②①③④ | B.④③①② | C.①②④③ | D.①②③④ |
您最近半年使用:0次



