名校
解题方法
1 . 我国科学家利用过渡金属碳化物(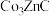 )合成了钴单质催化剂(
)合成了钴单质催化剂(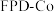 ),其晶胞转化如图所示。
),其晶胞转化如图所示。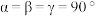 ,底长为
,底长为 、宽为
、宽为 、高为
、高为 ;
;
② 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
下列说法错误的是
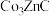 )合成了钴单质催化剂(
)合成了钴单质催化剂( ),其晶胞转化如图所示。
),其晶胞转化如图所示。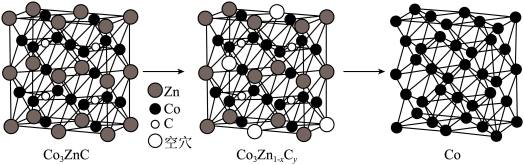
 ,底长为
,底长为 、宽为
、宽为 、高为
、高为 ;
;②
 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。下列说法错误的是
A.同周期基态原子,与 原子中所含单电子数相同的原子有2种 原子中所含单电子数相同的原子有2种 |
B.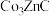 晶胞中与C原子距离最近的 晶胞中与C原子距离最近的 原子形成正八面体结构 原子形成正八面体结构 |
C. 晶胞中 晶胞中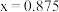 |
D.钴晶胞的密度为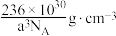 |
您最近半年使用:0次
名校
解题方法
2 . 氮化镓是第三代半导体材料,是坚硬的高熔点材料,常用金属有机物气相沉积法大批量生产。用三甲基镓与氨反应制备氮化镓的原理为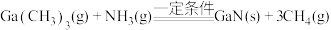 。下列说法错误的是
。下列说法错误的是
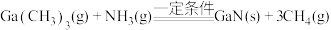 。下列说法错误的是
。下列说法错误的是A. 和 和 的 的 模型相同 模型相同 |
B.基态 原子的电子排布式: 原子的电子排布式: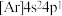 |
C. 中仅含有极性键 中仅含有极性键 |
D. 和N可形成共价晶体 和N可形成共价晶体 |
您最近半年使用:0次
名校
解题方法
3 . 人体血液中的血红蛋白(结构如图)可携带 ,供给生命活动的需要。其中
,供给生命活动的需要。其中 可与周围的6个原子形成配位键。下列说法错误的是
可与周围的6个原子形成配位键。下列说法错误的是
 ,供给生命活动的需要。其中
,供给生命活动的需要。其中 可与周围的6个原子形成配位键。下列说法错误的是
可与周围的6个原子形成配位键。下列说法错误的是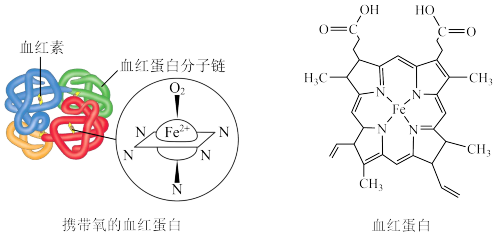
A.一个基态 含有3个未成对电子 含有3个未成对电子 |
| B.血红蛋白分子链间能够形成氢键 |
C.血红蛋白中一个 形成4个配位键 形成4个配位键 |
D. 中毒的本质是其与 中毒的本质是其与 配位,血红蛋白无法携带 配位,血红蛋白无法携带 |
您最近半年使用:0次
名校
解题方法
4 . 化学用语是学习化学的工具。下列说法错误的是
A.H2O的电子式: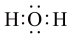 |
B. SiF4的空间填充模型: |
C.基态Fe原子的电子排布式: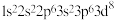 |
D.基态S原子价电子轨道表示式: |
您最近半年使用:0次
5 . 完成下列问题。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________
(2)①基态Cu原子有___________ 种不同能级的电子。位于在周期表___________ 区(填s、p、d或ds)。Cu+的价电子排布式为___________ 。
②N原子中最高能级的电子的电子云轮廓图为___________ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:___________ 。
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用___________ 盛装(填 酸式滴定管 或 碱式滴定管)滴定终点溶液的判断是___________ 颜色变化为由无色变为浅红色。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中
 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用
您最近半年使用:0次
6 . NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.1mol/L的NH4Cl溶液中 浓度小于0.1NA 浓度小于0.1NA |
B.室温下,等体积的pH=1的 溶液和pH=1的 溶液和pH=1的 溶液,所含有的 溶液,所含有的 的个数均为0.1NA 的个数均为0.1NA |
| C.3.2gCH4中所含σ键数目为0.8NA |
| D.1mol基态Al原子位于p能级上的电子数为3NA |
您最近半年使用:0次
7 . 下列化学用语或图示表达正确的是
A.HClO的电子式: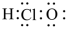 |
B.原子核内中子数为20的氯原子: |
C.基态磷原子的轨道表示式: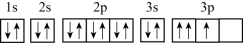 |
| D.基态S原子的核外电子排布式1s²2s²2p⁶3s²3p⁴ |
您最近半年使用:0次
8 . 已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是nsnnp2n;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其最外层电子数等于其能层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:A、___________ ,B、___________ ,C、___________ ,D、___________ ,E、___________ ,F、___________ 。
②B、C、D、E四种元素的第一电离能从大到小的顺序:___________ 。
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________ 。
(3)F元素位于周期表的___________ 区,此区元素的价电子层结构特点是___________ 。
(1)请用元素符号完成下列空白:
①元素:A、
②B、C、D、E四种元素的第一电离能从大到小的顺序:
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是
| 元素 | 电离能/(kJ·mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近半年使用:0次
9 . 回答下列问题。
(1)V2O5是常见催化剂,V的基态原子的价电子排布式为___________ ,其电子占据的原子轨道数为 ___________ ,最高能层符号为 ___________ 。
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为___________ ,该离子更稳定的原因是 ___________ 。
(3)基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是___________  填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是___________ ,属于共价化合物的是___________ 。
(1)V2O5是常见催化剂,V的基态原子的价电子排布式为
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为
(3)基态S原子电子占据最高能级的电子云轮廓图为
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是
 填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是
您最近半年使用:0次
解题方法
10 . 氢镍电池是目前使用最广的含镍电池,废旧电池的处理对环境保护和资源的再利用意义重大。一种对废旧氢镍电池负极材料(含有NiO、Ni和少量La、Fe、Mg、MnO2、石墨粉等)进行湿法处理的流程如图所示:
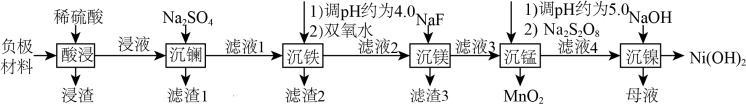
②Ksp(MgF2)=6.4 ;
;
③H2SO4第一步完全电离,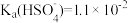 。
。
回答下列问题:
(1)Ni2+的价层电子排布式为_____________ 。
(2)能提高“酸浸”效率的措施有_____________ (任写一种)。
(3)若滤渣1的成分为 ,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因
,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因_________________ 。
(5)“沉镁”后滤液3中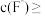
__________  (溶液中离子浓度
(溶液中离子浓度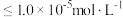 时认为该离子沉淀完全)。
时认为该离子沉淀完全)。
(6) 中存在过氧键(-O-O-),“沉锰”反应的离子方程式为
中存在过氧键(-O-O-),“沉锰”反应的离子方程式为_________________ 。
(7)“沉镍”所用试剂不宜选用氨水的原因为_________________ ,母液中可提取出的循环利用的物质为_____________ (填化学式)。
②Ksp(MgF2)=6.4
 ;
;③H2SO4第一步完全电离,
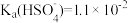 。
。回答下列问题:
(1)Ni2+的价层电子排布式为
(2)能提高“酸浸”效率的措施有
(3)若滤渣1的成分为
 ,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因
,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因 
| A.KSCN溶液 |
| B.K3[Fe(CN)6]溶液 |
| C.NaOH溶液 |
| D.KSCN溶液和氯水 |
(5)“沉镁”后滤液3中
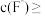
 (溶液中离子浓度
(溶液中离子浓度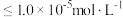 时认为该离子沉淀完全)。
时认为该离子沉淀完全)。(6)
 中存在过氧键(-O-O-),“沉锰”反应的离子方程式为
中存在过氧键(-O-O-),“沉锰”反应的离子方程式为(7)“沉镍”所用试剂不宜选用氨水的原因为
您最近半年使用:0次



