解题方法
1 . 回答下列问题:
(1)1 mol CO2中含有的σ键数目为_______ ,π键数目为_______ 。
(2)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是_______ 。
(3)铜原子的价层电子排布图:_______ ,写出钴的简化电子排布式_______ ,基态Fe2+与Fe3+离子中未成对的电子数之比为_______ 。
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_______ 、_______ (填标号)。
A. B.
B. 
C.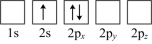 D.
D. 
(5)bte的分子式为C6H8N6,其结构简式如图所示:

①bte分子中碳原子轨道杂化类型为_______ 。
②1 mol bte分子中含σ键的数目为_______ mol。
(6)一个Cu2O晶胞(见图)中,Cu原子的数目为_______ 。

(1)1 mol CO2中含有的σ键数目为
(2)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是
(3)铜原子的价层电子排布图:
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. 
C.
 D.
D. 
(5)bte的分子式为C6H8N6,其结构简式如图所示:

①bte分子中碳原子轨道杂化类型为
②1 mol bte分子中含σ键的数目为
(6)一个Cu2O晶胞(见图)中,Cu原子的数目为

您最近半年使用:0次
2 . 下列化学用语表示正确的是
A.HClO的电子式: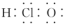 | B.基态Cr原子价层电子轨道表示式: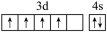 |
C. 的结构示意图: 的结构示意图: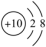 | D.O原子的2s轨道电子云轮廓图: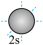 |
您最近半年使用:0次
解题方法
3 . 化学用语是化学专业术语。下列化学用语错误的是
| A.基态V原子的价层电子排布式为3d34s2 |
B.AsH3分子的VSEPR模型: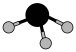 |
C.NH4Br的电子式: |
| D.2-氨基丁酸的结构简式:CH3CH2CH(NH2)COOH |
您最近半年使用:0次
2024-03-09更新
|
226次组卷
|
2卷引用:甘肃省白银市名校2023-2024学年高三下学期联合调研化学试题
名校
解题方法
4 . 传世名画之一的《千里江山图》中青绿山水用“绿青”[主要成分为CuCO3⋅Cu(OH)2]等矿物颜料绘制而成。下列有关说法正确的是
| A.氧元素位于元素周期表的s区 |
B. 中C原子的杂化方式为sp3 中C原子的杂化方式为sp3 |
| C.H、C、O三种元素的电负性由大到小的顺序:O>C>H |
D.“绿青”与盐酸反应的化学方程式为 |
您最近半年使用:0次
2024-03-07更新
|
226次组卷
|
3卷引用:甘肃省白银市名校2023-2024学年高三下学期联合调研化学试题
5 . 已知A、B、C三种元素的原子中,质子数:A<B<C,且都小于18,A元素原子的最外层电子数是次外层电子数的4倍;B元素的原子核外M层电子数是L层电子数的一半;C元素原子的次外层电子数比最外层电子数多3。试回答下列问题:
(1)写出三种元素的名称和符号:A___________ ,B___________ ,C___________ 。
(2)写出三种元素的原子核外电子排布式A___________ ,B___________ ,C___________ 。
(1)写出三种元素的名称和符号:A
(2)写出三种元素的原子核外电子排布式A
您最近半年使用:0次
6 . R、W、X、Y、Z是原子序数依次增大的前四周期元素,其中R与W位于同一周期,且R元素的第一电离能大于氧,W的单质在暗处与 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
(1)基态Z原子的价层电子排布式为__________ ,该元素位于元素周期表中的__________ 区。
(2)基态R原子中有__________ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为__________ 形。
(3)R、W、X三种元素中第一电离能由大到小的顺序为____ (用元素符号表示),原因是________ 。
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是__________ (填化学式)。
(5)X、Y两种元素组成的化合物 的电子式为
的电子式为__________ ,其中含有的化学键类型为__________ 。
 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:(1)基态Z原子的价层电子排布式为
(2)基态R原子中有
(3)R、W、X三种元素中第一电离能由大到小的顺序为
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是
(5)X、Y两种元素组成的化合物
 的电子式为
的电子式为
您最近半年使用:0次
2023-02-15更新
|
169次组卷
|
2卷引用:甘肃省白银市会宁县第四中学2023-2024学年高三上学期第三次月考化学试题
名校
解题方法
7 . 可通过 制备甲烷。下列说法正确的是
制备甲烷。下列说法正确的是
 制备甲烷。下列说法正确的是
制备甲烷。下列说法正确的是A.Al3+的电子式为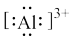 |
| B.H2O为非极性分子 |
| C.一个14C原子中含有7个中子 |
| D.基态氧原子的核外电子排布式为1s22s22p4 |
您最近半年使用:0次
2022-11-07更新
|
211次组卷
|
2卷引用:甘肃省白银市白银区大成学校2022-2023学年高二下学期第一次月考化学试题
名校
解题方法
8 . 我国科学家研发的新型光学材料(Sn7Br10S2)可替代传统光学材料硫镓银(AgGaS2)和磷锗锌(ZnGeP2)。请回答下列问题:
(1)基态硫原子核外电子云轮廓图呈纺锤形的能级上占据的电子总数为_______ 。
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图1所示。

①SF6是_______ (填“极性”或“非极性”)分子。
②1mol SF6分子中含_______ mol σ键。
(3)HF的极性比HBr的强,但是HF是弱酸,HBr是强酸,其主要原因是_______ 。
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是_______ ,碳原子的杂化类型是_______ 。
(5)四卤化锡的熔点如下表所示:
它们熔点递变的主要原因是_______ 。
(6)晶体锗的结构类似金刚石,晶胞如图2所示。已知晶胞参数为x nm,NA表示阿伏加德罗常数的值。

①锗晶体晶胞中a、b间的距离为_______ nm。
②锗晶体的密度为_______ g·cm-3。
(1)基态硫原子核外电子云轮廓图呈纺锤形的能级上占据的电子总数为
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图1所示。

①SF6是
②1mol SF6分子中含
(3)HF的极性比HBr的强,但是HF是弱酸,HBr是强酸,其主要原因是
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是
(5)四卤化锡的熔点如下表所示:
| 物质 | SnF4 | SnCl4 | SnBr4 | SnI4 |
| 熔点/°C | 705 | -33 | 31 | 144.5 |
它们熔点递变的主要原因是
(6)晶体锗的结构类似金刚石,晶胞如图2所示。已知晶胞参数为x nm,NA表示阿伏加德罗常数的值。

①锗晶体晶胞中a、b间的距离为
②锗晶体的密度为
您最近半年使用:0次
2022-04-13更新
|
132次组卷
|
2卷引用:甘肃省白银市靖远县2021-2022学年高三下学期开学考试理综化学试题
解题方法
9 . 总共含有6个能级的能层符号为
| A.M | B.N | C.P | D.Q |
您最近半年使用:0次
名校
10 . 下列Cr的价电子轨道表示式中,处于基态的是
A. |
B. |
C. |
D. |
您最近半年使用:0次
2022-01-22更新
|
546次组卷
|
5卷引用:甘肃省白银市白银区大成学校2022-2023学年高二下学期第一次月考化学试题



