已知A、B、C三种元素的原子中,质子数:A<B<C,且都小于18,A元素原子的最外层电子数是次外层电子数的4倍;B元素的原子核外M层电子数是L层电子数的一半;C元素原子的次外层电子数比最外层电子数多3。试回答下列问题:
(1)写出三种元素的名称和符号:A___________ ,B___________ ,C___________ 。
(2)写出三种元素的原子核外电子排布式A___________ ,B___________ ,C___________ 。
(1)写出三种元素的名称和符号:A
(2)写出三种元素的原子核外电子排布式A
更新时间:2023-03-31 08:19:52
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】根据提供条件推断元素,并按要求填空:
(1)原子核外有3个电子层,其最外层电子数为7,最高价氧化物化学式________ ,最高价氧化物对应水化物化学式______ ,其最高价氧化物对应水化物与NaOH反应的化学方程式为_________ 。
(2)第三周期元素,其最外层电子数与电子层数相同。该元素最高价氧化物的化学式为________ ,最高价氧化物对应水化物与氢氧化钠反应的化学方程式为_______ 。
(3)原子序数依次递增的同周期4种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为____________ 、__________ 、_________ 、______ 。
(4)某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧元素质量分数为60%。则该元素最高价氧化物的化学式为__________ ,该氧化物属________ (填“离子”或“共价”)化合物。
(1)原子核外有3个电子层,其最外层电子数为7,最高价氧化物化学式
(2)第三周期元素,其最外层电子数与电子层数相同。该元素最高价氧化物的化学式为
(3)原子序数依次递增的同周期4种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为
(4)某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧元素质量分数为60%。则该元素最高价氧化物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】W、X、Y、Z是短周期元素,其部分性质如表:
(1)X的简单氢化物的结构式_____ ,Y和W形成的化合物YW2的电子式_____ 。
(2)元素Z在周期表中的位置_____ 。
(3)比较X、Y最高价氧化物对应的水化物的酸性:_____ >_____ (填化学式)。
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的 |
| Z | 第三周期简单离子半径最小 |
(2)元素Z在周期表中的位置
(3)比较X、Y最高价氧化物对应的水化物的酸性:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】A、B、C、D、E、F六种元素均位于元素周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子占据四个原子轨道;D元素原子的成对电子总数是未成对电子总数的3倍;E与D位于同一主族;F位于ds区,且原子的最外层只有1个电子。
(1)基态F原子的核外电子排布式是_____ ,C原子的最高能级的电子云轮廓图是_____ 形。
(2)B、C、D元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是_______ ;B、C元素的这些氢化物的熔、沸点相差较大的主要原因是_______ 。
(4)A、B、D可形成分子式为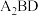 的某化合物,则该化合物分子中B原子的杂化类型是
的某化合物,则该化合物分子中B原子的杂化类型是_______ ;1mol该分子中含有π键的数目是_______ 。
(5)由A、D、E三种元素组成的两种常见化合物的酸性由强到弱的顺序为____ (用化学式表示)。
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是_______ ,若该立方晶胞的棱长为a,阿伏加德罗常数用NA表示,该晶体的密度表示为_______ ,

(1)基态F原子的核外电子排布式是
(2)B、C、D元素的第一电离能由大到小的顺序是
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是
(4)A、B、D可形成分子式为
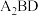 的某化合物,则该化合物分子中B原子的杂化类型是
的某化合物,则该化合物分子中B原子的杂化类型是(5)由A、D、E三种元素组成的两种常见化合物的酸性由强到弱的顺序为
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】已知元素X、Y、Z质子数都小于18,并且质子数X+Y=Z,X原子的电子层数与它的核外电子总数相同,Z原子有两个电子层,外层电子数是内层的电子数的三倍,则
(1)X是________ ,Z是________ ;Y原子结构示意图_______ 。
(2)由Y和Z组成,且Y和Z的质量比为7:20的化合物的分子式是________ 。
(3)X、Z可以形成两种化合物A和B,A中原子个数比为2:1,则A的摩尔质量是________ 。B中两原子个数比为1:1,实验室常用B制备少量的氧气,写出该反应的化学反应方程式________ 。
(1)X是
(2)由Y和Z组成,且Y和Z的质量比为7:20的化合物的分子式是
(3)X、Z可以形成两种化合物A和B,A中原子个数比为2:1,则A的摩尔质量是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D四种元素核电荷数均小于18。A元素原子核内无中子,B元素的原子L层电子数是K层电子数的3倍,C元素原子的M层电子数比K层电子数多1个,D2-离子比C3+离子多一个电子层。请回答:
(1)写出元素名称:A___ 、B___ 、C___ 、D___ 。
(2)画处C3+离子结构示意图_____ 。
(3)画出D2-离子的电子式_____ 。
(4)写出B、C形成的化合物的化学式____ 。
(1)写出元素名称:A
(2)画处C3+离子结构示意图
(3)画出D2-离子的电子式
(4)写出B、C形成的化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】通常情况下,微粒 A、B 为分子,C、E 为阳离子,D为阴离子,它们都含有10个电子;B 溶于 A 后所得的物质可电离出 C、D;A、B、E 三种微粒反应后可得 C 和一种白色沉淀。请回答:
(1)用化学符号表示下列 4 种微粒:A.__ 、B. __ 、C. __ 、D. __ 。
(2)写出A、B、E 三种微粒反应的离子方程式:__
(3)某元素原子的最外层电子数为次外层电子层数的 3 倍。该元素原子的简单离子的结构示意图为_______ 。该元素在化学反应容易_______ 电子,具有_______ 性。
(1)用化学符号表示下列 4 种微粒:A.
(2)写出A、B、E 三种微粒反应的离子方程式:
(3)某元素原子的最外层电子数为次外层电子层数的 3 倍。该元素原子的简单离子的结构示意图为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】C、Si、Ge、Sn都是IVA族元素,该族元素单质及其化合物在材料、医药等方面有重要应用.请回答下列问题:
(1)Ge的原子核外电子排布式为_______ 。
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是_______ 。
(3)CO2分子的空间构型及碳氧之间的成键方式_______ 。
(4)1molSiO2晶体中的硅氧键数目为_______ 。
(5)CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为_______ 。
(6)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm- 1,CO分子中碳氧键的伸缩振动频率为2143cm - 1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度_______ (填字母)。
(A)强 (B)弱 (C)相等 (D)无法判断。
(1)Ge的原子核外电子排布式为
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是
(3)CO2分子的空间构型及碳氧之间的成键方式
(4)1molSiO2晶体中的硅氧键数目为
(5)CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为
(6)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm- 1,CO分子中碳氧键的伸缩振动频率为2143cm - 1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度
(A)强 (B)弱 (C)相等 (D)无法判断。
您最近一年使用:0次
【推荐2】下表为元素周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中属于d区的元素是________ (填编号),其原子结构示意图是 ________________ 。
(2)写出元素⑩的基态原子的简化电子排布式:________________________________ 。
(3)某元素的特征电子排布式为 ,该元素是
,该元素是 ________ (填名称),原子的最外层电子的成对电子为 ________ 对。
(4)③和④的简单气态氢化物最稳定的是________ (填化学式,下同),⑦的最强含氧酸为 ________ 。
(5)⑦和③形成的化合物的电子式是________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | |||||||||||||||
| ⑧ | ⑨ | ⑩ |
(1)表中属于d区的元素是
(2)写出元素⑩的基态原子的简化电子排布式:
(3)某元素的特征电子排布式为
 ,该元素是
,该元素是 (4)③和④的简单气态氢化物最稳定的是
(5)⑦和③形成的化合物的电子式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】原子序数依次增大的A、B、C、D、E、F六种元素均为前四周期元素,A是形成化合物种类最多的元素,B与A同周期,其原子核外s能级上的电子总数与p能级上的电子总数相等,C为第3周期元素,其离子半径在该周期中最小,D原子核外p能级上的电子总数比s能级上的电子总数多2,E元素位于元素周期表中的第8列,F的单质为紫红色金属。回答下列问题:
(1)D在元素周期表中的位置为___________ 。
(2)A元素的原子核外共有___________ 种不同运动状态的电子;B元素基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)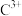 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为___________ 。
(4)E元素位于元素周期表中___________ 区(按电子排布分区),其基态原子价电子轨道表示式为___________ 。
(5)基态F原子的核外电子排布式为___________ ,其基态原子核外填充有电子的能量最高的电子层的符号为___________ ,该电子层上具有的原子轨道数是___________ 。
(1)D在元素周期表中的位置为
(2)A元素的原子核外共有
(3)
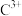 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为(4)E元素位于元素周期表中
(5)基态F原子的核外电子排布式为
您最近一年使用:0次



