名校
1 . Cu2S可用于钾离子电池的负极材料.冶炼铜时可使Cu2S在高温下与O2反应转化为Cu2O,生成的Cu2O与Cu2S进一步反应得到Cu。Cu2O在酸性溶液中会转化为Cu和Cu2+;Cu2S能被浓硝酸氧化为Cu(NO3)2.Cu在O2存在下能与氨水反应生成[Cu(NH3)4]2+;Cu(OH)2能与NaOH反应生成Na2[Cu(OH)4]。O3、O2的沸点分别为-111℃、-182℃。下列说法正确的是
| A.SO2的键角比SO3的大 | B.SO2是非极性分子 |
| C.1mol[Cu(NH3)4]2+含有16mol的σ键 | D.O2分子间作用力比O3的大 |
您最近半年使用:0次
名校
2 . 下列关于 及构成微粒的化学用语或图示表达错误的是
及构成微粒的化学用语或图示表达错误的是
 及构成微粒的化学用语或图示表达错误的是
及构成微粒的化学用语或图示表达错误的是A. 的分子结构模型: 的分子结构模型: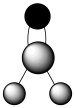 |
B.H原子电子的电子云轮廓图: |
C.C原子杂化轨道示意图: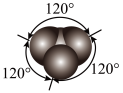 |
D.基态氧原子的轨道表示式为: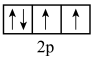 |
您最近半年使用:0次
名校
3 . 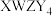 是构成电池的一种重要化合物,其阴离子结构如图所示,X、Y、Z、W为原子序数依次增大的前四周期元素,其中Y、Z为非金属元素且位于相邻主族,四种基态原子未成对电子数均不相等且不为0,未成对电子数存在关系:
是构成电池的一种重要化合物,其阴离子结构如图所示,X、Y、Z、W为原子序数依次增大的前四周期元素,其中Y、Z为非金属元素且位于相邻主族,四种基态原子未成对电子数均不相等且不为0,未成对电子数存在关系: 。下列说法错误的是
。下列说法错误的是
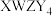 是构成电池的一种重要化合物,其阴离子结构如图所示,X、Y、Z、W为原子序数依次增大的前四周期元素,其中Y、Z为非金属元素且位于相邻主族,四种基态原子未成对电子数均不相等且不为0,未成对电子数存在关系:
是构成电池的一种重要化合物,其阴离子结构如图所示,X、Y、Z、W为原子序数依次增大的前四周期元素,其中Y、Z为非金属元素且位于相邻主族,四种基态原子未成对电子数均不相等且不为0,未成对电子数存在关系: 。下列说法错误的是
。下列说法错误的是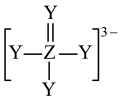
| A.电负性:Y>Z>X | B.W能与Y的简单氢化物反应生成 |
C.该化合物中Z采用 杂化 杂化 | D.Y元素形成的单质一定为非极性分子 |
您最近半年使用:0次
4 . 一种具有聚集诱导发光性能的分子结构如图所示。下列说法错误的是
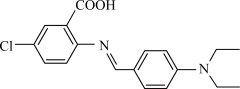
| A.分子中C原子有sp2、sp3两种杂化方式 |
| B.分子中没有手性碳原子 |
| C.1mol该物质最多可与7molH2发生加成反应 |
| D.苯环上的C-Cl键可通过苯环与氯气在光照条件下生成 |
您最近半年使用:0次
名校
解题方法
5 .  、
、 是新型磁性材料的成分,设
是新型磁性材料的成分,设 为阿伏加德罗常数的值,依据其中有关元素回答问题:
为阿伏加德罗常数的值,依据其中有关元素回答问题:
(1)钕(Nd)属于镧系元素,则其在元素周期表中处于___________ 区, 的价电子排布图为
的价电子排布图为___________ 。
(2) 的立体构型为
的立体构型为___________ ;F原子核外有___________ 种不同空间运动状态的电子。
(3) 是一种还原剂,B原子的杂化方式为
是一种还原剂,B原子的杂化方式为___________ 。该物质中是否存在配位键___________ (填“是”或“否”)。
(4) 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。___________ 。
②该晶体密度为 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为___________ pm。
(5) 的制备:称取研细的
的制备:称取研细的 和
和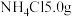 于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的
于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该反应的离子方程式
溶液。写出该反应的离子方程式___________ 。若上述实验过程中得到 ,则其中所含的
,则其中所含的 键数目为
键数目为___________ 。
(6)已知某温度下 的电离平衡常数:
的电离平衡常数: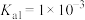 、
、 ,
,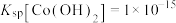 、
、 。写出该温度时向
。写出该温度时向 碳酸钠溶液中逐滴加入
碳酸钠溶液中逐滴加入 溶液,生成沉淀的离子方程式:
溶液,生成沉淀的离子方程式:___________ 。
 、
、 是新型磁性材料的成分,设
是新型磁性材料的成分,设 为阿伏加德罗常数的值,依据其中有关元素回答问题:
为阿伏加德罗常数的值,依据其中有关元素回答问题:(1)钕(Nd)属于镧系元素,则其在元素周期表中处于
 的价电子排布图为
的价电子排布图为(2)
 的立体构型为
的立体构型为(3)
 是一种还原剂,B原子的杂化方式为
是一种还原剂,B原子的杂化方式为(4)
 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。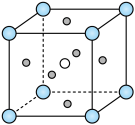
②该晶体密度为
 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为(5)
 的制备:称取研细的
的制备:称取研细的 和
和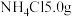 于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的
于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该反应的离子方程式
溶液。写出该反应的离子方程式 ,则其中所含的
,则其中所含的 键数目为
键数目为(6)已知某温度下
 的电离平衡常数:
的电离平衡常数: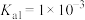 、
、 ,
,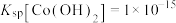 、
、 。写出该温度时向
。写出该温度时向 碳酸钠溶液中逐滴加入
碳酸钠溶液中逐滴加入 溶液,生成沉淀的离子方程式:
溶液,生成沉淀的离子方程式:
您最近半年使用:0次
名校
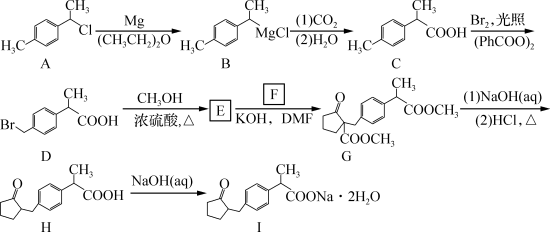
6 . 化合物I是一种非甾体类抗炎药,其合成路线如下:___________ (填“大”“小”或“无差别”)。
(2)B与CO2的反应过程中,CO2分子中碳原子杂化类型的变化为___________ 。
(3)F的分子式为C7H10O3,其结构简式为___________ 。
(4)C的一种同分异构体同时满足下列条件,其结构简式为___________ 。
①在碱性条件水解,酸化得2种产物;
②一种产物为芳香族化合物且能与NaHCO3溶液反应,且有4种不同化学环境的氢原子;
③另一种产物在铜催化条件下与氧气反应,所得有机产物不能发生银镜反应。
(5)已知:
(2)B与CO2的反应过程中,CO2分子中碳原子杂化类型的变化为
(3)F的分子式为C7H10O3,其结构简式为
(4)C的一种同分异构体同时满足下列条件,其结构简式为
①在碱性条件水解,酸化得2种产物;
②一种产物为芳香族化合物且能与NaHCO3溶液反应,且有4种不同化学环境的氢原子;
③另一种产物在铜催化条件下与氧气反应,所得有机产物不能发生银镜反应。
(5)已知:
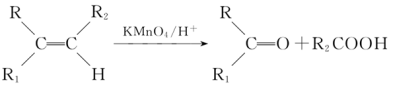 ①(R、R1、R2、R3、R4指烃基,下同)
①(R、R1、R2、R3、R4指烃基,下同)
② R1COOR2 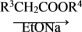
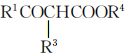
写出以 、CH3OH、CH3Cl为原料制备
、CH3OH、CH3Cl为原料制备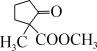 的合成路线流程图
的合成路线流程图
您最近半年使用:0次
名校
解题方法
7 . 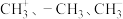 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是
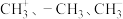 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是A.它们的碳原子均采取 杂化,其中 杂化,其中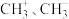 的结构示意图分别为: 的结构示意图分别为: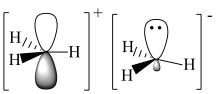 |
B. 与 与 形成的化合物中含有离子键 形成的化合物中含有离子键 |
C. 的键角和比 的键角和比 的键角小 的键角小 |
D. 与 与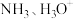 互为等电子体,VSEPR立体构型均为四面体形 互为等电子体,VSEPR立体构型均为四面体形 |
您最近半年使用:0次
名校
解题方法
8 . 第29届亚运会开幕式首次使用废碳(指 )再生的绿色甲醇(
)再生的绿色甲醇( )作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是
)作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是
 )再生的绿色甲醇(
)再生的绿色甲醇( )作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是
)作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是A. 为含极性键的非极性分子 为含极性键的非极性分子 |
B.甲醇分子中C为 杂化,O为 杂化,O为 杂化 杂化 |
C.“实现循环内的零排放”是指甲醇燃烧生成 , , 再转化为甲醇 再转化为甲醇 |
| D.甲醇与乙烷相对分子质量接近,但沸点(65℃)远高于乙烷(-89℃),是因为甲醇存在分子氢键 |
您最近半年使用:0次
名校
9 . 下列说法正确的是
| A.等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗氧气的量依次增加 |
B. 分子用系统命名法名称为:丁烯 分子用系统命名法名称为:丁烯 |
C.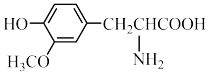 与 与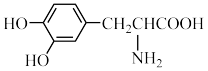 互为同系物 互为同系物 |
D.薄荷醇(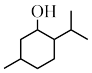 )分子中 )分子中 杂化的原子数为11个 杂化的原子数为11个 |
您最近半年使用:0次
10 . 我国科研工作者成功合成了一种含铜(II)高效催化剂,该催化剂的部分结构如下图所示,该部分结构中的所有原子共平面。下列说法正确的是
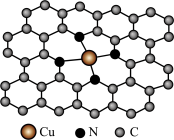
| A.铜元素位于周期表的d区 |
| B.该催化剂中铜的配位数为3 |
| C.该部分结构中C、N原子的杂化类型相同 |
| D.基态N原子核外有7种不同空间运动状态的电子 |
您最近半年使用:0次



