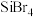1 . 、臭氧 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。
(1)基态铁原子有___________ 种空间运动状态不同的电子; 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ ; 的空间构型为
的空间构型为___________ (用文字描述); 为
为___________ 分子(填“极性”、“非极性”)。
(2)碘的四氯化碳溶液为紫红色,加入浓碘化钾水溶液,振荡后溶液紫色变浅,请用离子方程式说明原因___________ 。
(3)硫单质的常见形式为 ,其环状结构如图所示,
,其环状结构如图所示, 中含有
中含有___________ 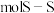 键。
键。 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的192℃,由此可以判断铝氟之间的化学键为
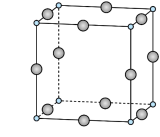
的192℃,由此可以判断铝氟之间的化学键为___________ 键。 结构属立方晶系,晶胞如图所示,
结构属立方晶系,晶胞如图所示, 的配位数为。若晶胞参数为
的配位数为。若晶胞参数为 ,晶体密度
,晶体密度
___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。(1)基态铁原子有
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为 为
为(2)碘的四氯化碳溶液为紫红色,加入浓碘化钾水溶液,振荡后溶液紫色变浅,请用离子方程式说明原因
(3)硫单质的常见形式为
 ,其环状结构如图所示,
,其环状结构如图所示, 中含有
中含有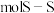 键。
键。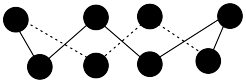
 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的192℃,由此可以判断铝氟之间的化学键为
的192℃,由此可以判断铝氟之间的化学键为 结构属立方晶系,晶胞如图所示,
结构属立方晶系,晶胞如图所示, 的配位数为。若晶胞参数为
的配位数为。若晶胞参数为 ,晶体密度
,晶体密度
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近半年使用:0次
名校
2 . 二氯化二硫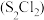 是广泛用于橡胶工业的硫化剂,广泛用于石油化工,其分子结构如下图所示。制备方法:在120℃向硫磺粉(用
是广泛用于橡胶工业的硫化剂,广泛用于石油化工,其分子结构如下图所示。制备方法:在120℃向硫磺粉(用 浸润)中通入
浸润)中通入 。下列说法错误的是
。下列说法错误的是
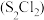 是广泛用于橡胶工业的硫化剂,广泛用于石油化工,其分子结构如下图所示。制备方法:在120℃向硫磺粉(用
是广泛用于橡胶工业的硫化剂,广泛用于石油化工,其分子结构如下图所示。制备方法:在120℃向硫磺粉(用 浸润)中通入
浸润)中通入 。下列说法错误的是
。下列说法错误的是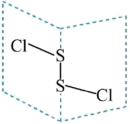
A. 分子中所有原子均满足8电子结构 分子中所有原子均满足8电子结构 |
B.用 浸润可加快反应速率,体现相似相溶原理 浸润可加快反应速率,体现相似相溶原理 |
C. 中S原子的杂化类型为 中S原子的杂化类型为 杂化 杂化 |
D. 晶体类似干冰晶体,则每个 晶体类似干冰晶体,则每个 周围等距且紧邻的 周围等距且紧邻的 有12个 有12个 |
您最近半年使用:0次
名校
解题方法
3 .  是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是
 是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是A.该化合物中 的中心原子的杂化轨道类型为 的中心原子的杂化轨道类型为 |
| B.该化合物中存在的化学键有离子键,共价键,配位键和氢键 |
C. 极易溶于 极易溶于 形成氨水,氨水中最多可形成4种氢键 形成氨水,氨水中最多可形成4种氢键 |
D.根据VSEPR模型预测的 的空间结构是正四面体形 的空间结构是正四面体形 |
您最近半年使用:0次
名校
4 . 抗癌药阿霉素与环糊精在水溶液中形成超分子包合物,结构如下图,增大了阿霉素的水溶性,控制了阿霉素的释放速度,从而提高药效。下列说法错误的是
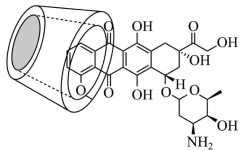
A.阿霉素分子中碳原子的杂化方式为 、 、 |
| B.可以通过晶体的X射线衍射实验获得阿霉素分子的键长和键角 |
C.该超分子包合物中既有 键,又有 键,又有 键 键 |
| D.阿霉素分子中不含手性碳原子 |
您最近半年使用:0次
名校
5 . 反应 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是
 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是A. 的电子式为 的电子式为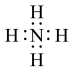 | B. 中N原子采用 中N原子采用 杂化 杂化 |
C. 晶体属于离子晶体 晶体属于离子晶体 | D. 为含极性键的非极性分子 为含极性键的非极性分子 |
您最近半年使用:0次
名校
解题方法
6 . 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. 平面三角形 平面三角形  杂化 杂化 | B. 平面三角形 平面三角形  杂化 杂化 |
C. V形 V形  杂化 杂化 | D. 三角锥形 三角锥形  杂化 杂化 |
您最近半年使用:0次
2024-04-21更新
|
218次组卷
|
7卷引用:四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题
四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题天津市静海区四校2022-2023学年高二下学期3月阶段性检测化学试题(已下线)期中模拟预测卷02(测试范围:选择性必修2+选择性必修3第1章)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)天津市第三中学2022-2023学年高二下学期期中质量检测化学试题陕西省渭南市华州区咸林中学2023-2024学年高二下学期第一次月考化学试题浙江省舟山中学2023-2024学年高二下学期4月月考化学试题福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题
7 . [Zn(CN)4]2-在水溶液中可与HCHO发生反应生成[Zn(H2O)4]2+和HOCH2CN,下列说法错误的是
| A.Zn2+基态核外电子排布式为[Ar]3d10 |
| B.1molHCHO分子中含有σ键的数目为3mol |
| C.HOCH2CN分子中碳原子轨道的杂化类型是sp3 |
D.[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,可表示为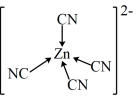 |
您最近半年使用:0次
名校
8 . NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_____ 。
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是_____ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是_____ 。
②NaHCO3分解得Na2CO3., 空间结构为
空间结构为_____ 。
(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
①NH3的中心原子的杂化轨道类型为_____ 。
②比较熔点:NH3BH3_____ CH3CH3(填“>”或“<”)。
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为_____ 。
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是_____ 。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是
②NaHCO3分解得Na2CO3.,
 空间结构为
空间结构为(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
| 元素 | H | B | N | F |
| 电负性 | 2.1 | 2.0 | 3.0 | 4.0 |
②比较熔点:NH3BH3
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是
您最近半年使用:0次
2024-03-03更新
|
267次组卷
|
2卷引用:北京市第十九中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
9 . 下列分子中的中心原子杂化轨道的类型相同的是
| A.CO2与SO2 | B.C2H4与C2H2 | C.BeCl2与BF3 | D.H2O与H3O+ |
您最近半年使用:0次
2024-03-03更新
|
564次组卷
|
4卷引用:北京市第十九中学2021-2022学年高二下学期期中考试化学试题
10 . 硅和卤素单质反应可以得到 。
。
 的熔沸点
的熔沸点
(1)①沸点依次升高的原因是______ ,②气态 分子的空间构型是
分子的空间构型是______ ;
(2) 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图甲所示。
的空间结构和相应的键角如图甲所示。 中P的杂化类型是
中P的杂化类型是______ 。
② 的沸点比
的沸点比 的
的______ (高或者低),原因是______ 。
(3)① 的空间构型为
的空间构型为______ (用文字描述);抗坏血酸的分子结构如图乙所示,分子中碳原子的轨道杂化类型为②______ ;③推测抗坏血酸在水中的溶解性______ (填“难溶于水”或“易溶于水”)。
 。
。 的熔沸点
的熔沸点
|
|
|
| |
熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(1)①沸点依次升高的原因是
 分子的空间构型是
分子的空间构型是(2)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图甲所示。
的空间结构和相应的键角如图甲所示。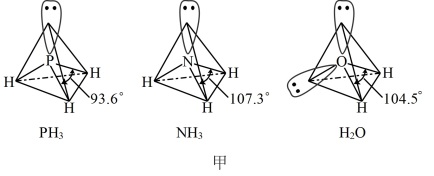
 中P的杂化类型是
中P的杂化类型是②
 的沸点比
的沸点比 的
的(3)①
 的空间构型为
的空间构型为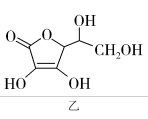
您最近半年使用:0次