名校
解题方法
1 . 观察下列模型并结合信息,判断有关说法错误的是
| 晶体硼的结构单元 (有12个  原子) 原子) |  分子 分子 |  分子 分子 |  | |
| 结构模型 示意图 | 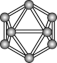 |  | 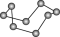 |  |
| A.固态硫S8中S原子为sp2杂化 |
| B.SF6中心原子的价层电子对数为6,其中S-F键的键长、键能均相等 |
| C.晶体硼的结构单元中含有30个B-B键,含20个正三角形 |
| D.HCN的结构式为H-C≡N |
您最近一年使用:0次
名校
解题方法
2 . 钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互熔,其固熔体为面心立方晶格。
(1)Co元素在周期表中属于_____ 区,其原子的简化电子排布式为________ 。
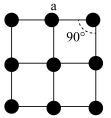
(2)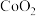 晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述
晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述 化学组成的是________(填序号)。
化学组成的是________(填序号)。
(3)二氯二吡啶合铂分子是一种铂配合物,有顺式和反式两种同分异构体(如图)。科学研究表明,顺式分子具有抗癌活性。
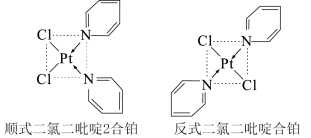
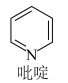
①顺式二氯二吡啶合铂分子中含有的化学键类型为___ (填字母)。
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
②反式二氯二吡啶合铂分子是___ 分子(填“极性”或“非极性”)。
③常用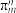 表示分子中的大
表示分子中的大 键,其中m代表参与形成大
键,其中m代表参与形成大 键的原子总数,n代表参与形成大
键的原子总数,n代表参与形成大 键的电子总数,如苯分子中存在
键的电子总数,如苯分子中存在 大
大 键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为
键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为___ ,吡啶分子中的大 键可表示为
键可表示为___ 。
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y、z轴的投影图均为如下图所示,则铂原子采取的堆积方式为___ 。该堆积方式中的空间利用率为_______ 。若金属铂的密度为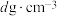 ,则晶胞参数
,则晶胞参数
______ nm(列出计算表达式)。
(1)Co元素在周期表中属于
(2)
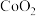 晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述
晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述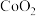 化学组成的是________(填序号)。
化学组成的是________(填序号)。A. | B.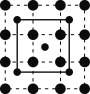 | C. | D. |
(3)二氯二吡啶合铂分子是一种铂配合物,有顺式和反式两种同分异构体(如图)。科学研究表明,顺式分子具有抗癌活性。


①顺式二氯二吡啶合铂分子中含有的化学键类型为
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
②反式二氯二吡啶合铂分子是
③常用
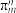 表示分子中的大
表示分子中的大 键,其中m代表参与形成大
键,其中m代表参与形成大 键的原子总数,n代表参与形成大
键的原子总数,n代表参与形成大 键的电子总数,如苯分子中存在
键的电子总数,如苯分子中存在 大
大 键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为
键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为 键可表示为
键可表示为(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y、z轴的投影图均为如下图所示,则铂原子采取的堆积方式为
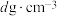 ,则晶胞参数
,则晶胞参数

您最近一年使用:0次
名校
解题方法
3 . 钛是20世纪50年代发展起来的一种重要的结构金属,被广泛用于各个领域。回答下列问题:
(1)基态Ti原子的价层电子排布图为___________ 。
(2)Ti的配合物有多种,如Ti(CO)6,[Ti(H2O)5Cl]3+ 等。
①Ti(CO)6和[Ti(H2O)5Cl]3+中配体所含元素的电负性由小到大的顺序是___________ (写元素符号),其中1molTi(CO)6含有σ键的数目为 ___________ 。
②[Ti(H2O)5Cl]3+的配位数为___________ ,配体H2O中键角∠HOH ___________ (填“大于”、“小于”或“等于”)单个H2O分子中键角∠HOH,原因是 ___________ 。
(3)TiO2作光催化剂能将室内空气污染物甲醛、苯等有害物质转化为CO2和H2O。甲醛分子中心原子的杂化方式为___________ ,甲醛极易溶于水的原因是 ___________ 。
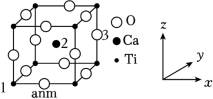
(4)某钛的化合物立方晶胞如图所示:
①与Ti4+最邻近且等距离的O2﹣构成的几何图形为___________ 。
②若设晶胞边长为anm,阿伏加德罗常数的值为NA,则该晶体密度为___________ g•cm﹣3.
③原子分数坐标可用于表示晶胞内部各原子的相对位置。其中,原子分数坐标1为(0,0,0),坐标2为 ( ,
, ,
, ),则坐标3的原子分数坐标为
),则坐标3的原子分数坐标为 ___________ 。
(1)基态Ti原子的价层电子排布图为
(2)Ti的配合物有多种,如Ti(CO)6,[Ti(H2O)5Cl]3+ 等。
①Ti(CO)6和[Ti(H2O)5Cl]3+中配体所含元素的电负性由小到大的顺序是
②[Ti(H2O)5Cl]3+的配位数为
(3)TiO2作光催化剂能将室内空气污染物甲醛、苯等有害物质转化为CO2和H2O。甲醛分子中心原子的杂化方式为
(4)某钛的化合物立方晶胞如图所示:
①与Ti4+最邻近且等距离的O2﹣构成的几何图形为
②若设晶胞边长为anm,阿伏加德罗常数的值为NA,则该晶体密度为
③原子分数坐标可用于表示晶胞内部各原子的相对位置。其中,原子分数坐标1为(0,0,0),坐标2为 (
 ,
, ,
, ),则坐标3的原子分数坐标为
),则坐标3的原子分数坐标为 
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]和Fe(CO)x等。
①基态氧原子的价电子排布式为___________ 。
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是___________ 、___________ 。
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_____ 。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于________ (填晶体类型)。
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为___________ 。已知该晶胞的密度为 g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
g/cm3,阿伏加德罗常数为NA,求晶胞边长a=___________ cm。(用含p、NA的计算式表示)___________ 。
a.第一电离能大小:S>P>Si
b.电负性顺序:C<N<O<F
c.因为晶格能CaO比KC1高,所以KCl比CaO熔点低
d.SO2与CO2的化学性质类似,分子结构也都呈直线形,相同条件下SO2的溶解度更大
(1)金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]和Fe(CO)x等。
①基态氧原子的价电子排布式为
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为
 g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
a.第一电离能大小:S>P>Si
b.电负性顺序:C<N<O<F
c.因为晶格能CaO比KC1高,所以KCl比CaO熔点低
d.SO2与CO2的化学性质类似,分子结构也都呈直线形,相同条件下SO2的溶解度更大
您最近一年使用:0次
名校
解题方法
5 . 下列离子的VSEPR模型与离子的空间立体构型一致的是
A. | B. | C. | D. |
您最近一年使用:0次
2023-12-21更新
|
572次组卷
|
42卷引用:黑龙江省绥化市第九中学2021-2022学年高二4月月考化学试题
黑龙江省绥化市第九中学2021-2022学年高二4月月考化学试题浙江省湖州市三贤联盟2021-2022学年高二下学期期中联考化学试题重庆市九龙坡区2021~2022学年高二下学期期末统考化学试题安徽省滁州市九校2021-2022学年高二下学期3月月考化学试题云南省玉溪市江川区第一中学2021-2022学年高二下学期3月月考化学试题第二节 分子的空间结构 第1课时 分子结构的测定 多样的分子空间结构 价层电子对互斥模型云南省富宁县第一中学校2021-2022学年高二下学期开学考试化学题宁夏贺兰县景博中学2021-2022学年高二下学期第一次月考化学试题黑龙江省绥化市第二中学2022-2023年高三上学期第一次月考化学试题四川省乐山市峨眉第二中学2022-2023学年高二上学期期中考试化学试题(已下线)【知识图鉴】单元讲练测选择性必修2第二章02练基础 湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题宁夏育才中学勤行校区2016-2017学年高二下学期第一次(3月)月考化学试题黑龙江省大庆市第四中学2018-2019学年高二下学期期中考试化学试题【全国百强校】天津市静海区第一中学2018-2019学年高二下学期5月月考化学试题广西壮族自治区崇左市天等县高级中学2019-2020学年高二下学期期中考试理科综合化学试题宁夏海原县第一中学2019-2020学年高二下学期期末考试化学试题(已下线)第二单元 化学键与分子间作用力(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)山西省太原市2020-2021学年高二下学期期中质量监测理科化学试题福建省莆田第十五中学2019-2020学年高二下学期期末考试化学试题人教2019选择性必修2第二章第二节 分子的空间结构课后习题天津市红桥区2020-2021学年高三上学期期末考试化学试题重庆市第一中学2022-2023学年高二上学期期末考试化学试题湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题北京市顺义区第一中学2022-2023学年高二下学期3月月考化学试题广东省韶关市新丰县第一中学2022-2023学年高二3月月考化学试题广东省肇庆市封开县广信中学等几校2022-2023学年高二下学期期中联考化学试题天津市第四十七中学2022-2023学年高二下学期期中考试化学试题四川省自贡市2022-2023学年高二下学期期末考试化学试题浙江省绍兴市柯桥区2022-2023学年高一下学期期末教学质量检测化学(实验班)试题(已下线)第4讲 空间构型北京师范大学第二附属中学2023-2024学年高二上学期12月月考化学试题 江西省宜春市宜丰中学2023-2024学年高二上学期12月月考化学试题(已下线)第04讲 分子的空间结构-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)辽宁省葫芦岛市普通高中2023-2024学年高二上学期学业质量监测考试化学试题江西省宜春市上高中学2023-2024学年高二上学期第二次月考化学试卷 (已下线)热点04 分子的空间结构(已下线)广东省深圳中学2023-2024学年高二上学期期末考试化学试题(已下线)广东省深圳市深圳中学2023-2024学年高二上学期期末考试化学试题浙江省台州市三门启超中学2023-2024学年高二上学期期中考试化学试题 四川省达州市高级中学校2023-2024学年高二下学期3月月考化学试题广东省潮州市饶平县第二中学2023-2024学年高二下学期第一次月考化学试题
6 . 研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

| A.雾和霾的分散剂相同 |
B.雾霾中含有硝酸铵和硫酸铵,其中 和 和 的的空间结构为正四面体 的的空间结构为正四面体 |
| C.NH3是形成无机颗粒物的催化剂,属于极性分子 |
| D.燃煤中加入CaO可以减少SO2气体的排放 |
您最近一年使用:0次
名校
7 . 我国科学家提出的聚集诱导发光机制已成为研究热点之一。一种具有聚集诱导发光性能的物质,其分子结构如图所示。下列说法不正确的是
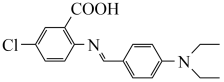

| A.分子中N原子有sp2、sp3两种杂化方式 |
| B.1mol该有机物最多可以消耗2molNaOH |
| C.该物质既有酸性又有碱性 |
| D.该物质可发生取代反应、加成反应 |
您最近一年使用:0次
2023-12-15更新
|
177次组卷
|
2卷引用:云南省腾冲市2022-2023学年高三上学期期中教育教学质量监测理科综合试卷
名校
解题方法
8 . 某温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:Na2GeO3;二锗酸钠:Na2Ge2O5等),也能形成类似于烷烃的锗烷(GenH2n+2)。
①Na2GeO3中锗原子的杂化方式是_____ 。
②推测1molGenH2n+2中含有的σ键的数目是_____ (用NA表示阿伏加德罗常数值)。
(2)利用离子液体[EMIM][AlCl4]可电沉积还原金属Ge,其熔点只有7℃,其中EMIM+结构如图所示。

①该物质的晶体类型是_____ 。
②EMIM+离子中组成元素的电负性由小到大的顺序是_____ 。
(3)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是_____ ;已知晶胞边长为apm,乙图为甲图的俯视图,A点坐标为(0,0,0),B点坐标为 ,则D点坐标为
,则D点坐标为_____ ;若该晶胞密度为ρg·cm-3,则阿伏加德罗常数NA为_____ (列出计算式)。

(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:Na2GeO3;二锗酸钠:Na2Ge2O5等),也能形成类似于烷烃的锗烷(GenH2n+2)。
①Na2GeO3中锗原子的杂化方式是
②推测1molGenH2n+2中含有的σ键的数目是
(2)利用离子液体[EMIM][AlCl4]可电沉积还原金属Ge,其熔点只有7℃,其中EMIM+结构如图所示。

①该物质的晶体类型是
②EMIM+离子中组成元素的电负性由小到大的顺序是
(3)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
 ,则D点坐标为
,则D点坐标为
您最近一年使用:0次
2023-10-06更新
|
69次组卷
|
2卷引用:江西省宜春市宜丰中学2022-2023学年高二上学期11月期中(第二次月考)化学试题
名校
解题方法
9 . 翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一。
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为___________ 。
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是___________ ,最小的是___________ (填标号)。
A. B.
B.  C.
C.  D.
D. 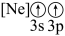
(3)配合物K[Cr(C2O4)(H2O)]中的配体是___________ ,H2O的沸点比CO2的高了许多,主要原因是___________ 。
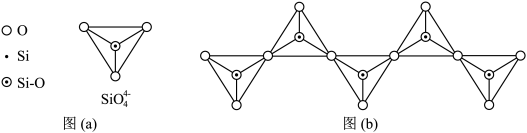
(4)在翡翠等硅酸盐中, 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为___________ ,其化学式为___________ 。低温石英中也存在有顶角相连的硅氧四面体形成螺旋上升的长链,没有封闭的环状结构,这一结构决定了它具有___________ 。
(5)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是___________ 原子。设Cr和Al原子半径分别为rCr和rAl,则金属原子空间占有率为___________ % (列出计算表达式)。

(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是
A.
 B.
B.  C.
C.  D.
D. 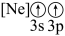
(3)配合物K[Cr(C2O4)(H2O)]中的配体是
(4)在翡翠等硅酸盐中,
 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
(5)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是

您最近一年使用:0次
名校
10 . 石墨烯是一种由碳原子组成六角形呈蜂巢晶格的二维碳纳米材料(如图甲),石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图乙)。

下列说法错误的是

下列说法错误的是
| A.图甲中,1号C与相邻C形成平面三角形结构 |
B.图乙中,1号C的杂化方式是 |
| C.图甲中碳原子数和六元环数之比为2:1 |
| D.将50nm左右的石墨烯或氧化石墨烯溶于水,在相同条件下所得到的分散系后者更为稳定 |
您最近一年使用:0次



