名校
1 . ① ②
② ③
③ ④
④ 这些分子和离子中,VSEPR模型为四面体形且分子或离子的空间结构为三角锥形的是
这些分子和离子中,VSEPR模型为四面体形且分子或离子的空间结构为三角锥形的是
 ②
② ③
③ ④
④ 这些分子和离子中,VSEPR模型为四面体形且分子或离子的空间结构为三角锥形的是
这些分子和离子中,VSEPR模型为四面体形且分子或离子的空间结构为三角锥形的是| A.①② | B.②③ | C.③④ | D.①④ |
您最近半年使用:0次
解题方法
2 . 腺嘌呤核苷酸是生产核酸类药物的中间体,其分子结构如图所示。下列有关说法正确的是

| A.能发生消去反应和加成反应 | B.所有中心原子均采取 杂化 杂化 |
C.水解生成的碱基的分子式为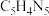 | D.水解生成的戊糖的核磁共振氢谱有7组峰 |
您最近半年使用:0次
名校
解题方法
3 . 下列叙述不 正确的是
A.杂化轨道只用于形成 键或用于容纳未参与成键的孤电子对 键或用于容纳未参与成键的孤电子对 |
| B.同系物相对分子质量一定不相同,同分异构体相对分子质量一定相同 |
C.某原子的电子排布式为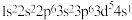 ,属于激发态 ,属于激发态 |
| D.接近水的沸点的水蒸气的相对分子质量测定值大于18 |
您最近半年使用:0次
名校
解题方法
4 . 甲胺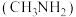 是一种弱碱
是一种弱碱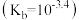 ,可与盐酸反应生成盐酸盐(用
,可与盐酸反应生成盐酸盐(用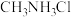 表示)。下列叙述不正确的是
表示)。下列叙述不正确的是
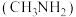 是一种弱碱
是一种弱碱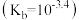 ,可与盐酸反应生成盐酸盐(用
,可与盐酸反应生成盐酸盐(用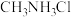 表示)。下列叙述不正确的是
表示)。下列叙述不正确的是A.甲胺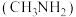 中氮原子采用 中氮原子采用 杂化 杂化 |
B. 水溶液的 水溶液的 |
C.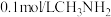 水溶液加水稀释, 水溶液加水稀释, 降低 降低 |
D.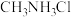 水溶液中: 水溶液中: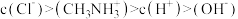 |
您最近半年使用:0次
名校
5 . 下列各组物质中,都含有两个π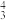 的是
的是
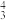 的是
的是A.N2O,CO2,N | B.N2O,NO2,N |
| C.N2O,CO2,NO2 | D.NO2,CO2,N |
您最近半年使用:0次
名校
6 . 下列关于原子轨道的说法正确的是
| A.杂化轨道既可能形成σ键,也可能形成π键 |
| B.CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和1个C原子的2p轨道混合起来而形成的 |
| C.s轨道和p轨道杂化不可能有sp4杂化轨道出现 |
| D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
您最近半年使用:0次
名校
解题方法
7 . 下列说法不正确的是
| A.氢键属于化学键 |
B.已知乙烯的分子结构中存在 ,其含有1个 ,其含有1个 键和1个 键和1个 键 键 |
C.杂化轨道只用于形成共价 键 键 |
D.粒子 的VSEPR模型与离子的空间结构不一致 的VSEPR模型与离子的空间结构不一致 |
您最近半年使用:0次
名校
解题方法
8 . 铁能形成多种化合物,如 (羰基铁),它们在生活生产中有广泛应用。
(羰基铁),它们在生活生产中有广泛应用。
(1)实验室常用KSCN溶液、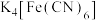 溶液、苯酚溶液检验
溶液、苯酚溶液检验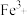 。N、O、S的第一电离能由大到小的顺序为
。N、O、S的第一电离能由大到小的顺序为___________ : 中的碳原子的杂化轨道类型为
中的碳原子的杂化轨道类型为___________ ;与 互为等电子体的分子是
互为等电子体的分子是___________ 。 中含
中含 键的数目为
键的数目为___________ 。
(2)汽车安全气囊气体发生剂一种组合主要有叠氮化钠( )、三氧化二铁(
)、三氧化二铁( )、硝酸铵(
)、硝酸铵( )。叠氢化钠收到撞击后产生气体并放出热量,硝酸铵吸收热量分解,金属钠与铁的氧化物反应。
)。叠氢化钠收到撞击后产生气体并放出热量,硝酸铵吸收热量分解,金属钠与铁的氧化物反应。 为
为___________ (共价化合物、离子化合物、), 中心原子杂化轨道类型为
中心原子杂化轨道类型为___________ 。
(3)羰基铁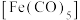 为分子构成的物质,可用作催化剂。据文献报道:
为分子构成的物质,可用作催化剂。据文献报道: 催化某反应的一种反应机理如下图所示。下列叙述错误的是___________。
催化某反应的一种反应机理如下图所示。下列叙述错误的是___________。
 (羰基铁),它们在生活生产中有广泛应用。
(羰基铁),它们在生活生产中有广泛应用。(1)实验室常用KSCN溶液、
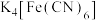 溶液、苯酚溶液检验
溶液、苯酚溶液检验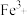 。N、O、S的第一电离能由大到小的顺序为
。N、O、S的第一电离能由大到小的顺序为 中的碳原子的杂化轨道类型为
中的碳原子的杂化轨道类型为 互为等电子体的分子是
互为等电子体的分子是 中含
中含 键的数目为
键的数目为(2)汽车安全气囊气体发生剂一种组合主要有叠氮化钠(
 )、三氧化二铁(
)、三氧化二铁( )、硝酸铵(
)、硝酸铵( )。叠氢化钠收到撞击后产生气体并放出热量,硝酸铵吸收热量分解,金属钠与铁的氧化物反应。
)。叠氢化钠收到撞击后产生气体并放出热量,硝酸铵吸收热量分解,金属钠与铁的氧化物反应。 为
为 中心原子杂化轨道类型为
中心原子杂化轨道类型为(3)羰基铁
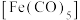 为分子构成的物质,可用作催化剂。据文献报道:
为分子构成的物质,可用作催化剂。据文献报道: 催化某反应的一种反应机理如下图所示。下列叙述错误的是___________。
催化某反应的一种反应机理如下图所示。下列叙述错误的是___________。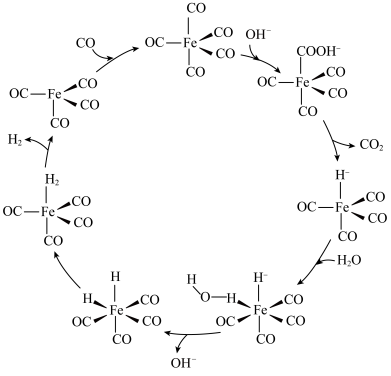
A. 参与了该催化循环 参与了该催化循环 | B.该反应可产生清洁燃料 |
C.该反应可消耗温室气体 | D.该催化循环中Fe的成键数目发生变化 |
您最近半年使用:0次
9 . 碳中和的目标是减少含碳气体的排放。CH4与CO2都能引起温室效应,将二者联合处理不仅可以减缓温室气体排放,还可以转化为CH3OH、CH3COOH、H2等高附加值产品。
(1)CH4与CO2在一定条件下能发生如下两个反应:
Ⅰ.CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1=+247kJ/mol
2CO(g)+2H2(g) ΔH1=+247kJ/mol
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ/mol
CO(g)+H2O(g) ΔH2=+41kJ/mol
若CH4与CO2按物质的量之比1∶3投料在某恒容密闭容器中发生上述反应,一定时间内CH4与CO2的转化率随温度的变化如图所示,其中CO2在1000℃时的平衡转化率为60%,CH4在1000℃时的平衡转化率几乎为100%。_______ 下能自发进行(填“高温”或“低温”)。
②温度高于700℃ 时,随温度升高,平衡产物中H2O的体积分数_______ (填“增大”“减小”或“不变”)。
③1000℃时反应Ⅱ 的平衡常数K=_______ (保留3位有效数字,下同),平衡时CO的体积分数为_______ 。
(2)CH4与CO2在催化剂作用下反应可生成CH3COOH,其反应机理如图所示。_______ 。
②转化过程中经历了i→ii的变化,该变化过程_______ (填“吸热”或“放热”)。产物CH3COOH中碳原子的杂化方式为_______ 。
③甲醇(CH3OH)与氧气形成的燃料电池是新能源汽车等领域常用的电池。通常以石墨为电极,KOH溶液为电解质溶液,该电池放电时,负极反应式为_______ 。
(1)CH4与CO2在一定条件下能发生如下两个反应:
Ⅰ.CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1=+247kJ/mol
2CO(g)+2H2(g) ΔH1=+247kJ/molⅡ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ/mol
CO(g)+H2O(g) ΔH2=+41kJ/mol若CH4与CO2按物质的量之比1∶3投料在某恒容密闭容器中发生上述反应,一定时间内CH4与CO2的转化率随温度的变化如图所示,其中CO2在1000℃时的平衡转化率为60%,CH4在1000℃时的平衡转化率几乎为100%。
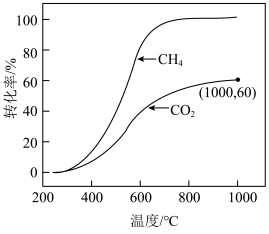
②温度高于700℃ 时,随温度升高,平衡产物中H2O的体积分数
③1000℃时反应Ⅱ 的平衡常数K=
(2)CH4与CO2在催化剂作用下反应可生成CH3COOH,其反应机理如图所示。
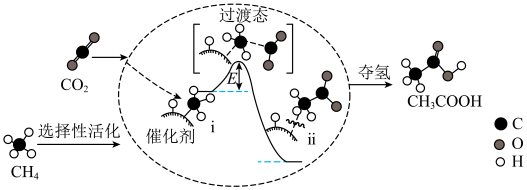
②转化过程中经历了i→ii的变化,该变化过程
③甲醇(CH3OH)与氧气形成的燃料电池是新能源汽车等领域常用的电池。通常以石墨为电极,KOH溶液为电解质溶液,该电池放电时,负极反应式为
您最近半年使用:0次
名校
解题方法
10 . 焦亚硫酸钠( )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1) 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为__________ 。
(2)“ 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图:__________ 。
②饱和碳酸氢钠溶液的作用是__________ 。
③三颈烧瓶中生成 反应的化学方程式为
反应的化学方程式为__________ ( 为沉淀物)。
为沉淀物)。
(3)“ 制备”反应过程分四步:
制备”反应过程分四步:
步骤Ⅰ.在碳酸钠溶液中通入 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;
步骤Ⅱ.停止通 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;
步骤Ⅲ.继续通入 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;
步骤Ⅳ.当溶液中 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。
①步骤Ⅰ测量溶液的pH=4.1所用仪器是__________ 。
②写出步骤Ⅱ中反应的离子方程式:__________ 。
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:__________ 。
 )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1)
 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为(2)“
 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图: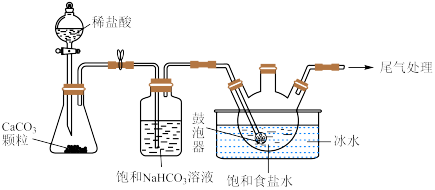
②饱和碳酸氢钠溶液的作用是
③三颈烧瓶中生成
 反应的化学方程式为
反应的化学方程式为 为沉淀物)。
为沉淀物)。(3)“
 制备”反应过程分四步:
制备”反应过程分四步:步骤Ⅰ.在碳酸钠溶液中通入
 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;步骤Ⅱ.停止通
 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;步骤Ⅲ.继续通入
 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;步骤Ⅳ.当溶液中
 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。①步骤Ⅰ测量溶液的pH=4.1所用仪器是
②写出步骤Ⅱ中反应的离子方程式:
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:
您最近半年使用:0次
2024-04-07更新
|
208次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题



