名校
解题方法
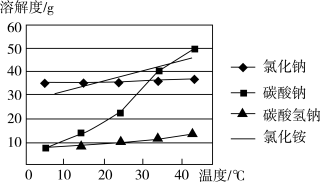
1 . 我国化工专家侯德榜提出将氨碱法与合成氨联合生产的改进工艺,这就是联合制碱法,也称侯氏制碱法。侯氏制碱法的工业生产分为两个过程,分别为生产纯碱的制碱过程和生产氯化铵的制氨过程。工艺流程如下:
(1)“产品1”的化学式为___________ ,“过滤”后得到“产品1”的方法为___________ ,写出“产品2”的一种常见用途___________ 。
(2)写出“碳化”时发生反应的化学方程式___________
(3)采用“冷析”分离出产品2的原因是___________
(4)关于“母液1”的说法正确的是___________ (填序号)。
A.“母液1”中主要含有 、
、 、
、 、
、
B.“母液1”与“母液2”成分相同
C.“母液1”中溶质只有氯化铵
(5)研究表明,“吸氨2”不仅可以促进“产品2”的分离还可以减少某种杂质的析出,写出“吸氨2”中反应的离子方程式___________ 。

(1)“产品1”的化学式为
(2)写出“碳化”时发生反应的化学方程式
(3)采用“冷析”分离出产品2的原因是
(4)关于“母液1”的说法正确的是
A.“母液1”中主要含有
 、
、 、
、 、
、
B.“母液1”与“母液2”成分相同
C.“母液1”中溶质只有氯化铵
(5)研究表明,“吸氨2”不仅可以促进“产品2”的分离还可以减少某种杂质的析出,写出“吸氨2”中反应的离子方程式
您最近半年使用:0次
解题方法
2 . 下列说法不正确的是
| A.侯德榜是我国著名化工专家,发明了侯氏制碱法 |
| B.舍勒发现了一种黄绿色气体,戴维确认该气体为氯气 |
| C.屠呦呦——从青蒿中提取青蒿素 |
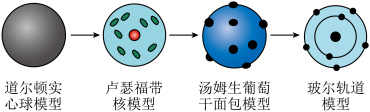
| D.原子结构模型演变历史可以表示为如图 |
您最近半年使用:0次
3 . 侯德榜提出的联合制碱法得到世界各国认可,其工业流程如图所示:

| A.试剂X可以是NaCl,滤液中加入试剂X有利于NaHCO3析出 |
| B.进行反应1时,往饱和食盐水中先通入NH3,再通入CO2 |
| C.操作1为蒸发浓缩,冷却结晶,过滤洗涤干燥 |
| D.副产物可以用作肥料使用 |
您最近半年使用:0次
4 . 在指定条件下,下列选项所示的物质间转化能实现的是
A.N2(g)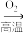 NO(g) NO(g) HNO3(aq) HNO3(aq) |
B.Al2O3(s)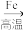 Al(s) Al(s) NaAlO2(aq) NaAlO2(aq) |
C.BaCl2(aq)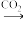 BaCO3(g) BaCO3(g) BaSO4(s) BaSO4(s) |
D.NaCl(aq)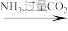 NaHCO3(aq) NaHCO3(aq) Na2CO3(s) Na2CO3(s) |
您最近半年使用:0次
2024-04-20更新
|
136次组卷
|
2卷引用:12 2024苏州太仓明德高级中学高一3月月考
23-24高一下·全国·课后作业
名校
5 . 氮及其化合物的转化具有重要应用。下列说法不正确的是
| A.“雷雨发庄稼”和合成氨工业都属于氮的固定 |
| B.侯氏制碱法的副产物可以作为氮肥 |
| C.多种形态的氮及其化合物间的转化形成了自然界的“氮循环” |
| D.二氧化硫、氮氧化物溶于雨水会形成酸雨,酸雨的pH约为5.6 |
您最近半年使用:0次
2024-04-11更新
|
919次组卷
|
4卷引用:5.2.1氮气和氮的氧化物课后作业基础篇
6 . 化学与生产、生活紧密相关,下列说法正确的是
| A.食盐是由钠原子和氯原子直接组成的 |
| B.95%的酒精一定比75%的酒精消毒效果更好 |
| C.模拟“侯氏制碱法”的实验中,应向饱和氯化钠溶液中依次通入CO2、NH3 |
| D.“百炼成钢”是指通过反复锤炼,除去铁中部分杂质,使其转化为钢 |
您最近半年使用:0次
名校
解题方法
7 . 以食盐为钠源制备纯碱的一种工艺流程如图。 碳酸化,过滤。
碳酸化,过滤。
①煅烧滤渣制取纯碱的化学方程式为_____ 。
②滤渣成分可作膨松剂,制馒头时与食醋( )共用效果更佳,相关的离子方程式为
)共用效果更佳,相关的离子方程式为_____ 。
(2)该流程中,可以循环利用的物质有 和
和_____ 。

 碳酸化,过滤。
碳酸化,过滤。①煅烧滤渣制取纯碱的化学方程式为
②滤渣成分可作膨松剂,制馒头时与食醋(
 )共用效果更佳,相关的离子方程式为
)共用效果更佳,相关的离子方程式为(2)该流程中,可以循环利用的物质有
 和
和
您最近半年使用:0次
名校
解题方法
8 . 下列有关化学工业的说法中,正确的是
| A.侯氏制碱法的目标产品是碳酸氢钠 |
| B.电子工业中常用覆铜板为基础材料制作印刷电路板 |
| C.硫酸工业中,常用水吸收SO3来生成H2SO4 |
| D.冶金工业上常用氢气还原法从NaCl中获取Na |
您最近半年使用:0次
名校
解题方法
9 . 焦亚硫酸钠( )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1) 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为__________ 。
(2)“ 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图:__________ 。
②饱和碳酸氢钠溶液的作用是__________ 。
③三颈烧瓶中生成 反应的化学方程式为
反应的化学方程式为__________ ( 为沉淀物)。
为沉淀物)。
(3)“ 制备”反应过程分四步:
制备”反应过程分四步:
步骤Ⅰ.在碳酸钠溶液中通入 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;
步骤Ⅱ.停止通 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;
步骤Ⅲ.继续通入 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;
步骤Ⅳ.当溶液中 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。
①步骤Ⅰ测量溶液的pH=4.1所用仪器是__________ 。
②写出步骤Ⅱ中反应的离子方程式:__________ 。
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:__________ 。
 )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1)
 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为(2)“
 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图: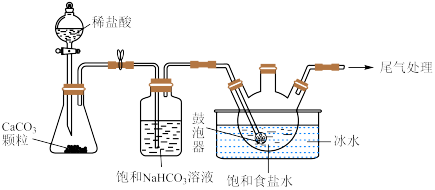
②饱和碳酸氢钠溶液的作用是
③三颈烧瓶中生成
 反应的化学方程式为
反应的化学方程式为 为沉淀物)。
为沉淀物)。(3)“
 制备”反应过程分四步:
制备”反应过程分四步:步骤Ⅰ.在碳酸钠溶液中通入
 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;步骤Ⅱ.停止通
 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;步骤Ⅲ.继续通入
 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;步骤Ⅳ.当溶液中
 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。①步骤Ⅰ测量溶液的pH=4.1所用仪器是
②写出步骤Ⅱ中反应的离子方程式:
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:
您最近半年使用:0次
2024-04-07更新
|
208次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
10 . 下列现象对应的离子反应方程式正确的是
A.水玻璃长期露置在空气中变浑浊 |
B.铜丝与铁丝缠绕一起浸在稀硫酸中,铜丝表面有气泡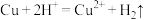 |
C.二氧化硫通入品红溶液中,红色褪去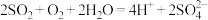 |
D.食盐的氨水溶液中通入过量的二氧化碳,有白色固体产生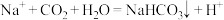 |
您最近半年使用:0次



