名校
1 . 根据侯德榜制碱法原理并参考下表的数据,实验室制备纯碱  的主要步骤是:将配制好的饱和
的主要步骤是:将配制好的饱和 溶液倒入烧杯中加热,控制温度在
溶液倒入烧杯中加热,控制温度在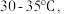 搅拌下分批加入研细的
搅拌下分批加入研细的 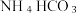 固体,加料完毕后,继续保温 30分钟,静置、过滤得
固体,加料完毕后,继续保温 30分钟,静置、过滤得  晶体。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得
晶体。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得 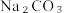 固体。
固体。
四种盐在不同温度下的溶解度(g/100g水)表
 会有分解
会有分解
请回答:
(1)反应温度控制在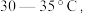 是因为若高于
是因为若高于 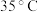 ;则
;则___________ ,若低于 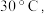 则
则___________ ;为控制此温度范围,采取的加热方法为___________ 。
(2)加料完毕后,继续保温30分钟,目的是___________ 。静置后只析出  晶体的原因是
晶体的原因是___________ 。用蒸馏水洗涤  品体的目的是除去
品体的目的是除去___________ 杂质(以化学式表示)。
(3)过滤所得的母液中含有___________ (以化学式表示),需加入___________ ,并作进一步处理,使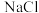 溶液循环使用,同时可回收
溶液循环使用,同时可回收 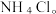
(4)测试纯碱产品中 含量的方法是:准确称取纯碱样品
含量的方法是:准确称取纯碱样品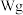 ,放入锥形瓶中加蒸馏水溶解,加 1~2滴酚酞指示剂,用物质的量浓度为
,放入锥形瓶中加蒸馏水溶解,加 1~2滴酚酞指示剂,用物质的量浓度为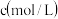 的
的 溶液滴定至溶液由红色到无色(指示
溶液滴定至溶液由红色到无色(指示 反应的终点),所用
反应的终点),所用 溶液体积为
溶液体积为 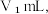 再加 1~2 滴甲基橙指示剂,继续用
再加 1~2 滴甲基橙指示剂,继续用 溶液滴定至溶液由黄变橙,所
溶液滴定至溶液由黄变橙,所 溶液总体积为
溶液总体积为 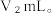 、写出纯碱样品中
、写出纯碱样品中  质量分数的计算式:
质量分数的计算式: 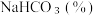 =
=___________ 。
 的主要步骤是:将配制好的饱和
的主要步骤是:将配制好的饱和 溶液倒入烧杯中加热,控制温度在
溶液倒入烧杯中加热,控制温度在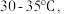 搅拌下分批加入研细的
搅拌下分批加入研细的 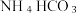 固体,加料完毕后,继续保温 30分钟,静置、过滤得
固体,加料完毕后,继续保温 30分钟,静置、过滤得  晶体。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得
晶体。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得 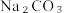 固体。
固体。四种盐在不同温度下的溶解度(g/100g水)表
| 盐 溶解度 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH₄HCO₃ | 11.9 | 15.8 | 21.0 | 27.0 | -① | — | — | — |
| NaHCO₃ | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
| NH₄Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
 会有分解
会有分解请回答:
(1)反应温度控制在
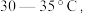 是因为若高于
是因为若高于 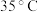 ;则
;则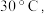 则
则(2)加料完毕后,继续保温30分钟,目的是
 晶体的原因是
晶体的原因是 品体的目的是除去
品体的目的是除去(3)过滤所得的母液中含有
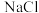 溶液循环使用,同时可回收
溶液循环使用,同时可回收 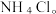
(4)测试纯碱产品中
 含量的方法是:准确称取纯碱样品
含量的方法是:准确称取纯碱样品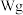 ,放入锥形瓶中加蒸馏水溶解,加 1~2滴酚酞指示剂,用物质的量浓度为
,放入锥形瓶中加蒸馏水溶解,加 1~2滴酚酞指示剂,用物质的量浓度为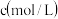 的
的 溶液滴定至溶液由红色到无色(指示
溶液滴定至溶液由红色到无色(指示 反应的终点),所用
反应的终点),所用 溶液体积为
溶液体积为 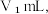 再加 1~2 滴甲基橙指示剂,继续用
再加 1~2 滴甲基橙指示剂,继续用 溶液滴定至溶液由黄变橙,所
溶液滴定至溶液由黄变橙,所 溶液总体积为
溶液总体积为 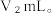 、写出纯碱样品中
、写出纯碱样品中  质量分数的计算式:
质量分数的计算式: 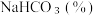 =
=
您最近半年使用:0次
2 . 1943年侯德榜发明联合制碱法,其生产流程可简要表示为

已知: 极易溶于水生成
极易溶于水生成 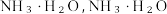 可电离产生
可电离产生 和
和 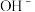 。
。
下列说法中错误的是

已知:
 极易溶于水生成
极易溶于水生成 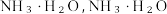 可电离产生
可电离产生 和
和 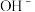 。
。下列说法中错误的是
A.母液中的溶质只含有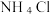 |
| B.若实验室进行第③步操作需要漏斗、烧杯、玻璃棒等仪器 |
C.侯氏制碱法制备 ,利用了物质的溶解度差异 ,利用了物质的溶解度差异 |
D.生成 悬浊液的离子方程式为 悬浊液的离子方程式为 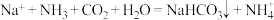 |
您最近半年使用:0次
2023-11-17更新
|
147次组卷
|
2卷引用:天津市滨海新区塘沽第一中学2023-2024学年高一上学期11月期中化学试题
3 . 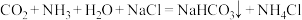 为侯氏制碱法的反应原理,制备过程为:
为侯氏制碱法的反应原理,制备过程为:
气体A的饱和溶液 A和食盐的饱和溶液
A和食盐的饱和溶液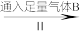 悬浊液
悬浊液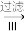 晶体
晶体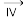 纯碱
纯碱
则下列叙述错误的是
| A.把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉 |
B.第IV步操作发生的化学反应方程式为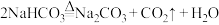 |
C.A气体是 ,B气体是 ,B气体是 |
| D.纯碱可广泛地用于玻璃、制皂、造纸、纺织等工业中 |
您最近半年使用:0次
2023-09-21更新
|
223次组卷
|
2卷引用:天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题
4 . 1943年发明联合制碱法,为我国的化学工业发展和技术创新作出重要贡献的科学家是
| A.屠呦呦 | B.侯德榜 | C.张青莲 | D.徐光宪 |
您最近半年使用:0次
5 . 侯氏制碱法为国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备少量 ,得到副产品
,得到副产品 和
和 ,流程如下图:
,流程如下图:
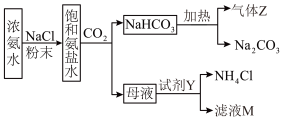
按要求回答下列问题。
(1)写出上图制备 总反应的化学方程式:
总反应的化学方程式:___________ 。
(2)制取 时为使下图A装置中分液漏斗内的稀盐酸顺利滴下,可将玻璃塞上的凹槽对准漏斗颈部的小孔或者
时为使下图A装置中分液漏斗内的稀盐酸顺利滴下,可将玻璃塞上的凹槽对准漏斗颈部的小孔或者___________ 。
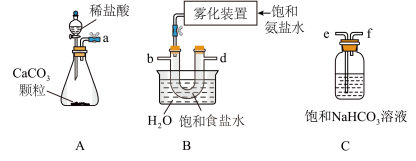
(3)制备 时,需将A装置产生的气体,与B、C装置导管进行连接,其接口顺序是a
时,需将A装置产生的气体,与B、C装置导管进行连接,其接口顺序是a___________ (按气流方向,用小写字母表示)。“雾化装置”的优点是___________ 。
(4)反应完成后,将装置B中混合物处理得到固体 和母液。
和母液。
①将固体 加热充分,并将产生的气体先通过足量的试剂X吸收水分,再通过足量
加热充分,并将产生的气体先通过足量的试剂X吸收水分,再通过足量 ,
, 增重0.14g。试剂X为
增重0.14g。试剂X为___________ ,产品 的质量为
的质量为___________ g。
②已知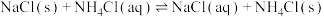 ;NaCl和
;NaCl和 溶解度曲线(如图)。
溶解度曲线(如图)。
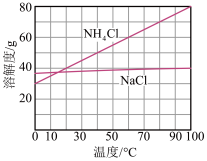
i.为使 沉淀从母液中充分析出,需向母液中加入的试剂Y为
沉淀从母液中充分析出,需向母液中加入的试剂Y为___________ ;
ii.得到副产品 所需的操作有
所需的操作有___________ 、___________ 、过滤、洗涤、干燥。
(5)题干实验流程中可以回收再利用的物质有___________ 。
(6)称量吸收了一定量水分的 粉末,配制成
粉末,配制成 标准溶液,用于滴定未知浓度盐酸的浓度。预测该标准液对滴定结果造成的影响是
标准溶液,用于滴定未知浓度盐酸的浓度。预测该标准液对滴定结果造成的影响是___________ (填“偏高”“偏低”“无影响”)。
 ,得到副产品
,得到副产品 和
和 ,流程如下图:
,流程如下图:
按要求回答下列问题。
(1)写出上图制备
 总反应的化学方程式:
总反应的化学方程式:(2)制取
 时为使下图A装置中分液漏斗内的稀盐酸顺利滴下,可将玻璃塞上的凹槽对准漏斗颈部的小孔或者
时为使下图A装置中分液漏斗内的稀盐酸顺利滴下,可将玻璃塞上的凹槽对准漏斗颈部的小孔或者
(3)制备
 时,需将A装置产生的气体,与B、C装置导管进行连接,其接口顺序是a
时,需将A装置产生的气体,与B、C装置导管进行连接,其接口顺序是a(4)反应完成后,将装置B中混合物处理得到固体
 和母液。
和母液。①将固体
 加热充分,并将产生的气体先通过足量的试剂X吸收水分,再通过足量
加热充分,并将产生的气体先通过足量的试剂X吸收水分,再通过足量 ,
, 增重0.14g。试剂X为
增重0.14g。试剂X为 的质量为
的质量为②已知
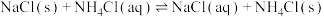 ;NaCl和
;NaCl和 溶解度曲线(如图)。
溶解度曲线(如图)。
i.为使
 沉淀从母液中充分析出,需向母液中加入的试剂Y为
沉淀从母液中充分析出,需向母液中加入的试剂Y为ii.得到副产品
 所需的操作有
所需的操作有(5)题干实验流程中可以回收再利用的物质有
(6)称量吸收了一定量水分的
 粉末,配制成
粉末,配制成 标准溶液,用于滴定未知浓度盐酸的浓度。预测该标准液对滴定结果造成的影响是
标准溶液,用于滴定未知浓度盐酸的浓度。预测该标准液对滴定结果造成的影响是
您最近半年使用:0次
解题方法
6 . 回答下列问题
(1)侯德榜先生发明的侯氏制碱法为我国纯碱工业和经济发展做出了重要贡献.某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 。
。
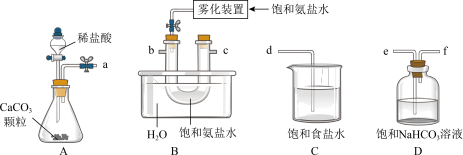
①如图B中饱和氨盐水是在饱和食盐水中通入氨气形成的,使用雾化装置的优点是______ 。
②向饱和氨盐水中通入二氧化碳,利用 在溶液中溶解度较小,析出
在溶液中溶解度较小,析出 .生成
.生成 的总反应的化学方程式为
的总反应的化学方程式为______ 。
③A~D中选择合适的仪器制备 ,正确的连接顺序是
,正确的连接顺序是______ (按气流方向,用小写字母表示),最后通入NaOH溶液。
(2)实验室需配制240mL1.0mol/L 溶液,请回答下列问题:
溶液,请回答下列问题:
①实验中除了用到托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管外,还需用到的玻璃仪器有______ 。
②通过计算可知,该实验需要用托盘天平称量______ g 。
。
③实际配得溶液的浓度小于1.0mo/L,原因不可能的是______ (填序号)。
a.转移溶液前容量瓶内有少量蒸馏水
b.定容摇匀后,发现液面下降,继续加水至刻度线
c.定容时仰视刻度线
(3) 与砂糖混用可以作补血剂,工业上用
与砂糖混用可以作补血剂,工业上用 溶液和
溶液和 溶液发生复分解反应制备.(已知溶液pH大于8.8时,
溶液发生复分解反应制备.(已知溶液pH大于8.8时, 转化为
转化为 沉淀,实验中所用
沉淀,实验中所用 溶液的pH=10)。
溶液的pH=10)。
①上述制备 沉淀时的具体操作是将
沉淀时的具体操作是将______ 溶液缓慢加入盛有______ 溶液的烧杯中,过滤、洗涤、干燥。
②将 溶液缓慢加入到盛有
溶液缓慢加入到盛有 ,溶液的烧杯中也能得到
,溶液的烧杯中也能得到 沉淀,同时在实验中观察到有无色无味的气体产生,该反应的离子方程式为
沉淀,同时在实验中观察到有无色无味的气体产生,该反应的离子方程式为______ 。
(4)某同学在常温下,向100mLNaOH溶液中通入一定量的 气体制备
气体制备 溶液。为测定溶液成分,该同学向所得溶液中逐滴加入0.3mol/L的盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示(不考虑
溶液。为测定溶液成分,该同学向所得溶液中逐滴加入0.3mol/L的盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示(不考虑 溶于水)
溶于水)
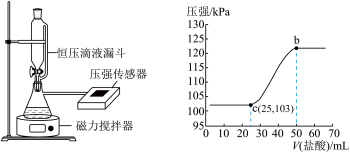
①该同学所得溶液的溶质成分为______ 。
②该同学使用的NaOH溶液的物质的量浓度为______ mol/L。
(1)侯德榜先生发明的侯氏制碱法为我国纯碱工业和经济发展做出了重要贡献.某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备
 。
。①如图B中饱和氨盐水是在饱和食盐水中通入氨气形成的,使用雾化装置的优点是
②向饱和氨盐水中通入二氧化碳,利用
 在溶液中溶解度较小,析出
在溶液中溶解度较小,析出 .生成
.生成 的总反应的化学方程式为
的总反应的化学方程式为③A~D中选择合适的仪器制备
 ,正确的连接顺序是
,正确的连接顺序是
(2)实验室需配制240mL1.0mol/L
 溶液,请回答下列问题:
溶液,请回答下列问题:①实验中除了用到托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管外,还需用到的玻璃仪器有
②通过计算可知,该实验需要用托盘天平称量
 。
。③实际配得溶液的浓度小于1.0mo/L,原因不可能的是
a.转移溶液前容量瓶内有少量蒸馏水
b.定容摇匀后,发现液面下降,继续加水至刻度线
c.定容时仰视刻度线
(3)
 与砂糖混用可以作补血剂,工业上用
与砂糖混用可以作补血剂,工业上用 溶液和
溶液和 溶液发生复分解反应制备.(已知溶液pH大于8.8时,
溶液发生复分解反应制备.(已知溶液pH大于8.8时, 转化为
转化为 沉淀,实验中所用
沉淀,实验中所用 溶液的pH=10)。
溶液的pH=10)。①上述制备
 沉淀时的具体操作是将
沉淀时的具体操作是将②将
 溶液缓慢加入到盛有
溶液缓慢加入到盛有 ,溶液的烧杯中也能得到
,溶液的烧杯中也能得到 沉淀,同时在实验中观察到有无色无味的气体产生,该反应的离子方程式为
沉淀,同时在实验中观察到有无色无味的气体产生,该反应的离子方程式为(4)某同学在常温下,向100mLNaOH溶液中通入一定量的
 气体制备
气体制备 溶液。为测定溶液成分,该同学向所得溶液中逐滴加入0.3mol/L的盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示(不考虑
溶液。为测定溶液成分,该同学向所得溶液中逐滴加入0.3mol/L的盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示(不考虑 溶于水)
溶于水)
①该同学所得溶液的溶质成分为
②该同学使用的NaOH溶液的物质的量浓度为
您最近半年使用:0次
名校
7 . 侯德榜创立了中国人自己的制碱工艺——侯氏制碱法。实验室模拟侯氏制碱法,下列装置的选择及连接顺序最优的是
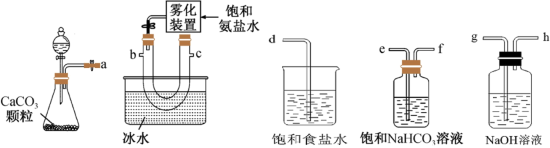

| A.abcgh | B.aghbcd | C.aefbcd | D.aefbcgh |
您最近半年使用:0次
名校
8 . 侯德榜是我国杰出的化学家,“侯氏制碱法”的创始人。1926年,塘沽“红三角”牌纯碱在万国博览会获金质奖章。反应: ,是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解,其中不正确的是
,是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解,其中不正确的是

 ,是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解,其中不正确的是
,是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解,其中不正确的是
A.小韩同学说:该条件下 的溶解度较小 的溶解度较小 |
B.小韦同学说: 不是纯碱 不是纯碱 |
C.小羊同学说:析出 固体后的溶液中只含氯化铵,可做化肥 固体后的溶液中只含氯化铵,可做化肥 |
| D.小任同学说:该反应是在饱和食盐水中先通入氨气,再通入二氧化碳 |
您最近半年使用:0次
名校
9 . 氨是一种重要的化工原料,根据下图转化判断下列有关表述正确的是
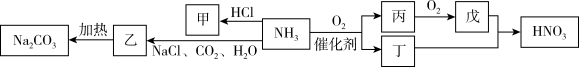

| A.浓硝酸见光易分解且易挥发,应用棕色试剂瓶盛放且用胶塞密封 |
| B.戊与丁反应时,氧化剂与还原剂的物质的量之比为1∶2 |
| C.实验室中可以采取加热甲物质的方法制取氨气 |
D.向饱和NaCl溶液中依次通入过量的 和 和 ,然后过滤可制得乙 ,然后过滤可制得乙 |
您最近半年使用:0次
2023-05-11更新
|
772次组卷
|
4卷引用:天津市河北区2022-2023学年高三下学期总复习质量监测(二)化学试题
天津市河北区2022-2023学年高三下学期总复习质量监测(二)化学试题(已下线)第5讲 氮及其化合物(已下线)考点16 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)黑龙江省哈尔滨市第三中学校2023-2024学年高三上学期第一次验收(开学测试)化学试题
10 . 下列过程涉及氧化还原反应的是
A.工业上电解熔融状态 制备 制备 |
B.用 作沉淀剂,除去工业废水中的 作沉淀剂,除去工业废水中的 |
| C.石油经过分馏后可以得到汽油、煤油、柴油等轻质油 |
D.侯氏制碱法以 为原料制备 为原料制备 和 和 |
您最近半年使用:0次



