名校
解题方法
1 . 英菲替尼(化合物L)是治疗胆管癌的新型药物,其合成路线如下。
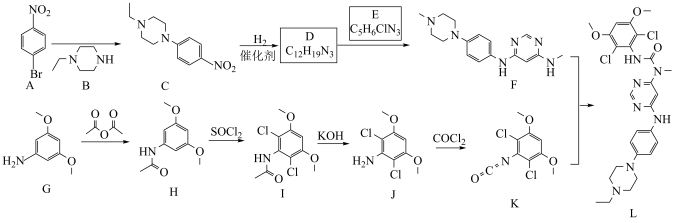
回答下列问题:
(1)A的化学名称是___________ 。
(2)由A生成C的反应类型是___________ 。
(3)E的结构简式为___________ 。
(4)由G→J的转化过程可知,G转化为H的目的是___________
(5)符合下列条件的B的同分异构体共有___________ 种,其中一种的结构简式为___________ 。
①分子中含环状结构 ②核磁共振氢谱显示2组峰
(6)L中氮原子的杂化方式为___________ 。
(7)1,3-二苯基脲(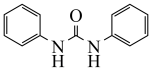 )是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
)是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。 ___________

回答下列问题:
(1)A的化学名称是
(2)由A生成C的反应类型是
(3)E的结构简式为
(4)由G→J的转化过程可知,G转化为H的目的是
(5)符合下列条件的B的同分异构体共有
①分子中含环状结构 ②核磁共振氢谱显示2组峰
(6)L中氮原子的杂化方式为
(7)1,3-二苯基脲(
 )是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
)是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
您最近半年使用:0次
2024-01-22更新
|
1062次组卷
|
6卷引用:2024年1月广西普通高等学校招生考试适应性测试化学试题
2024年1月广西普通高等学校招生考试适应性测试化学试题(已下线)2024年1月“九省联考”广西卷真题完全解读与考后提升(已下线)T18-有机综合题(已下线)化学(九省联考考后提升卷,贵州卷)-2024年1月“九省联考”真题完全解读与考后提升辽宁省沈阳市东北育才学校高中部2023-2024学年高三下学期第六次模拟考试化学试题(已下线)专题11 有机推断综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
2 . ECH(环氧氯丙烷,结构为 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。
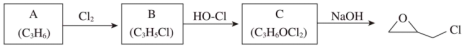
已知:
(1)A为丙烯,其分子中含有的官能团是_______ 。
(2)已知 为加成反应,
为加成反应, 的反应类型是
的反应类型是_______ 反应。
(3) 的反应中,B与次氯酸加成得到的C,有两种结构。
的反应中,B与次氯酸加成得到的C,有两种结构。
①C结构简式是ⅰ: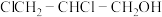 和ⅱ:
和ⅱ:_______ 。
②由分子中化学键的极性分析:ⅰ为 的主要产物。该分析过程是
的主要产物。该分析过程是_______ 。
(4)对 环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中
环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中 和物质C的比例增大,环氧氯丙烷的产率如图所示:
和物质C的比例增大,环氧氯丙烷的产率如图所示:
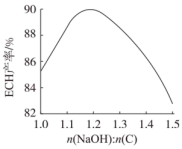
根据该反应中各物质的性质,分析随 的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):
的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):_______ 。
(5)原料中的丙烯可由石油裂解得到。在裂解分离得到的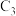 馏分中,除丙烯外,杂质气体中含有2种分子式均为
馏分中,除丙烯外,杂质气体中含有2种分子式均为 的链烃。
的链烃。
①杂质的其中一种分子内含有 杂化的碳原子,则该分子名称是
杂化的碳原子,则该分子名称是_______ 。
②杂质的另一种分子内,无 杂化的碳原子,则该分子内碳原子的杂化类型是
杂化的碳原子,则该分子内碳原子的杂化类型是_______ ;已知该分子中,4个氢原子不在同一个平面内,由分子中碳原子的杂化解释其原因:_______ 。
 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。
已知:

(1)A为丙烯,其分子中含有的官能团是
(2)已知
 为加成反应,
为加成反应, 的反应类型是
的反应类型是(3)
 的反应中,B与次氯酸加成得到的C,有两种结构。
的反应中,B与次氯酸加成得到的C,有两种结构。①C结构简式是ⅰ:
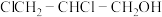 和ⅱ:
和ⅱ:②由分子中化学键的极性分析:ⅰ为
 的主要产物。该分析过程是
的主要产物。该分析过程是(4)对
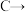 环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中
环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中 和物质C的比例增大,环氧氯丙烷的产率如图所示:
和物质C的比例增大,环氧氯丙烷的产率如图所示:
根据该反应中各物质的性质,分析随
 的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):
的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):(5)原料中的丙烯可由石油裂解得到。在裂解分离得到的
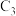 馏分中,除丙烯外,杂质气体中含有2种分子式均为
馏分中,除丙烯外,杂质气体中含有2种分子式均为 的链烃。
的链烃。①杂质的其中一种分子内含有
 杂化的碳原子,则该分子名称是
杂化的碳原子,则该分子名称是②杂质的另一种分子内,无
 杂化的碳原子,则该分子内碳原子的杂化类型是
杂化的碳原子,则该分子内碳原子的杂化类型是
您最近半年使用:0次
3 . 中国科学院天津工业生物技术研究所科研团队在实验室里首次实现了以CO2为原料人工合成淀粉,其合成路线如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
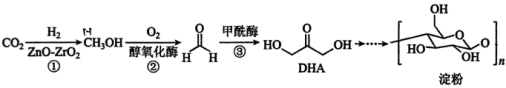

| A.1mol DHA中含有σ键数目为7NA |
| B.1mol DHA中,sp3杂化的原子数为2NA |
| C.过程②中,1mol CH3OH断裂极性键的数目为2NA |
| D.CH3OH分子中,碳原子与氧原子之间的共价键为sp3-p σ键 |
您最近半年使用:0次
2023·全国·模拟预测
解题方法
4 . 聚四氟乙烯具有耐热、耐酸碱腐蚀等优异的性能,用途广泛,有“塑料王”之称,其合成路线如图。
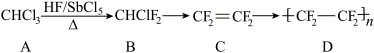
下列说法错误的是
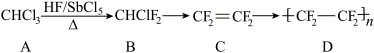
下列说法错误的是
| A.图中合成路线中涉及的碳原子杂化类型有2种 |
| B.由化合物C到化合物D的反应符合原子经济性要求 |
C. (共价化合物)中Sb的价层电子对数为5 (共价化合物)中Sb的价层电子对数为5 |
| D.H—F键的键能比H—Cl键大,所以HF的酸性强于HCl |
您最近半年使用:0次
5 . 磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷的化合物在药物生产和农药制造等方面用途非常广泛。请回答下列有关问题:
(1)画出基态P原子的核外电子排布图____ 。
(2)NH3比PH3易液化的原因是____ 。
(3)P4S3可用于制造火柴,其结构如图所示。
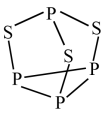
①P4S3中硫原子的杂化轨道类型为____ 。
②电负性:磷____ 硫(填“>”或“<”);第一电离能磷大于硫的原因是____ 。
(4)NH4BF4是合成氮化硼纳米管的原料之一,1mol NH4BF4中含有___ mol配位键。
(1)画出基态P原子的核外电子排布图
(2)NH3比PH3易液化的原因是
(3)P4S3可用于制造火柴,其结构如图所示。

①P4S3中硫原子的杂化轨道类型为
②电负性:磷
(4)NH4BF4是合成氮化硼纳米管的原料之一,1mol NH4BF4中含有
您最近半年使用:0次
名校
解题方法
6 . 2016 年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB 族元素对应离子的萃取,如La3+、Sc2+。写出基态二价 钪离子(Sc2+)的核外电子排布式:____ ,其中电子占据的轨道数为_____ 个。
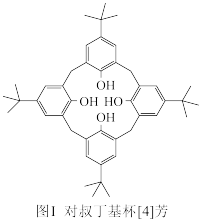
(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为_____ ,羟基间的相互作用力为_____ 。
(3)不同大小苯芳烃能识别某些离子,如:N3-、SCN−等。一定条件下,SCN−与 MnO2反应可得到(SCN)2,试写出(SCN)2的结构式_______ 。
(4)NH3分子在独立存在时 H-N-H 键角为 106.7°。 [Zn(NH3)6]2+离子中 H-N-H 键角变为 109.5°,其原因是:_________________________ 。
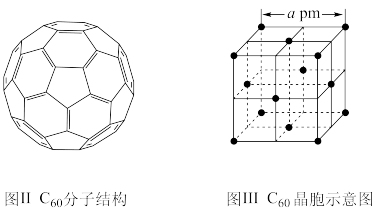
(5)已知 C60 分子结构和 C60 晶胞示意图(如图Ⅱ、图Ⅲ所示):则一个 C60 分子中含有σ键的个数为______ ,C60 晶体密度的计算式为____ g•cm−3。(NA 为阿伏加 德罗常数 的值)
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB 族元素对应离子的萃取,如La3+、Sc2+。写出基态二价 钪离子(Sc2+)的核外电子排布式:

(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为
(3)不同大小苯芳烃能识别某些离子,如:N3-、SCN−等。一定条件下,SCN−与 MnO2反应可得到(SCN)2,试写出(SCN)2的结构式
(4)NH3分子在独立存在时 H-N-H 键角为 106.7°。 [Zn(NH3)6]2+离子中 H-N-H 键角变为 109.5°,其原因是:
(5)已知 C60 分子结构和 C60 晶胞示意图(如图Ⅱ、图Ⅲ所示):则一个 C60 分子中含有σ键的个数为

您最近半年使用:0次
2020-03-03更新
|
297次组卷
|
3卷引用:湖北省武汉市华中师大学第一附属中学2020届高三二月网上检测理科综合化学试题
7 . Ⅰ. (1) 为ⅣA族元素,单质
为ⅣA族元素,单质 与干燥
与干燥 反应生成
反应生成 .常温常压下
.常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为_______ 。
(2) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式,下同),还原性由强到弱的顺序为_______ ,键角由大到小的顺序为_______ 。
Ⅱ.(1)气态氢化物热稳定性 大于
大于 的主要原因是
的主要原因是_______ 。
(2) 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是_______ 。
(3)常温下,在水中的溶解度乙醇大于氯乙烷,原因是_______ 。
Ⅲ.(1)比较给出 能力的相对强弱:
能力的相对强弱:
_______  (填“>”“<”或“=”);用一个化学方程式说明
(填“>”“<”或“=”);用一个化学方程式说明 和
和 结合
结合 能力的相对强弱:
能力的相对强弱:_______ 。
(2) 是离子化合物,各原子均满足8电子稳定结构.写出
是离子化合物,各原子均满足8电子稳定结构.写出 的电子式:
的电子式:_______ 。
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(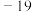 ℃)高.主要原因是
℃)高.主要原因是_______ 。
Ⅳ.研究发现,在 低压合成甲醇反应(
低压合成甲醇反应(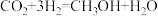 )中,
)中, 氧化物负载的
氧化物负载的 氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景.回答下列问题:
氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景.回答下列问题:
(1) 和
和 分子中C原子的杂化形式分别为
分子中C原子的杂化形式分别为_______ 和_______ 。
(2)在 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_______ ,原因是_______ 。
(3)硝酸锰是制备上述反应催化剂的原料, 中的化学键除了
中的化学键除了 键外,还存在
键外,还存在_______ 。
 为ⅣA族元素,单质
为ⅣA族元素,单质 与干燥
与干燥 反应生成
反应生成 .常温常压下
.常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为(2)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为Ⅱ.(1)气态氢化物热稳定性
 大于
大于 的主要原因是
的主要原因是(2)
 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是(3)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
Ⅲ.(1)比较给出
 能力的相对强弱:
能力的相对强弱:
 (填“>”“<”或“=”);用一个化学方程式说明
(填“>”“<”或“=”);用一个化学方程式说明 和
和 结合
结合 能力的相对强弱:
能力的相对强弱:(2)
 是离子化合物,各原子均满足8电子稳定结构.写出
是离子化合物,各原子均满足8电子稳定结构.写出 的电子式:
的电子式:(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(
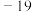 ℃)高.主要原因是
℃)高.主要原因是Ⅳ.研究发现,在
 低压合成甲醇反应(
低压合成甲醇反应(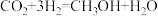 )中,
)中, 氧化物负载的
氧化物负载的 氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景.回答下列问题:
氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景.回答下列问题:(1)
 和
和 分子中C原子的杂化形式分别为
分子中C原子的杂化形式分别为(2)在
 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为(3)硝酸锰是制备上述反应催化剂的原料,
 中的化学键除了
中的化学键除了 键外,还存在
键外,还存在
您最近半年使用:0次
名校
解题方法
8 . 硼、镓、氮的化合物在生产、生活中有广泛用途:
(1)氮化镓(GaN)是新型的半导体材料。基态Ga原子的价电子排布图为_______ ;基态N原子的核外有______ 种空间运动状态的电子。
(2)氟硼酸铵(NH4BF4)是合成氮化硼纳米管的原料之一。0.1 molNH4BF4含有的配位键数目为______ ,该物质中四种元素的电负性由大到小的顺序是________________ 。
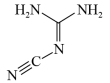
(3)鉴定镍、钴、铜、钯等可用双氰胺,其结构如下图所示。该分子中碳原子的杂化方式有_______ ;该分子中σ键与π键数目之比为__________ ;该分子中键能最大的是_________ 键。
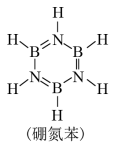
(4)硼与氮形成类似苯的化合物硼氮苯(B3N3H6),俗称无机苯,其结构如图。硼氮苯属于_______ 分子(填“极性”或“非极性”)。分子中的大π键可用符号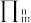 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,该分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,该分子中的大π键可表示为______________ 。
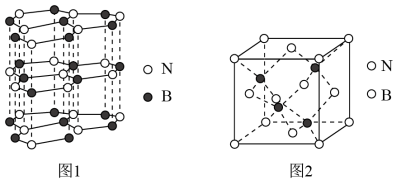
(5)氮化硼是一种性能优异的新型材料,主要结构有六方氮化硼(图1)和立方氮化硼(图2)。后者与石墨结构类似。
①50.0 g六方氮化硼晶体中含有六元环的数目为____________ 。
②立方氮化硼中N的配位数为_________ 。已知立方氮化硼密度为dg·cm-3,NA代表阿伏加德罗常数,立方氮化硼晶胞中面心上6个N原子相连构成正八面体,该正八面体的边长为_______ pm(列式即可)。
(1)氮化镓(GaN)是新型的半导体材料。基态Ga原子的价电子排布图为
(2)氟硼酸铵(NH4BF4)是合成氮化硼纳米管的原料之一。0.1 molNH4BF4含有的配位键数目为
(3)鉴定镍、钴、铜、钯等可用双氰胺,其结构如下图所示。该分子中碳原子的杂化方式有

(4)硼与氮形成类似苯的化合物硼氮苯(B3N3H6),俗称无机苯,其结构如图。硼氮苯属于
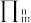 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,该分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,该分子中的大π键可表示为
(5)氮化硼是一种性能优异的新型材料,主要结构有六方氮化硼(图1)和立方氮化硼(图2)。后者与石墨结构类似。

①50.0 g六方氮化硼晶体中含有六元环的数目为
②立方氮化硼中N的配位数为
您最近半年使用:0次



