设NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2022·全国卷) 溶液中,
溶液中, 的数目为
的数目为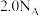
B.(2022·全国卷)电解熔融 ,阴极增重
,阴极增重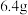 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
C.(2022·浙江卷) 和
和 于密闭容器中充分反应后,
于密闭容器中充分反应后, 分子总数为
分子总数为
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
E.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
F.(2021·广东卷)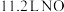 与
与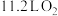 混合后的分子数目为
混合后的分子数目为
G.(2021·浙江卷)0.1 mol CH3COOH与足量CH3CH2OH充分反应生成的CH3COOCH2CH3分子数目为0.1NA
A.(2022·全国卷)
 溶液中,
溶液中, 的数目为
的数目为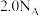
B.(2022·全国卷)电解熔融
 ,阴极增重
,阴极增重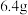 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
C.(2022·浙江卷)
 和
和 于密闭容器中充分反应后,
于密闭容器中充分反应后, 分子总数为
分子总数为
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
E.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
F.(2021·广东卷)
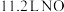 与
与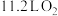 混合后的分子数目为
混合后的分子数目为
G.(2021·浙江卷)0.1 mol CH3COOH与足量CH3CH2OH充分反应生成的CH3COOCH2CH3分子数目为0.1NA
2024高三·全国·专题练习 查看更多[1]
(已下线)题型02 阿伏加德罗常数的判断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
更新时间:2024-01-06 08:11:22
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】钠及其化合物在生活生产和科研中有广泛的应用。完成下列问题:
(1)碳酸氢钠是常用膨松剂,受热分解时发生反应的化学方程式是_______ ;把一定量过氧化钠和未知量碳酸氢钠混合物放置在密闭体系中,充分加热后,产生气体,固体残留物中一定含有的物质是_______ (写化学式)。
(2) 是实验室中最常用的试剂之一,某实验需要
是实验室中最常用的试剂之一,某实验需要 的氢氧化钠溶液
的氢氧化钠溶液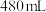 。
。
①实验除了需要托盘天平(带砝码)、药匙、烧杯和玻璃棒外,还需要的玻璃仪器是_______ 。
②根据计算需要称量 固体
固体_______ g。
③在配制过程中,若其他操作都是规范的,下列操作会引起浓度偏大的是_______ (填标号)。
A.转移溶液时不慎有少量液体洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复摇匀静置后,液面低于刻度线,再加水至刻度线
(3)汽车安全气囊中含有叠氮化钠( ),受撞击完全分解产生钠和氮气,写出反应的化学方程式
),受撞击完全分解产生钠和氮气,写出反应的化学方程式_______ ,若产生 (标准状况下)氮气,至少需要叠氮化钠
(标准状况下)氮气,至少需要叠氮化钠_______ g。
(4)钠钾合金可在核反应堆中用作热交换液。取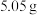 钠-钾(与钠化学性质相似)合金溶于
钠-钾(与钠化学性质相似)合金溶于 水生成
水生成 氢气。该钠-钾合金的化学组成(用
氢气。该钠-钾合金的化学组成(用 的形式表示)为
的形式表示)为_______ 。
(1)碳酸氢钠是常用膨松剂,受热分解时发生反应的化学方程式是
(2)
 是实验室中最常用的试剂之一,某实验需要
是实验室中最常用的试剂之一,某实验需要 的氢氧化钠溶液
的氢氧化钠溶液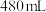 。
。①实验除了需要托盘天平(带砝码)、药匙、烧杯和玻璃棒外,还需要的玻璃仪器是
②根据计算需要称量
 固体
固体③在配制过程中,若其他操作都是规范的,下列操作会引起浓度偏大的是
A.转移溶液时不慎有少量液体洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复摇匀静置后,液面低于刻度线,再加水至刻度线
(3)汽车安全气囊中含有叠氮化钠(
 ),受撞击完全分解产生钠和氮气,写出反应的化学方程式
),受撞击完全分解产生钠和氮气,写出反应的化学方程式 (标准状况下)氮气,至少需要叠氮化钠
(标准状况下)氮气,至少需要叠氮化钠(4)钠钾合金可在核反应堆中用作热交换液。取
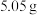 钠-钾(与钠化学性质相似)合金溶于
钠-钾(与钠化学性质相似)合金溶于 水生成
水生成 氢气。该钠-钾合金的化学组成(用
氢气。该钠-钾合金的化学组成(用 的形式表示)为
的形式表示)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)含 个
个 的
的 溶液中,氯化镁的质量为
溶液中,氯化镁的质量为___________ g。
(2)标准状况下,A气体的密度为1.25 ,B气体相对于氢气的密度为32,11.2LA和B的混合气体质量为17.6g,则A气体的相对分子质量为
,B气体相对于氢气的密度为32,11.2LA和B的混合气体质量为17.6g,则A气体的相对分子质量为___________ ,该混合气体中A和B的体积比为___________ 。
(3)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳,该反应可表示为: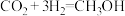
 ,则要减少0.44吨二氧化碳至少需要标准状况下
,则要减少0.44吨二氧化碳至少需要标准状况下 的体积为
的体积为___________  。
。
(4)结晶氯化铝价格便宜应用大,是饮用水、工业用水及游泳池循环水处理的高效廉价絮凝剂。为测定其化学式,现将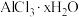 的晶体48.3g溶于水配成250
的晶体48.3g溶于水配成250 溶液,此溶液正好与含0.6
溶液,此溶液正好与含0.6
 的溶液完全作用。由上述数据可知此
的溶液完全作用。由上述数据可知此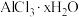 中x的数值是
中x的数值是___________
(5)苏打和小苏打在我们日常生活中用途很广泛。加热13.7g苏打和小苏打的混合物至质量不再变化,剩余固体的质量为10.6g,则此混合物中苏打与小苏打的物质的量之比为___________ 。
(1)含
 个
个 的
的 溶液中,氯化镁的质量为
溶液中,氯化镁的质量为(2)标准状况下,A气体的密度为1.25
 ,B气体相对于氢气的密度为32,11.2LA和B的混合气体质量为17.6g,则A气体的相对分子质量为
,B气体相对于氢气的密度为32,11.2LA和B的混合气体质量为17.6g,则A气体的相对分子质量为(3)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳,该反应可表示为:
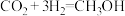
 ,则要减少0.44吨二氧化碳至少需要标准状况下
,则要减少0.44吨二氧化碳至少需要标准状况下 的体积为
的体积为 。
。(4)结晶氯化铝价格便宜应用大,是饮用水、工业用水及游泳池循环水处理的高效廉价絮凝剂。为测定其化学式,现将
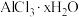 的晶体48.3g溶于水配成250
的晶体48.3g溶于水配成250 溶液,此溶液正好与含0.6
溶液,此溶液正好与含0.6
 的溶液完全作用。由上述数据可知此
的溶液完全作用。由上述数据可知此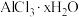 中x的数值是
中x的数值是(5)苏打和小苏打在我们日常生活中用途很广泛。加热13.7g苏打和小苏打的混合物至质量不再变化,剩余固体的质量为10.6g,则此混合物中苏打与小苏打的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下物质:①H2SO4;②氯水;③KOH固体;④熔融KHSO4;⑤漂白粉;⑥生铁;⑦SO2;⑧Al2O3;⑨蔗糖。请回答下列问题:
(1)以上物质中能导电的是_______ (填序号),以上物质中属于电解质的是_______ (填序号)。以上物质中属于非电解质的是_______ (填序号)。
(2)某物质A加热时按化学方程式 分解,产物均为全体,测得相同条件下由生成物组成的混合气体对
分解,产物均为全体,测得相同条件下由生成物组成的混合气体对 的相对密度为50,则反应物A的摩尔质量为
的相对密度为50,则反应物A的摩尔质量为_______ 。
(3)标准状况下,将V L的氨气溶于1 L的水中,所得溶液的密度为 ,此氨水的物质的量浓度是
,此氨水的物质的量浓度是_______ mol/L:已知8 mol/L的氨水的密度为 ,2 mol/L的氨水的密度为
,2 mol/L的氨水的密度为 ,
, ,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度_______ 5 mol/L(填>、<或=)。
(1)以上物质中能导电的是
(2)某物质A加热时按化学方程式
 分解,产物均为全体,测得相同条件下由生成物组成的混合气体对
分解,产物均为全体,测得相同条件下由生成物组成的混合气体对 的相对密度为50,则反应物A的摩尔质量为
的相对密度为50,则反应物A的摩尔质量为(3)标准状况下,将V L的氨气溶于1 L的水中,所得溶液的密度为
 ,此氨水的物质的量浓度是
,此氨水的物质的量浓度是 ,2 mol/L的氨水的密度为
,2 mol/L的氨水的密度为 ,
, ,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质的量是沟通宏观和微观的桥梁。
(1)0.3 mol H2S与___________ g 甲烷中所含氢原子数相等。
(2)将34.2 g Al2( SO4)3固体溶于水配成100 mL溶液,从中取出10 mL,稀释到100 mL,稀释后,所得溶液的物质的量浓度为___________ mol·L-1。
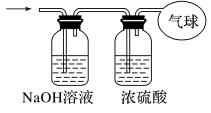
(3)现有21.6 g由CO和CO2组成的混合气体,在标准状况下体积为13.44 L。将其依次通过如图所示装置,最后收集在气球中。则气球中收集到的气体的电子总数为___________ (用NA表示阿伏加德罗常数的值),气球的体积为___________ L。(实验在标准状况下测定)
(4)48gRO 中,核外电子总数比质子总数多6.02 ×1023个,则R元素的摩尔质量为
中,核外电子总数比质子总数多6.02 ×1023个,则R元素的摩尔质量为___________ g/ mol。
(5)已知a g气体XY3中含有b个原子,设阿伏加德罗常数的值为NA,气体摩尔体积为Vm,则该条件下11.2 L该气体的质量为___________ g。
(6)某温度时,将一定量的元素A的氢化物AH3在恒温、恒压的密闭容器中完全分解为两种气态单质,此时容器的体积变为原来的 ,则A单质的化学式为
,则A单质的化学式为___________ 。
(1)0.3 mol H2S与
(2)将34.2 g Al2( SO4)3固体溶于水配成100 mL溶液,从中取出10 mL,稀释到100 mL,稀释后,所得溶液的物质的量浓度为
(3)现有21.6 g由CO和CO2组成的混合气体,在标准状况下体积为13.44 L。将其依次通过如图所示装置,最后收集在气球中。则气球中收集到的气体的电子总数为

(4)48gRO
 中,核外电子总数比质子总数多6.02 ×1023个,则R元素的摩尔质量为
中,核外电子总数比质子总数多6.02 ×1023个,则R元素的摩尔质量为(5)已知a g气体XY3中含有b个原子,设阿伏加德罗常数的值为NA,气体摩尔体积为Vm,则该条件下11.2 L该气体的质量为
(6)某温度时,将一定量的元素A的氢化物AH3在恒温、恒压的密闭容器中完全分解为两种气态单质,此时容器的体积变为原来的
 ,则A单质的化学式为
,则A单质的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列表格
| 物质 | N2 | HNO3 | SO2 |
| 质量/g | 18.9 | ___ | |
| 物质的量/mol | ___ | ___ | 1.5 |
| 标况下的体积/L | 4.48 | ___ | ___ |
| 分子个数 | ___ | ___ | ___ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.钛及其合金具有密度小,强度高,耐腐蚀等优良性能,被广泛用于航天、航空、航海、石油化工、医药等部门,因此,钛被誉为第三金属和战略金属。从钛铁矿提取金属钛(海绵钛)的主要工艺过程如下:
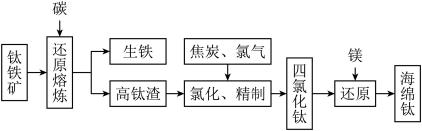
(1)钛铁矿的主要成分是 ,第一步发生的反应:
,第一步发生的反应: ,在钛酸亚铁中,钛的化合价为
,在钛酸亚铁中,钛的化合价为___________ 。
(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,该反应的氧化产物是___________ ,氧化剂和还原剂的化学计量数之比是___________ 。
Ⅱ.高铁酸钾 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。
(3)干法制备高铁酸钠的主要反应为: 该反应中还原剂是
该反应中还原剂是___________ (填化学式)。
(4)湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。
。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
②每生成 转移
转移___________  电子,若反应过程中转移了
电子,若反应过程中转移了 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为___________ mol。

(1)钛铁矿的主要成分是
 ,第一步发生的反应:
,第一步发生的反应: ,在钛酸亚铁中,钛的化合价为
,在钛酸亚铁中,钛的化合价为(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,该反应的氧化产物是
Ⅱ.高铁酸钾
 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。(3)干法制备高铁酸钠的主要反应为:
 该反应中还原剂是
该反应中还原剂是(4)湿法制备高铁酸钾(
 )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。
。①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
②每生成
 转移
转移 电子,若反应过程中转移了
电子,若反应过程中转移了 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】实验室里用软锰矿(含MnO2质量分数为60%)与浓盐酸反应来制取适量的氯气,反应方程式如下: (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。
(1)用双线桥标出该反应中电子转移的方向和数目_______ 。
(2)若生成5个Cl2分子,计算转移电子总数_______ 。
(3)产生7.1g氯气时,计算所需软锰矿的质量_______ ,被氧化的HCl的质量_______ 。
 (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。(1)用双线桥标出该反应中电子转移的方向和数目
(2)若生成5个Cl2分子,计算转移电子总数
(3)产生7.1g氯气时,计算所需软锰矿的质量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某课外小组分别用如图所示装置对原电池和电解池的原理进行实验探究。

请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)实验过程中N极附近变红,左边反应原理为Zn+CuCl2=ZnCl2+Cu。电极M是__ 极,电极反应式为___ 。
(2)若实验过程中有0.4mol电子转移,则有___ molCl-通过隔膜。
Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区逐渐产生蓝色沉淀;停止实验,铜电极明显变细,电解液仍然澄清;分别收集两极产生的气体进行实验,发现其中一种气体可在另一种气体中燃烧,据此回答下列问题。
(3)Y极产生的气体为___ (填化学式),产生该气体的电极反应式为__ 。
(4)电解过程中,X极区溶液的pH__ (填“增大“减小”或“不变”)。
(5)若在X极收集到672mL气体时,Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极( 电极)质量减少
电极)质量减少___ g。

请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)实验过程中N极附近变红,左边反应原理为Zn+CuCl2=ZnCl2+Cu。电极M是
(2)若实验过程中有0.4mol电子转移,则有
Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区逐渐产生蓝色沉淀;停止实验,铜电极明显变细,电解液仍然澄清;分别收集两极产生的气体进行实验,发现其中一种气体可在另一种气体中燃烧,据此回答下列问题。
(3)Y极产生的气体为
(4)电解过程中,X极区溶液的pH
(5)若在X极收集到672mL气体时,Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极(
 电极)质量减少
电极)质量减少
您最近一年使用:0次
【推荐2】(1)下列有关电化学的图示中,完全正确的是_____________
A.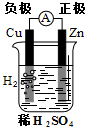 Cu-Zn原电池 B.
Cu-Zn原电池 B.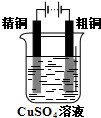 粗铜精炼
粗铜精炼
C.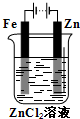 铁片镀锌 D.
铁片镀锌 D.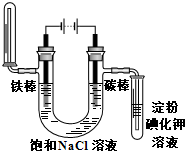 验证气体产物
验证气体产物
(2)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
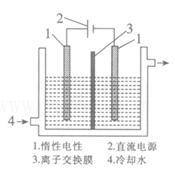
请回答下列问题:
a.碘是_________ (填颜色)固体物质,实验室常用_______ 方法来分离提纯含有少量泥沙杂质的固体碘。
b.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为________ ,每生成1mol KIO3,电路中通过的电子的物质的量为________ 。
c.电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂:淀粉溶液、淀粉-KI试纸、过氧化氢溶液、稀硫酸(用其中的一种或多种均可。)
d.电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是______________ ,步骤⑤的操作名称是________ 。步骤④洗涤晶体的目的是_________________ 。
A.
 Cu-Zn原电池 B.
Cu-Zn原电池 B. 粗铜精炼
粗铜精炼C.
 铁片镀锌 D.
铁片镀锌 D. 验证气体产物
验证气体产物(2)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。

请回答下列问题:
a.碘是
b.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为
c.电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂:淀粉溶液、淀粉-KI试纸、过氧化氢溶液、稀硫酸(用其中的一种或多种均可。)
| 实验方法 | 实验现象及结论 |
d.电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少 。
。
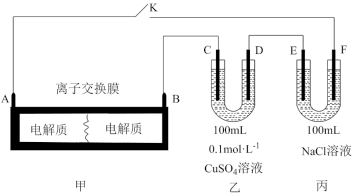
(1)装置甲的A电极为电池的_______ 极,电解质中的 从离子交换膜的
从离子交换膜的_________  填“左侧”或“右侧”,下同
填“左侧”或“右侧”,下同 向离子交换膜的
向离子交换膜的_________ 迁移;B电极的电极反应式为_______ 。
(2)装置乙D电极析出的气体是___________ ,体积为___________  标准状况
标准状况 。
。
(3)若将装置丙中的NaCl溶液换成 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。
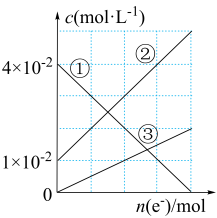
①图中②表示的是__________  填金属离子符号
填金属离子符号 的变化曲线。
的变化曲线。
②反应结束后,若用 溶液沉淀丙装置溶液中的金属阳离子
溶液沉淀丙装置溶液中的金属阳离子 设溶液体积为
设溶液体积为 ,则至少需要
,则至少需要 溶液
溶液________ mL。
(4)该小组运用工业上离子交换膜法制烧碱的原理,用如图所示装置电解 溶液。
溶液。
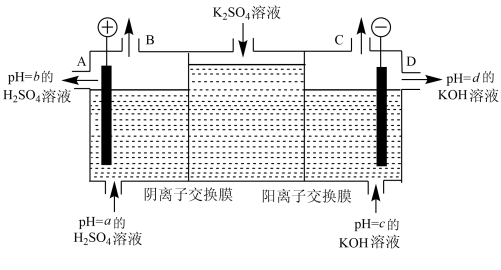
①该电解槽的阳极反应式为_____________ ,通过阴离子交换膜的离子数_______  填“
填“ ”“
”“ ”或“
”或“ ”
” 通过阳离子交换膜的离子数。
通过阳离子交换膜的离子数。
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为_________ 。
③电解一段时间后,B口与C口产生气体的质量比为__________________ 。
 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少 。
。
(1)装置甲的A电极为电池的
 从离子交换膜的
从离子交换膜的 填“左侧”或“右侧”,下同
填“左侧”或“右侧”,下同 向离子交换膜的
向离子交换膜的(2)装置乙D电极析出的气体是
 标准状况
标准状况 。
。(3)若将装置丙中的NaCl溶液换成
 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。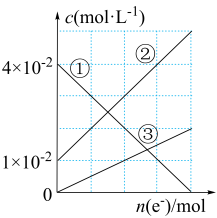
①图中②表示的是
 填金属离子符号
填金属离子符号 的变化曲线。
的变化曲线。②反应结束后,若用
 溶液沉淀丙装置溶液中的金属阳离子
溶液沉淀丙装置溶液中的金属阳离子 设溶液体积为
设溶液体积为 ,则至少需要
,则至少需要 溶液
溶液(4)该小组运用工业上离子交换膜法制烧碱的原理,用如图所示装置电解
 溶液。
溶液。
①该电解槽的阳极反应式为
 填“
填“ ”“
”“ ”或“
”或“ ”
” 通过阳离子交换膜的离子数。
通过阳离子交换膜的离子数。②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为
③电解一段时间后,B口与C口产生气体的质量比为
您最近一年使用:0次



