请同学们仔细思考并回答下列问题:
(1)过氧化钠与二氧化碳反应的化学方程式为___________ ;39g过氧化钠完全反应,转移的电子数为___________ ,生成___________ L(换算成标准状况下)氧气。
(2) 与
与___________  所含的原子数目相等。
所含的原子数目相等。
(3)如图所示,将等质量的气体m和气体n充入带有活塞(可自由移动且厚度不计)的密闭容器中,最终活塞停留在图示位置,则m与n的摩尔质量之比为___________ 。

(4)实验室可用 固体与浓盐酸常温下反应制备氯气。
固体与浓盐酸常温下反应制备氯气。

该反应的氧化剂为___________ ,写出配平后的上述反应的化学方程式:___________ 。
(1)过氧化钠与二氧化碳反应的化学方程式为
(2)
 与
与 所含的原子数目相等。
所含的原子数目相等。(3)如图所示,将等质量的气体m和气体n充入带有活塞(可自由移动且厚度不计)的密闭容器中,最终活塞停留在图示位置,则m与n的摩尔质量之比为

(4)实验室可用
 固体与浓盐酸常温下反应制备氯气。
固体与浓盐酸常温下反应制备氯气。
该反应的氧化剂为
更新时间:2023-11-17 07:39:41
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】概括归纳是化学学习的一种重要方法,回答下列问题。
(1)依据物质的性质分析: 、
、 、
、 、
、 均属于
均属于_______ (填“酸性氧化物”、“碱性氧化物”或“两性氧化物”)。下列物质均能与它们发生反应的是_______ (填字母)。
a.水 b.盐酸 c.氢氧化钠
(2)在一定条件下,1mol不同物质的体积如下表所示。
分析表中数据,可得出的结论是_______ (写出两条即可)。
(3)短周期部分元素的原子半径随原子序数递增呈现周期性的变化,如图所示。
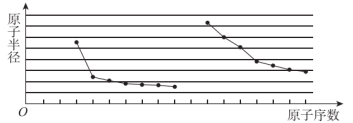
分析图中曲线,可得出的结论是_______ 。
(1)依据物质的性质分析:
 、
、 、
、 、
、 均属于
均属于a.水 b.盐酸 c.氢氧化钠
(2)在一定条件下,1mol不同物质的体积如下表所示。
| 化学式 | H2 | O2 | CO2 | |
| 体积 | 0℃、101kPa | 22.4L | 22.4L | 22.3L |
| 20℃、101kPa | 24.0L | 24.0L | 23.9L | |
| 0℃、202kPa | 11.2L | 11.2L | 11.2L | |
(3)短周期部分元素的原子半径随原子序数递增呈现周期性的变化,如图所示。

分析图中曲线,可得出的结论是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)4gH2与24.5L(常温常压)CO2相比,所含分子数目多的是____ ;各1.5 mol上述两种气体相比较,质量大的是_____
(2)在温度和压强相等的条件下,氧气和氢气的密度比为____ ,质量相等时的体积比为____ ,体积相等时的物质的量之比为____ 。
(2)在温度和压强相等的条件下,氧气和氢气的密度比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氮及其化合物在生活和生产等方面有重要的应用。回答下列问题:
(1)下列含氮物质中属于盐的是_____ ,属于非电解质的是_____ 。
A.NH3 B.HNO3 C.NaNO3 D.N2
(2)写出KNO3的电离方程式:_______________ 。
(3)0.3 mol的N2H4气体和0.1molNH3气体,它们在同温、同压下的体积比是______ ;若N2H4和NH3两种气体具有相同的氢原子数目,则n(N2H4):n(NH3)=______ .
(4)将____ g NaNO3溶于水配成200mL溶液,所得溶液溶质的物质量浓度为0.2 mol·L-1。
(1)下列含氮物质中属于盐的是
A.NH3 B.HNO3 C.NaNO3 D.N2
(2)写出KNO3的电离方程式:
(3)0.3 mol的N2H4气体和0.1molNH3气体,它们在同温、同压下的体积比是
(4)将
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】简答题
(1)含1.0molFe3+的Fe2(SO4)3中所含SO 的物质的量是
的物质的量是_______ 。
(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是_______ 。
(3)某混合溶液中含有Na+、Al3+、Cl-、SO 测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为_______ 。
(4)黑火药是我国古代四大发明之一,其化学反应方程式为: 。
。
①上述反应所涉及到的物质中属于非电解质的是_______ ;
②上述反应中被氧化的元素是_______ (填元素符号);
(1)含1.0molFe3+的Fe2(SO4)3中所含SO
 的物质的量是
的物质的量是(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是
(3)某混合溶液中含有Na+、Al3+、Cl-、SO
 测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为(4)黑火药是我国古代四大发明之一,其化学反应方程式为:
 。
。①上述反应所涉及到的物质中属于非电解质的是
②上述反应中被氧化的元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】完成下列填空:
(1)1.204×1024个氯气分子的物质的量是___________ ,0.5mol的NH3中含有的电子数为___________ 。
(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为___________ 。
(3)3.1 g Na2X含有Na+0.1 mol,则 Na2X 的摩尔质量为___________ 。
(4)在标准状况下,CO和CO2的混合气体共 6.72 L,质量为 12 g,则混合气体的平均摩尔质量为___________ 。
(1)1.204×1024个氯气分子的物质的量是
(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为
(3)3.1 g Na2X含有Na+0.1 mol,则 Na2X 的摩尔质量为
(4)在标准状况下,CO和CO2的混合气体共 6.72 L,质量为 12 g,则混合气体的平均摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】将0.3molCu与足量的稀硝酸反应,被还原的硝酸为_______ mol,转移的电子数为_______ 个。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据下列物质的转化关系请完成下列空白。
C CO2
CO2 H2CO3
H2CO3 CaCO3
CaCO3 CO2
CO2
(1)转化反应中属于复分解反应的是_______ (填反应序号,下同),氧化还原 反应的是_______ 。
(2)上述氧化还原反应中氧化剂的名称是_______ ,若标准状况下生成11.2L CO2 ,则转移 电子数为_______ ,生成还原产物的质量为_______ 。
(3)写出反应③的离子方程式_______ 。
C
 CO2
CO2 H2CO3
H2CO3 CaCO3
CaCO3 CO2
CO2(1)转化反应中属于复分解反应的是
(2)上述氧化还原反应中氧化剂的名称是
(3)写出反应③的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】用NA表示阿伏加德罗常数,判断下列说法是否正确。
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求填空
(1)铁屑加入硝酸银溶液中反应的离子方程式为______ 。
(2)醋酸(CH3COOH)与烧碱溶液反应的离子方程式为______ 。
(3)NaHSO4是一种______ (填“酸、碱、盐”),向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性时,该反应的离子方程式为_____ 。
(4)实验室制备少量Fe(OH)3胶体的化学方程式为______ 。
(5)配平下列方程式:____SO32-+___IO3-+___H+=___SO42-+___I2+___H2O,______
(6)一定条件下,RO3n-和氟气可发生如下反应:RO3n-+F2+2OH-=RO4-+2F-+H2O,从而可知在RO3n-中,元素R的化合价是____ 。
(1)铁屑加入硝酸银溶液中反应的离子方程式为
(2)醋酸(CH3COOH)与烧碱溶液反应的离子方程式为
(3)NaHSO4是一种
(4)实验室制备少量Fe(OH)3胶体的化学方程式为
(5)配平下列方程式:____SO32-+___IO3-+___H+=___SO42-+___I2+___H2O,
(6)一定条件下,RO3n-和氟气可发生如下反应:RO3n-+F2+2OH-=RO4-+2F-+H2O,从而可知在RO3n-中,元素R的化合价是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Ⅰ. 可用作清洁剂、防腐剂等。请按要求回答下列问题:
可用作清洁剂、防腐剂等。请按要求回答下列问题:
(1)下列关于 的说法正确的是______。
的说法正确的是______。
(2)将 溶液滴加到
溶液滴加到 溶液中至溶液呈中性时,发生反应的离子方程式为
溶液中至溶液呈中性时,发生反应的离子方程式为______ 。
Ⅱ.请按要求回答下列问题:
(3) 溶液与
溶液与 溶液反应的离子方程为
溶液反应的离子方程为______ 。
(4)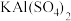 的电离方程式
的电离方程式______ 。
(5)工业上制取 用
用 与C、
与C、 在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是
在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是______ 。
(6)反应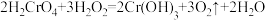 中
中 的变化
的变化
①该反应的氧化产物是______ (填化学式)。
②在该反应方程式中用单线桥法标明电子转移的方向和数目______ 。
 可用作清洁剂、防腐剂等。请按要求回答下列问题:
可用作清洁剂、防腐剂等。请按要求回答下列问题:(1)下列关于
 的说法正确的是______。
的说法正确的是______。A. 固体能导电 固体能导电 |
B. 溶液的导电性一定强于 溶液的导电性一定强于 溶液 溶液 |
C. 属于强电解质 属于强电解质 |
D. 溶液显酸性 溶液显酸性 |
 溶液滴加到
溶液滴加到 溶液中至溶液呈中性时,发生反应的离子方程式为
溶液中至溶液呈中性时,发生反应的离子方程式为Ⅱ.请按要求回答下列问题:
(3)
 溶液与
溶液与 溶液反应的离子方程为
溶液反应的离子方程为(4)
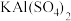 的电离方程式
的电离方程式(5)工业上制取
 用
用 与C、
与C、 在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是
在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是(6)反应
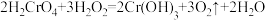 中
中 的变化
的变化
①该反应的氧化产物是
②在该反应方程式中用单线桥法标明电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题
(1)现有下列物质:①干冰②氨水③Na2CO3晶体 ④纯醋酸⑤ FeCl3溶液 ⑥铜 ⑦ Fe(OH)3胶体 ⑧蔗糖,其中属于电解质的是___________ ,
(2)写出FeCl3的电离方程式:___________ ,
(3)写出Na2CO3(aq)与稀盐酸反应的离子方程式:___________ ,
(4)胶体是一种常见的分散系,回答下列问题。
①向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为___________ 。
②区分胶体和溶液常用的方法叫___________ 。
(1)现有下列物质:①干冰②氨水③Na2CO3晶体 ④纯醋酸⑤ FeCl3溶液 ⑥铜 ⑦ Fe(OH)3胶体 ⑧蔗糖,其中属于电解质的是
(2)写出FeCl3的电离方程式:
(3)写出Na2CO3(aq)与稀盐酸反应的离子方程式:
(4)胶体是一种常见的分散系,回答下列问题。
①向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为
②区分胶体和溶液常用的方法叫
您最近一年使用:0次



