(1) 2 mol H2SO4中约含 ___________ 个H2SO4分子
(2)0.2 mol的Al2(SO4)3 中含___________ mol Al3+
(3)2 mol NaOH的质量是___________ 克
(4)在标准状况下,6.72 L CO2的物质的量是___________ mol
(5)2.7克铝与足量NaOH溶液完全反应,放出(标准状况下)氢气___________ L
(2)0.2 mol的Al2(SO4)3 中含
(3)2 mol NaOH的质量是
(4)在标准状况下,6.72 L CO2的物质的量是
(5)2.7克铝与足量NaOH溶液完全反应,放出(标准状况下)氢气
更新时间:2021/02/01 19:11:57
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某双原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA,则:
(1)该气体的物质的量为_______ mol;
(2)该气体在标准状况下的体积为_______ L;
(3)该气体在标准状况下的密度为_______ g/L;
(4)该气体所含原子总数为_______ 个;
(1)该气体的物质的量为
(2)该气体在标准状况下的体积为
(3)该气体在标准状况下的密度为
(4)该气体所含原子总数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】根据所学知识,回答下列问题
(1)1mol H2SO4中含_______ 个氧原子;同温同压下,物质的量相等的CO和CO2中,分子个数之比为_______ ;50mL0.1mol/L Na2CO3溶液中Na+的物质的量浓度为_______ 。
(2)化学是一门实用性很强的科学,请根据题意填空。
钠有多种化合物,其中俗称“纯碱”的是_______ (填“Na2CO3”或“NaHCO3”);铁有多种氧化物,其中为黑色且具有磁性的是_______ (填“Fe2O3”或“Fe3O4);漂白粉的有效成分是_______ (填“CaCl2”或“Ca(ClO)2);日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了_______ (填“Al2O3”或“Al(OH)3”)。
(1)1mol H2SO4中含
(2)化学是一门实用性很强的科学,请根据题意填空。
钠有多种化合物,其中俗称“纯碱”的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】现有14.4gCO和CO2的混合气体,在标准状况下所占的体积约为8.96L。回答下列问题:
(1)该混合气体的平均摩尔质量:___________ 。
(2)混合气体中碳原子的个数:___________ 。(用NA表示阿伏加德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。
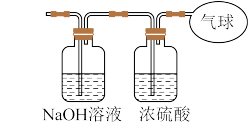
①气球中收集到的气体摩尔质量:___________ ;
②标准状况下气球中收集到的气体的体积为___________ ;
③气球中收集到的气体的电子总数___________ 。(用NA表示阿伏加德罗常数的值)
(1)该混合气体的平均摩尔质量:
(2)混合气体中碳原子的个数:
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体摩尔质量:
②标准状况下气球中收集到的气体的体积为
③气球中收集到的气体的电子总数
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】利用相关知识填空。
(1)标准状况下 11.2LNH3中含电子数为___________ 。
(2)等质量的SO2和SO3物质的量之比是___________ ;所含的氧原子个数之比是___________ 。
(3)4.8gCH4中所含氢原子数与___________ g 水所含氢原子数相等。
(4)已知A 是一种金属,82 gA(NO3)2中含有6.02 × 1023个硝酸根离子,则该硝酸盐的摩尔质量为___________ 。
(5)标况下,一定量的N2与 22.4LCO 所含电子的物质的量相等,则N2的质量是___________ 。
(6)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为____ 。若此时压强为101 kPa,则温度___________ 0℃(填“高于”“低于”或“等于”)。
(1)标准状况下 11.2LNH3中含电子数为
(2)等质量的SO2和SO3物质的量之比是
(3)4.8gCH4中所含氢原子数与
(4)已知A 是一种金属,82 gA(NO3)2中含有6.02 × 1023个硝酸根离子,则该硝酸盐的摩尔质量为
(5)标况下,一定量的N2与 22.4LCO 所含电子的物质的量相等,则N2的质量是
(6)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)标准状况下,3.4g NH3的体积为_______ L,0.1 molH2S共有_______ 个H;同质量的NH3和H2S中分子个数比为_________ ;
(2)在同温同压条件下,质量相同的CO2 、NH3、H2S、 Cl2 四种气体中,体积最小的是_________ 。
(3)1.6g某气体含有3.01×1022个分子,该气体的摩尔质量为_______ 。
(1)标准状况下,3.4g NH3的体积为
(2)在同温同压条件下,质量相同的CO2 、NH3、H2S、 Cl2 四种气体中,体积最小的是
(3)1.6g某气体含有3.01×1022个分子,该气体的摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)3.6 g H2O的物质的量是____ ,含有水分子的数目是_____ ,含有氢原子的物质的量是_____ 。
(2)1.5molCO2和______ g CH4在标准状况下占有相同的体积,其体积为________ 。
(3)在标准状况下,100mL某气体的质量为0.179g,该气体的相对分子质量为________ 。
(4)现有mg某X2气体,它的摩尔质量为M g/mol,阿伏加 德罗常数用NA表示,则:该气体的物质的量为______ mol;一个X原子的质量为_______ g;该气体在标准状况下的体积为______ L。
(2)1.5molCO2和
(3)在标准状况下,100mL某气体的质量为0.179g,该气体的相对分子质量为
(4)现有mg某X2气体,它的摩尔质量为M g/mol,阿伏加 德罗常数用NA表示,则:该气体的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】3.01×1023个OH-的物质的量是___ ,质量是___ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为________ ,R的相对原子质量为________ 。含R的质量为1.6 g的Na2R,含Na+的个数为________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】现有下列物质:
①金属钠②碳酸氢钠固体③过氧化钠固体④ 胶体⑤液氯⑥澄清石灰水⑦纯醋酸⑧盐酸⑨酒精
胶体⑤液氯⑥澄清石灰水⑦纯醋酸⑧盐酸⑨酒精
回答下列问题:
(1)以上物质中属于电解质的是______ 。(填序号)
(2)物质②溶于水的电离方程式______ 。
(3)写出实验室制备④的化学方程式______ 。
(4)将②的水溶液,逐滴加入⑥中至沉淀量最大时的离子方程式______ 。
(5)一定量③与水完全反应,若产生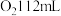 (标准状况),则反应过程中转移的电子数目为
(标准状况),则反应过程中转移的电子数目为______ 。若反应后溶液的体积为 ,则反应后所得溶液的物质的量浓度为
,则反应后所得溶液的物质的量浓度为______ 。
①金属钠②碳酸氢钠固体③过氧化钠固体④
 胶体⑤液氯⑥澄清石灰水⑦纯醋酸⑧盐酸⑨酒精
胶体⑤液氯⑥澄清石灰水⑦纯醋酸⑧盐酸⑨酒精回答下列问题:
(1)以上物质中属于电解质的是
(2)物质②溶于水的电离方程式
(3)写出实验室制备④的化学方程式
(4)将②的水溶液,逐滴加入⑥中至沉淀量最大时的离子方程式
(5)一定量③与水完全反应,若产生
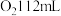 (标准状况),则反应过程中转移的电子数目为
(标准状况),则反应过程中转移的电子数目为 ,则反应后所得溶液的物质的量浓度为
,则反应后所得溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】向Ba(OH)2溶液中先滴加一定量CuSO4溶液,直至沉淀质量为m克,再不断滴加H2SO4溶液。整个过程中,产生沉淀的质量与加入溶液的质量关系如图所示。
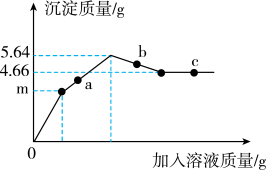
(1)a点对应溶液pH___________ (选填“>”、“=”或“<”)7。
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是___________ 。
(3)通过计算确定m的值___________ 。(写出计算过程)

(1)a点对应溶液pH
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是
(3)通过计算确定m的值
您最近一年使用:0次
【推荐3】硝酸是重要的化工原料,工业上用氨催化氧化法生产硝酸,反应如下:
①氧化炉:4NH3+5O2=4NO+6H2O
②吸收塔:4NO+3O2+2H2O=4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80。完成下列计算:
(1)1mol NH3完全转化为NO至少需要空气______ mol。工业上先将氨气和空气混合好,在氧化炉反应后直接通入吸收塔中用冷水吸收,为了确保吸收效果,第②步反应要求氧气至少过量20%,计算起始时空气与氨气的体积比至少为______
(2)硝酸工业产生的氮氧化物尾气(NO和NO2),可用烧碱吸收,反应如下:
①NO+NO2+2NaOH=2NaNO2+H2O
②2NO2+2NaOH=NaNO3+NaNO2+H2O
现有含0.5mol氮氧化物的尾气,用8mol/L的NaOH溶液完全吸收,吸收后的溶液中c(OH﹣):c(NO2﹣):c(NO3﹣)=5:4:1。所用NaOH溶液的体积为______ mL。若将尾气中NO与NO2的平均组成记为NOx,则x=______
(3)工业上用硝酸与氨气反应制取硝酸铵:HNO3+NH3=NH4NO3,反应时NH3的吸收率为97%,硝酸的利用率为98%。在用氨气制取硝酸时,氨气的利用率为90%。计算生产80吨的硝酸铵共需氨气__ 吨?(保留1位小数)
①氧化炉:4NH3+5O2=4NO+6H2O
②吸收塔:4NO+3O2+2H2O=4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80。完成下列计算:
(1)1mol NH3完全转化为NO至少需要空气
(2)硝酸工业产生的氮氧化物尾气(NO和NO2),可用烧碱吸收,反应如下:
①NO+NO2+2NaOH=2NaNO2+H2O
②2NO2+2NaOH=NaNO3+NaNO2+H2O
现有含0.5mol氮氧化物的尾气,用8mol/L的NaOH溶液完全吸收,吸收后的溶液中c(OH﹣):c(NO2﹣):c(NO3﹣)=5:4:1。所用NaOH溶液的体积为
(3)工业上用硝酸与氨气反应制取硝酸铵:HNO3+NH3=NH4NO3,反应时NH3的吸收率为97%,硝酸的利用率为98%。在用氨气制取硝酸时,氨气的利用率为90%。计算生产80吨的硝酸铵共需氨气
您最近一年使用:0次



