回答下列问题:
(1)标准状况下,3.4g NH3的体积为_______ L,0.1 molH2S共有_______ 个H;同质量的NH3和H2S中分子个数比为_________ ;
(2)在同温同压条件下,质量相同的CO2 、NH3、H2S、 Cl2 四种气体中,体积最小的是_________ 。
(3)1.6g某气体含有3.01×1022个分子,该气体的摩尔质量为_______ 。
(1)标准状况下,3.4g NH3的体积为
(2)在同温同压条件下,质量相同的CO2 、NH3、H2S、 Cl2 四种气体中,体积最小的是
(3)1.6g某气体含有3.01×1022个分子,该气体的摩尔质量为
更新时间:2021-10-28 08:22:00
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】0.5 mol SO2的质量是____ g,在标准状况下的体积为____ L;含________ 个氧原子。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
①分离饱和食盐水与沙子的混合物。____________ ;
②从硝酸钾和氯化钠的混合溶液中获得硝酸钾晶体。___________ ;
③分离CCl4(沸点为76. 75°C)和甲苯(沸点为110. 6°C)的互溶混合物。_____________ ;
④分离NaCl固体和单质碘固体的混合物。____________ 。
(2)47. 5g某二价金属的氯化物中含有1molCl-,则该金属氯化物的摩尔质量为_______ ;该金属的相对原子质量为_______
A.萃取 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
①分离饱和食盐水与沙子的混合物。
②从硝酸钾和氯化钠的混合溶液中获得硝酸钾晶体。
③分离CCl4(沸点为76. 75°C)和甲苯(沸点为110. 6°C)的互溶混合物。
④分离NaCl固体和单质碘固体的混合物。
(2)47. 5g某二价金属的氯化物中含有1molCl-,则该金属氯化物的摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】据报道,加利福尼亚大学的科研人员发现了世界上最强的酸,这种强酸的化学式是 。其中11个硼原子和1个碳原子排列成20面体,这是目前化合物中化学性质最为稳定的原子组合。请回答下列问题:用
。其中11个硼原子和1个碳原子排列成20面体,这是目前化合物中化学性质最为稳定的原子组合。请回答下列问题:用 表示阿伏加德罗常数的数值,那么
表示阿伏加德罗常数的数值,那么 该超强酸中含有的氯原子数目为
该超强酸中含有的氯原子数目为___________ ,若称取该超强酸 ,则其中含硼原子的数目为
,则其中含硼原子的数目为___________ 。
 。其中11个硼原子和1个碳原子排列成20面体,这是目前化合物中化学性质最为稳定的原子组合。请回答下列问题:用
。其中11个硼原子和1个碳原子排列成20面体,这是目前化合物中化学性质最为稳定的原子组合。请回答下列问题:用 表示阿伏加德罗常数的数值,那么
表示阿伏加德罗常数的数值,那么 该超强酸中含有的氯原子数目为
该超强酸中含有的氯原子数目为 ,则其中含硼原子的数目为
,则其中含硼原子的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题
(1)请填写下表:
(2)摩尔质量是指单位物质的量的物质所含有的质量。
①已知NH3的相对分子质量为17,则NH3的摩尔质量为___________ 。
②NA为阿伏加德罗常数的值,已知ag某气体中含分子数为b,则该气体的摩尔质量为___________ 。
③已知一个铁原子的质量为bg,则铁的摩尔质量为___________ (用含b的代数式表示)
(1)请填写下表:
| 物质 | 摩尔质量 | 物质的量 | 质量 | 分子或离子数目 |
 | 64g/mol | 2mol | ① | ② |
 | 96g/mol | ③ | ④ | 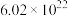 |
 | 32g/mol | ⑤ | 8.0g | ⑥ |
①已知NH3的相对分子质量为17,则NH3的摩尔质量为
②NA为阿伏加德罗常数的值,已知ag某气体中含分子数为b,则该气体的摩尔质量为
③已知一个铁原子的质量为bg,则铁的摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】计算。
(1)6.02×1023个氢氧根离子的物质的量是___________ mol,其摩尔质量为___________ 。
(2)3.01×1023个H2O的物质的量为___________ mol,其中,所有的原子的物质的量为___________ mol。
(3)1.204×1023个 的物质的量为
的物质的量为___________ mol,质量为_________ g。
(4)等质量的SO2和O2物质的量之比为___________ ,分子数之比为___________ ,原子数之比为___________ ,摩尔质量之比为___________ 。
(1)6.02×1023个氢氧根离子的物质的量是
(2)3.01×1023个H2O的物质的量为
(3)1.204×1023个
 的物质的量为
的物质的量为(4)等质量的SO2和O2物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)0.3mol NH3分子中所含原子数与___________ mol H2O分子中所含原子数相等。
(2)含有 NA个氦原子的氦气在标准状况下的体积约为___________ L
(3)物质的量浓度相同时,碳酸钠溶液的pH比碳酸氢钠的___________ (填“大”或“小”)
(4)氢氧化钡与稀硫酸反应的离子方程式___________ 。
(1)0.3mol NH3分子中所含原子数与
(2)含有 NA个氦原子的氦气在标准状况下的体积约为
(3)物质的量浓度相同时,碳酸钠溶液的pH比碳酸氢钠的
(4)氢氧化钡与稀硫酸反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】森林是大自然的清洁器,一亩森林一昼夜可吸收66kg二氧化碳,呼出48kg氧气,即在标准状况下吸收__________ L二氧化碳,呼出___________ mol氧气。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】利用相关知识填空。
(1)标准状况下11.2L NH3中含__ 个氨分子。
(2)等质量的SO2和SO3物质的量之比是___ ;所含的氧原子个数之比是__ 。
(3)12.4g Na2R含Na+0.4mol,则Na2R的摩尔质量为__ 。
(1)标准状况下11.2L NH3中含
(2)等质量的SO2和SO3物质的量之比是
(3)12.4g Na2R含Na+0.4mol,则Na2R的摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】简答题
(1)含1.0molFe3+的Fe2(SO4)3中所含SO 的物质的量是
的物质的量是_______ 。
(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是_______ 。
(3)某混合溶液中含有Na+、Al3+、Cl-、SO 测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为_______ 。
(4)黑火药是我国古代四大发明之一,其化学反应方程式为: 。
。
①上述反应所涉及到的物质中属于非电解质的是_______ ;
②上述反应中被氧化的元素是_______ (填元素符号);
(1)含1.0molFe3+的Fe2(SO4)3中所含SO
 的物质的量是
的物质的量是(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是
(3)某混合溶液中含有Na+、Al3+、Cl-、SO
 测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为(4)黑火药是我国古代四大发明之一,其化学反应方程式为:
 。
。①上述反应所涉及到的物质中属于非电解质的是
②上述反应中被氧化的元素是
您最近一年使用:0次



