北京时间2022年12月4日20时09分,神舟十四号载人飞船返回舱在东风着陆场成功着陆。搭载神舟十四号载人飞船的是长征二号F遥十四运载火箭。
燃料主要有:①煤油 ②液氢 ③肼( ) ④固态铝粉
) ④固态铝粉
氧化剂主要有:⑤液氧 ⑥ ⑦高氯酸铵(
⑦高氯酸铵( )
)
(1)16g肼中含有H原子数目约为___________ 个。
(2)同温同压下,氧气与氢气的密度之比为___________ 。
(3)飞船以铝粉与高氨酸铵的混合物为固体燃料,其中高氯酸铵发生分解反应生成: 、
、 、
、 、和
、和 。请写出该反应的化学方程式:
。请写出该反应的化学方程式:___________ ,其中被氧化的元素是______ ,还原产物是______ 。
(4)空间站中可利用过氧化钠与人体代谢的 、
、 反应制备呼吸必需的
反应制备呼吸必需的 。过氧化钠的颜色为
。过氧化钠的颜色为_______ ,其中阴离子与阳离子的个数比为______ 。写出 与
与 反应的化学方程式
反应的化学方程式_______ 。在25℃和101 的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为_______ L,转移电子数目为_______ 个。
燃料主要有:①煤油 ②液氢 ③肼(
 ) ④固态铝粉
) ④固态铝粉氧化剂主要有:⑤液氧 ⑥
 ⑦高氯酸铵(
⑦高氯酸铵( )
)(1)16g肼中含有H原子数目约为
(2)同温同压下,氧气与氢气的密度之比为
(3)飞船以铝粉与高氨酸铵的混合物为固体燃料,其中高氯酸铵发生分解反应生成:
 、
、 、
、 、和
、和 。请写出该反应的化学方程式:
。请写出该反应的化学方程式:(4)空间站中可利用过氧化钠与人体代谢的
 、
、 反应制备呼吸必需的
反应制备呼吸必需的 。过氧化钠的颜色为
。过氧化钠的颜色为 与
与 反应的化学方程式
反应的化学方程式 的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
更新时间:2023-12-23 07:09:06
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有20g由2H和16O组成的水分子,其中含质子数为__________ ,中子数为_________ ,电子数为__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请根据物质的量的相关概念和公式,完成下列各题:
(1) 个
个 分子中共含有
分子中共含有___________ 个质子。
(2)4.9g 中含有
中含有___________ molS原子。
(3)含2.6 个电子的Al的质量为
个电子的Al的质量为___________ g。
(4)32g 完全燃烧产生标准状况下的CO2的体积为
完全燃烧产生标准状况下的CO2的体积为___________ L。
(5)等质量的 和
和 含有的原子数之比为
含有的原子数之比为________ ,氧原子数之比为___________ 。
(1)
 个
个 分子中共含有
分子中共含有(2)4.9g
 中含有
中含有(3)含2.6
 个电子的Al的质量为
个电子的Al的质量为(4)32g
 完全燃烧产生标准状况下的CO2的体积为
完全燃烧产生标准状况下的CO2的体积为(5)等质量的
 和
和 含有的原子数之比为
含有的原子数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】判断正误:
1.常温常压下,3.2gO2所含的原子数为0.2NA。(_______)
2.标准状况下,18gH2O所含的氧原子数目为NA。(_______)
3.室温下,1molCH4中含有5NA原子。(_______)
4.常温常压下,1molCO2与SO2的混合气体中含氧原子数为2NA。(_______)
5.2g石墨晶体中,含有的质子数目为6NA。(_______)
6.2molSO2和1molO2在一定条件下充分反应后,混合物的分子数为2NA。(_______)
7.密闭容器中2amolNO与amolO2充分反应,产物的分子数为2aNA。(_______)
8.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA。(_______)
9.1L0.1mol·L-1的氨水中有NA个NH 。(_______)
。(_______)
10.向含4molHCl的浓盐酸中,加入足量的MnO2,加热,充分反应后,生成NA个Cl2。(_______)
11.用含有1molFeCl3的溶液充分反应后得的Fe(OH)3胶体中含有NA个Fe(OH)3胶粒。(_______)
1.常温常压下,3.2gO2所含的原子数为0.2NA。(_______)
2.标准状况下,18gH2O所含的氧原子数目为NA。(_______)
3.室温下,1molCH4中含有5NA原子。(_______)
4.常温常压下,1molCO2与SO2的混合气体中含氧原子数为2NA。(_______)
5.2g石墨晶体中,含有的质子数目为6NA。(_______)
6.2molSO2和1molO2在一定条件下充分反应后,混合物的分子数为2NA。(_______)
7.密闭容器中2amolNO与amolO2充分反应,产物的分子数为2aNA。(_______)
8.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA。(_______)
9.1L0.1mol·L-1的氨水中有NA个NH
 。(_______)
。(_______)10.向含4molHCl的浓盐酸中,加入足量的MnO2,加热,充分反应后,生成NA个Cl2。(_______)
11.用含有1molFeCl3的溶液充分反应后得的Fe(OH)3胶体中含有NA个Fe(OH)3胶粒。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下列叙述中完全正确的是______
①常温常压下,1 mol甲基(—CH3)所含的电子数为10NA
②1mol含8个碳原子的某烃分子,最多形成8mol碳碳单键
③在标准状况下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
④16.9 g 过氧化钡(BaO2)固体中阴、阳离子总数为0.2NA
⑤1 mol C10H22分子中共价键总数为31 NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2NA
⑦室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA
⑧标准状况下,测得一定量的铜与浓硝酸反应后生成22.4 L的气体,则被还原的硝酸的分子数一定等于NA
⑨精炼铜过程中阳极减轻6.4g时,电路中转移电子数是0.2NA
⑩常温常压下,2.24L四氯化碳中所含氯原子数大于0.4NA
⑪在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移4NA个电子
①常温常压下,1 mol甲基(—CH3)所含的电子数为10NA
②1mol含8个碳原子的某烃分子,最多形成8mol碳碳单键
③在标准状况下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
④16.9 g 过氧化钡(BaO2)固体中阴、阳离子总数为0.2NA
⑤1 mol C10H22分子中共价键总数为31 NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2NA
⑦室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA
⑧标准状况下,测得一定量的铜与浓硝酸反应后生成22.4 L的气体,则被还原的硝酸的分子数一定等于NA
⑨精炼铜过程中阳极减轻6.4g时,电路中转移电子数是0.2NA
⑩常温常压下,2.24L四氯化碳中所含氯原子数大于0.4NA
⑪在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移4NA个电子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在反应2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O中,氧化剂是________ ,氧化产物是________ ,氧化产物与还原产物的物质的量之比为________ ,被氧化与未被氧化的HCl的质量之比为________ ,若有73 g HCl被氧化,电子转移的总数为________ (用NA表示阿伏加德罗),标准状况生成Cl2的体积为________ L。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】业内人士预测,2023年对中国汽车的出口量将历史性的超过日本,成为世界第一、中国电动汽车技术处于世界领先地位。比亚迪公司充电电池全线搭载了刀片电池,刀片电池具有续航里程高,安全性好的优点。刀片电池的正极材料使用了磷酸铁锂(LiFePO4)。磷酸铁锂(LiFePO4)由Li2CO3、C6H12O6和FePO4在高温条件下制备。
(1)LiFePO4中的化合物态的铁价电子排布式为___________ ,铁元素在元素周期表中的位置为___________ 。
(2)C6H12O6在反应中表现出___________ (填氧化性、还原性),每生成27 g C6H12O6参与反应,转移电子数目为___________ 。
(3)CO2的电子式为___________ ,Li2CO3中负离子的立体结构为___________ 。
(4)电动汽车相对于燃油动力汽车更加环保,原因是___________ 。

(1)LiFePO4中的化合物态的铁价电子排布式为
(2)C6H12O6在反应中表现出
(3)CO2的电子式为
(4)电动汽车相对于燃油动力汽车更加环保,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症。硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:

实验Ⅲ:标定Na2S2O3溶液的浓度
称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+ +14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2
+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2 =2I-+
=2I-+ ,三次消耗Na2S2O3溶液的平均体积为25.00mL,则所标定的硫代硫酸钠溶液的浓度为
,三次消耗Na2S2O3溶液的平均体积为25.00mL,则所标定的硫代硫酸钠溶液的浓度为_______ mol∙L-1
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:

实验Ⅲ:标定Na2S2O3溶液的浓度
称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+
 +14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2
+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2 =2I-+
=2I-+ ,三次消耗Na2S2O3溶液的平均体积为25.00mL,则所标定的硫代硫酸钠溶液的浓度为
,三次消耗Na2S2O3溶液的平均体积为25.00mL,则所标定的硫代硫酸钠溶液的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】金属切削加工废液中含有2%~5%的亚硝酸钠( )。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。
)。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。
(1)写出亚硝酸钠和氯化铵反应的化学方程式_________ 。
(2)第二步反应中,1mol亚硝酸铵完全分解,共有_________ mol电子转移。
 )。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。
)。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。(1)写出亚硝酸钠和氯化铵反应的化学方程式
(2)第二步反应中,1mol亚硝酸铵完全分解,共有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。含氯消毒剂在日常生产生活中有着广泛的用途。
(1)实验室除了可以用 和浓盐酸制氯气外,还可以利用如下反应制取氯气:
和浓盐酸制氯气外,还可以利用如下反应制取氯气: 。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为
。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为___________ g,其中被氧化的HCl的物质的量为___________ mol,反应过程中转移的电子数为___________  。
。
(2)二氧化氯(ClO2)是一种黄绿色的气体,可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用 和浓盐酸在一定温度下反应制得:
和浓盐酸在一定温度下反应制得: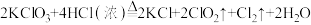 。
。
①该反应的氧化产物为___________ (填化学式)。
②在该反应中浓盐酸表现出来的性质是___________ (填标号)。
A.还原性 B.氧化性 C.酸性
③ 、
、 、
、 (还原产物为
(还原产物为 )、NaClO等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是
)、NaClO等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是___________ (填标号)。
A. B.
B. C.
C. D.NaClO
D.NaClO
(1)实验室除了可以用
 和浓盐酸制氯气外,还可以利用如下反应制取氯气:
和浓盐酸制氯气外,还可以利用如下反应制取氯气: 。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为
。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为 。
。(2)二氧化氯(ClO2)是一种黄绿色的气体,可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用
 和浓盐酸在一定温度下反应制得:
和浓盐酸在一定温度下反应制得: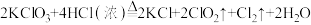 。
。①该反应的氧化产物为
②在该反应中浓盐酸表现出来的性质是
A.还原性 B.氧化性 C.酸性
③
 、
、 、
、 (还原产物为
(还原产物为 )、NaClO等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是
)、NaClO等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是A.
 B.
B. C.
C. D.NaClO
D.NaClO
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
(1)金属与水的反应
①Na的原子结构示意图是__________ 。
②钠与水反应的化学方程式是__________ 。
③钠与水的反应放出热量的现象是__________ 。
(2)钠失火时,可用不同的灭火剂灭火。如可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因__________ 。

(1)金属与水的反应
①Na的原子结构示意图是
②钠与水反应的化学方程式是
③钠与水的反应放出热量的现象是
(2)钠失火时,可用不同的灭火剂灭火。如可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求书写方程式:
(1)过氧化钠与CO2反应的化学方程式:__________________________________________
(2)镁条在二氧化碳中燃烧的化学方程式:________________________________________
(3)将少量硫酸铝溶液滴入足量NaOH溶液中的离子方程式:________________________
(4)铁与高温水蒸气反应的化学方程式:______________________________
(1)过氧化钠与CO2反应的化学方程式:
(2)镁条在二氧化碳中燃烧的化学方程式:
(3)将少量硫酸铝溶液滴入足量NaOH溶液中的离子方程式:
(4)铁与高温水蒸气反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下八种物质:
①石墨 ②CO2 ③稀盐酸 ④Ba(OH)2溶液 ⑤熔融KNO3 ⑥CaCO3固体 ⑦酒精(C2H5OH) ⑧NaHSO4溶液
(1)以上物质中能导电的是___________ 。(填写编号,下同)
(2)属于电解质的是___________ 。
(3)属于非电解质的是___________ 。
(4)将一小块金属钠投入水中,发生反应的离子方程式为___________ ,请回答:可观察到的实验现象正确的是___________ (填字母)。
a.钠沉到水底 b.钠熔成小球
c.小球四处游动 d.向反应后的溶液中滴加石蕊试剂,溶液变为红色
(5)在实验室中,通常将金属钠保存在___________ (填字母)。
a.水中 b.煤油中 c.四氯化碳中
(6)过氧化钠与二氧化碳反应,化学方程式:___________ 。
①石墨 ②CO2 ③稀盐酸 ④Ba(OH)2溶液 ⑤熔融KNO3 ⑥CaCO3固体 ⑦酒精(C2H5OH) ⑧NaHSO4溶液
(1)以上物质中能导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)将一小块金属钠投入水中,发生反应的离子方程式为
a.钠沉到水底 b.钠熔成小球
c.小球四处游动 d.向反应后的溶液中滴加石蕊试剂,溶液变为红色
(5)在实验室中,通常将金属钠保存在
a.水中 b.煤油中 c.四氯化碳中
(6)过氧化钠与二氧化碳反应,化学方程式:
您最近一年使用:0次



