在反应2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O中,氧化剂是________ ,氧化产物是________ ,氧化产物与还原产物的物质的量之比为________ ,被氧化与未被氧化的HCl的质量之比为________ ,若有73 g HCl被氧化,电子转移的总数为________ (用NA表示阿伏加德罗),标准状况生成Cl2的体积为________ L。
更新时间:2017-12-16 17:55:46
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】NA为阿伏加德罗常数的值。下列说法正确的是__________ 。
A.在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。反应转移电子为0.1NA
B.电解熔融CuCl2,阴极增重6.4g,外电路中通过电子的数目为0.10NA
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
D.电解熔融MgCl2制2.4gMg,电路中通过的电子数为0.1NA
E.3mol的NO2与H2O完全反应时转移的电子数为4NA
F.78gNa2O2与足量水完全反应,电子转移数为NA
G.4MnO +5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol[4MnO
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol[4MnO +5HCHO]完全反应转移的电子数为20NA
+5HCHO]完全反应转移的电子数为20NA
H.用电解粗铜的方法精炼铜,当电路中通过的电子数为NA时,阳极应有32gCu转化为Cu2+
A.在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。反应转移电子为0.1NA
B.电解熔融CuCl2,阴极增重6.4g,外电路中通过电子的数目为0.10NA
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
D.电解熔融MgCl2制2.4gMg,电路中通过的电子数为0.1NA
E.3mol的NO2与H2O完全反应时转移的电子数为4NA
F.78gNa2O2与足量水完全反应,电子转移数为NA
G.4MnO
 +5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol[4MnO
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol[4MnO +5HCHO]完全反应转移的电子数为20NA
+5HCHO]完全反应转移的电子数为20NAH.用电解粗铜的方法精炼铜,当电路中通过的电子数为NA时,阳极应有32gCu转化为Cu2+
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列填空:
(1)与标准状况下4.48LCO2中所含氧原子数目相同的水的质量是__ g;
(2)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为__ mol/L;
(3)氧化铜在高温下发生分解反应:4CuO 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为__ 。(阿伏加 德罗常数为NA)。
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了__ 性和__ 性,则56gFe参加反应时,被还原的HNO3为__ g。
(1)与标准状况下4.48LCO2中所含氧原子数目相同的水的质量是
(2)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为
(3)氧化铜在高温下发生分解反应:4CuO
 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)0.5 mol H2O的质量为____ ,含有______ 个原子。
(2)质量都是50 g的 HCl、CH4、N2三种气体中,原子数目最多的是气体是_______ ,在相同温度和相同压强条件下,密度最大的气体是__________ 。
(3)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为_______ 。
(4)实验室需用浓硫酸配制100 mL 1 mol•L-1的稀硫酸。可供选用的仪器有:
①量筒;②烧杯;③胶头滴管,还必须需要的玻璃仪器有________________ (写仪器名称)。
(5)一定条件下,RO 和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO
和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO 中,元素R的化合价是
中,元素R的化合价是_____ ,当有标准状况下8.96L Cl2被消耗时,反应中共转移电子物质的量为____ mol。
(2)质量都是50 g的 HCl、CH4、N2三种气体中,原子数目最多的是气体是
(3)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为
(4)实验室需用浓硫酸配制100 mL 1 mol•L-1的稀硫酸。可供选用的仪器有:
①量筒;②烧杯;③胶头滴管,还必须需要的玻璃仪器有
(5)一定条件下,RO
 和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO
和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO 中,元素R的化合价是
中,元素R的化合价是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】汽车尾气已成为城市空气的主要污染源,治理汽车尾气的SCR(选择性催化还原)和NSR (NOx储存还原)技术均可有效降低柴油发动机工作过程中排放的NOx。
(1)SCR工作原理
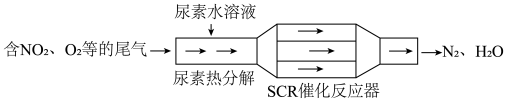
①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式是___________ 。
②反应器中NH3还原NO2的化学方程式是___________ 。
(2)NSR(NOx储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,通过BaO和Ba(NO3)2的相互转化实现NOx 的储存和还原。

①BaO吸收NO2的反应中氧化剂与还原剂的物质的量之比是___________ 。
②富燃条件下Pt表面反应的化学方程式是___________ 。
③若柴油中硫含量较高,在稀燃过程中,BaO吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因:___________ 。
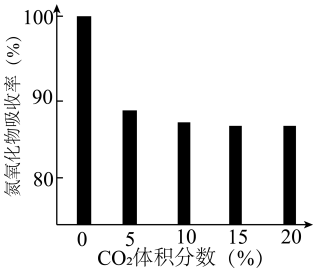
④研究发现:尾气中的CO2对BaO吸收氮氧化物有影响。一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如下图所示。则:一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因是___________ ;当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,原因可能是___________ 。
(1)SCR工作原理

①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式是
②反应器中NH3还原NO2的化学方程式是
(2)NSR(NOx储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,通过BaO和Ba(NO3)2的相互转化实现NOx 的储存和还原。

①BaO吸收NO2的反应中氧化剂与还原剂的物质的量之比是
②富燃条件下Pt表面反应的化学方程式是
③若柴油中硫含量较高,在稀燃过程中,BaO吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因:
④研究发现:尾气中的CO2对BaO吸收氮氧化物有影响。一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如下图所示。则:一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾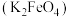 为暗紫色固体,可溶于水。结合所学知识回答相关问题:
为暗紫色固体,可溶于水。结合所学知识回答相关问题:
(1) 中铁元素的化合价是
中铁元素的化合价是___________ 价。
(2)制备高铁酸钠的主要反应为: (已知
(已知 中氧元素化合价为
中氧元素化合价为 价)。该反应中还原剂是
价)。该反应中还原剂是___________ (填化学式),若有 生成,转移电子的物质的量为
生成,转移电子的物质的量为___________  。
。
(3)某反应体系中有六种数粒: ,写出在碱性条件下,制备高铁酸钾的离子反应方程式
,写出在碱性条件下,制备高铁酸钾的离子反应方程式___________ 。
(4)在水处理过程中, 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮物聚沉。胶体区别于其他分散系的本质特征是
胶体,使水中悬浮物聚沉。胶体区别于其他分散系的本质特征是___________ 。
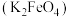 为暗紫色固体,可溶于水。结合所学知识回答相关问题:
为暗紫色固体,可溶于水。结合所学知识回答相关问题:(1)
 中铁元素的化合价是
中铁元素的化合价是(2)制备高铁酸钠的主要反应为:
 (已知
(已知 中氧元素化合价为
中氧元素化合价为 价)。该反应中还原剂是
价)。该反应中还原剂是 生成,转移电子的物质的量为
生成,转移电子的物质的量为 。
。(3)某反应体系中有六种数粒:
 ,写出在碱性条件下,制备高铁酸钾的离子反应方程式
,写出在碱性条件下,制备高铁酸钾的离子反应方程式(4)在水处理过程中,
 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮物聚沉。胶体区别于其他分散系的本质特征是
胶体,使水中悬浮物聚沉。胶体区别于其他分散系的本质特征是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO中Cl的化合价为______ ,有较强的______ (填氧化、还原)性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式______ 。
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为______ ;
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为______ ;
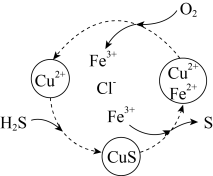
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有______ (写元素符号),Fe2+和Cu2+反应过程中起______ 作用,该图示的总反应的化学方程式为______ 。
(1)NaClO中Cl的化合价为
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________ ,还原产物是____________ 。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________ 价。
②以上反应中的氧化剂为________ ,当有1 mol CuI参与反应时,转移电子________ mol。
③标明上述反应电子转移的方向和数目。____________________________ 。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:______ ,MnO4-+Fe2++H+=Mn2++Fe3++H2O
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________ mol。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显
②以上反应中的氧化剂为
③标明上述反应电子转移的方向和数目。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在上海召开的第七届全球人类基因大会上,我国科学家第一次提出可以用砒霜(As2O3)来治疗早期幼粒白血病。
(1)完成并配平下列化学方程式:_____________
As2O3+ Zn+ H2SO4 → AsH3+ ZnSO4+ ______
(2)As2O3在上述反应中显示出来的性质是_____________ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.1 mol AsH3,则转移电子的物质的量为___________ mol。
(1)完成并配平下列化学方程式:
As2O3+ Zn+ H2SO4 → AsH3+ ZnSO4+ ______
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.1 mol AsH3,则转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究表明,我国酸雨区域占国土面积的40%以上,我国农业每年因遭受酸雨而造成经济损失高达15亿多元,酸雨的防治迫在眉睫。
(1) 是形成酸雨的主要物质之一,模仿示例图“
是形成酸雨的主要物质之一,模仿示例图“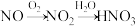 ”,画出由
”,画出由 形成硫酸型酸雨的可能的过程
形成硫酸型酸雨的可能的过程___________ 。
(2)某地降雨经检验,除 和
和 外,还含有
外,还含有 、
、 、
、 、
、 它们的浓度如下:
它们的浓度如下:
则该降雨的pH为___________ ,该降雨___________ (选填“是”或“不是”)酸雨。
(3)常温下,下列三种溶液:
①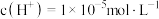 ②
②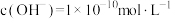 ③
③
按溶液酸性由强到弱的顺序排列为___________ 。
(4)为了减少酸雨产生的途径,你认为可采取的措施为___________。
(1)
 是形成酸雨的主要物质之一,模仿示例图“
是形成酸雨的主要物质之一,模仿示例图“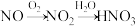 ”,画出由
”,画出由 形成硫酸型酸雨的可能的过程
形成硫酸型酸雨的可能的过程(2)某地降雨经检验,除
 和
和 外,还含有
外,还含有 、
、 、
、 、
、 它们的浓度如下:
它们的浓度如下:| 微粒 |  |  |  |  |  |  |
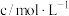 | ? |  |  |  | 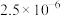 | 很小,可忽略 |
(3)常温下,下列三种溶液:
①
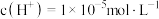 ②
②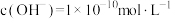 ③
③
按溶液酸性由强到弱的顺序排列为
(4)为了减少酸雨产生的途径,你认为可采取的措施为___________。
| A.把工厂烟囱造高 | B.在汽车排气管上安装汽车尾气催化转化器 |
| C.化石燃料脱硫 | D.在已酸化的土壤中加石灰 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】过渡元素在现代社会得到广泛应用。请回答下列问题
(1)ZnO、ZnS、Se共热可制备荧光材料ZnSe,同时产生了SO ,写出该反应的化学方程式:
,写出该反应的化学方程式:___ 。
(2)高锰酸钾因其强氧化性和溶液颜色变化明显而被用于物质的鉴定。请写出SO2与酸性高锰酸钾溶液反应的离子方程式:____ 。(高锰酸根离子的还原产物为Mn2+)
(3)高铁酸钠(Na2FeO4)是一种新型高效水处理剂,工业上采用碱性(NaOH)条件下,次氯酸钠溶液与氢氧化铁制备高铁酸钠。请写出其化学方程式:___ 。
(4)铬能够生成美丽多色的化合物。自然界中铬以铬铁矿Fe(CrO2)2形式存在,将铬铁矿和碳酸钠混合后在空气中煅烧,将其转化为易溶于水的物质。请完成其化学方程式:4Fe(CrO2)2+8Na2CO3+7O2=______+2Fe2O3+8CO2。____
(5)稀土金属包括____ 、钇和钪,在合金中加入稀土金属,能大大改善合金的性能,稀土金属被称为“冶金工业的维生素”。
(6)镍主要用于合金(可用来制造货币等)及用作催化剂(如氢化的催化剂),常见化合价为+2价、+3价。已知镍的氢氧化物均不溶于水。请写出碱性条件下Ni2+与溴水反应的离子方程式:____ 。
(1)ZnO、ZnS、Se共热可制备荧光材料ZnSe,同时产生了SO
 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)高锰酸钾因其强氧化性和溶液颜色变化明显而被用于物质的鉴定。请写出SO2与酸性高锰酸钾溶液反应的离子方程式:
(3)高铁酸钠(Na2FeO4)是一种新型高效水处理剂,工业上采用碱性(NaOH)条件下,次氯酸钠溶液与氢氧化铁制备高铁酸钠。请写出其化学方程式:
(4)铬能够生成美丽多色的化合物。自然界中铬以铬铁矿Fe(CrO2)2形式存在,将铬铁矿和碳酸钠混合后在空气中煅烧,将其转化为易溶于水的物质。请完成其化学方程式:4Fe(CrO2)2+8Na2CO3+7O2=______+2Fe2O3+8CO2。
(5)稀土金属包括
(6)镍主要用于合金(可用来制造货币等)及用作催化剂(如氢化的催化剂),常见化合价为+2价、+3价。已知镍的氢氧化物均不溶于水。请写出碱性条件下Ni2+与溴水反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请完成以下离子方程式的书写。
(1)二氧化锰与浓盐酸共热制氯气__________ 。
(2)鸡蛋壳溶于醋酸中_________ 。
(3)NaHSO4溶液与Ba(OH)2溶液反应后呈中性_________ 。
(4)弱酸环境下,高锰酸钾将Mn2+氧化为MnO2_________ 。
(1)二氧化锰与浓盐酸共热制氯气
(2)鸡蛋壳溶于醋酸中
(3)NaHSO4溶液与Ba(OH)2溶液反应后呈中性
(4)弱酸环境下,高锰酸钾将Mn2+氧化为MnO2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上从海水中提取单质溴,其中有一种工艺采用如下方法:
(1)向海水中通入氯气将海水中的溴化物氧化,其离子方程式为:________ 。
(2)向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,这时,溴就转化成溴离子和溴酸根离子,其化学方程式为:____________ ;通入空气吹出Br2,并用Na2CO3吸收的目的是_________________ 。
(3)将(2)所得溶液用H2SO4酸化,又可得到单质溴,再用有机溶液萃取溴后,还可以得到副产品Na2SO4。 这一过程可用化学方程式表示为:___________ 。
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中加入________ (填字母)。
a.CCl4 b.NaBr溶液 c.NaOH溶液 d.Na2SO3溶液
(1)向海水中通入氯气将海水中的溴化物氧化,其离子方程式为:
(2)向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,这时,溴就转化成溴离子和溴酸根离子,其化学方程式为:
(3)将(2)所得溶液用H2SO4酸化,又可得到单质溴,再用有机溶液萃取溴后,还可以得到副产品Na2SO4。 这一过程可用化学方程式表示为:
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中加入
a.CCl4 b.NaBr溶液 c.NaOH溶液 d.Na2SO3溶液
您最近一年使用:0次



