解题方法
1 . 如图所示, 是固体金属单质,燃烧时火焰呈黄色,且生成物
是固体金属单质,燃烧时火焰呈黄色,且生成物 为淡黄色固体.回答下列问题:
为淡黄色固体.回答下列问题:
B____________ ,C____________ ,D____________ .
(2)写出下列转化反应的化学方程式或离子方程式:
①B→D:____________ (写化学方程式);
②A→C:____________ (写离子方程式):
③B→C:____________ (写离子方程式).
 是固体金属单质,燃烧时火焰呈黄色,且生成物
是固体金属单质,燃烧时火焰呈黄色,且生成物 为淡黄色固体.回答下列问题:
为淡黄色固体.回答下列问题: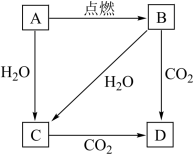
B
(2)写出下列转化反应的化学方程式或离子方程式:
①B→D:
②A→C:
③B→C:
您最近半年使用:0次
2 . 下列有关物质的性质与用途不具有对应关系的是
| A.干冰升华时吸热,可用作人工降雨 |
B. 吸收 吸收 产生 产生 ,可用作呼吸面具供氧剂 ,可用作呼吸面具供氧剂 |
C. 溶液显酸性,可蚀刻印刷电路板上的Cu 溶液显酸性,可蚀刻印刷电路板上的Cu |
D. 固体受热分解产生 固体受热分解产生 ,可用作膨松剂 ,可用作膨松剂 |
您最近半年使用:0次
名校
3 . 为保持航天器中气体成分恒定,需处理人体呼出气体。下表列出相关气体的成分及含量:
(1)上述气体组分中,N2不参与人体新陈代谢,若有100L空气被人体吸入,则相同条件下,人体呼出气体的体积为___________ L。(保留1位小数)(均为体积百分含量)
(2)设航天器内有100L空气被人体吸入,现将呼出的气体通过Na2O2处理,若Na2O2先与呼出的CO2反应,再与呼出的H2O(g)作用;试通过计算回答:欲使气体恢复至原空气成分且体积仍为100L,是否还需额外补充水蒸气。若需要,应补充多少升的水蒸气;若不需要,应使多少升的水蒸气冷凝。(计算过程保留3位小数)___________ 。
| 成分 | 人体吸入空气 | 人体呼出气体 |
| N2 | 78% | 74% |
| O2 | 21% | 16% |
| H2O(g) | 0.5% | 6% |
| CO2 | 0.03% | 4% |
(2)设航天器内有100L空气被人体吸入,现将呼出的气体通过Na2O2处理,若Na2O2先与呼出的CO2反应,再与呼出的H2O(g)作用;试通过计算回答:欲使气体恢复至原空气成分且体积仍为100L,是否还需额外补充水蒸气。若需要,应补充多少升的水蒸气;若不需要,应使多少升的水蒸气冷凝。(计算过程保留3位小数)
您最近半年使用:0次
名校
解题方法
4 . 2022年11月30日,神舟十五号载人飞船与空间站组合体成功交会对接。飞船的轨道舱内安装盛有Na2O2颗粒装置,为宇航员供氧。
(1)Na2O2中的正、负离子的个数比为___________ 。
(2)Na2O2与CO2发生反应的化学方程式为___________ ,该反应中体现了Na2O2的性质有___________ 。
(1)Na2O2中的正、负离子的个数比为
(2)Na2O2与CO2发生反应的化学方程式为
您最近半年使用:0次
解题方法
5 . 某化学兴趣小组对钠和钠的化合物进行了一系列的实验探究,请回答下列问题。
实验Ⅰ:探究二氧化碳与过氧化钠的反应是否有氧气生成,设计了如图所示的实验装置。_______ ,作用是_______ 。
(2)指出装置 中的错误之处:
中的错误之处:_______ 。
(3)取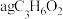 在氧气中完全燃烧,将其产物与足量
在氧气中完全燃烧,将其产物与足量 固体完全反应,反应后固体质量的增加量
固体完全反应,反应后固体质量的增加量_______ (填“大于”“等于”或“小于”) 。
。
实验Ⅱ:利用如图所示装置(省略夹持装置)模拟工业级 的制备。
的制备。 。
。
(4)装置 中盛放的药品为
中盛放的药品为_______ 。
(5)实验中使用油浴加热而不使用水浴加热的原因是_______ 。
(6)氨气与熔融钠反应生成 的化学方程式为
的化学方程式为_______ 。
实验Ⅰ:探究二氧化碳与过氧化钠的反应是否有氧气生成,设计了如图所示的实验装置。
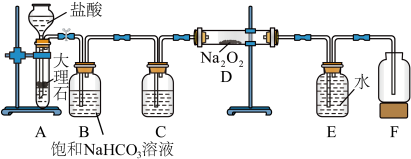
(2)指出装置
 中的错误之处:
中的错误之处:(3)取
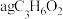 在氧气中完全燃烧,将其产物与足量
在氧气中完全燃烧,将其产物与足量 固体完全反应,反应后固体质量的增加量
固体完全反应,反应后固体质量的增加量 。
。实验Ⅱ:利用如图所示装置(省略夹持装置)模拟工业级
 的制备。
的制备。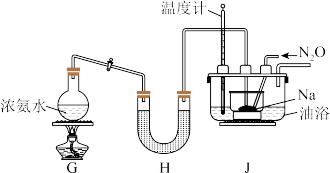
 。
。(4)装置
 中盛放的药品为
中盛放的药品为(5)实验中使用油浴加热而不使用水浴加热的原因是
(6)氨气与熔融钠反应生成
 的化学方程式为
的化学方程式为
您最近半年使用:0次
解题方法
6 . 过氧化钠可作为氧气的来源。常温常压下,二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物理量正确的是(NA表示阿伏加德罗常数的值)
| 二氧化碳 | 碳酸钠 | 转移的电子 | |
| A | 1mol | 2NA | |
| B | 22.4L | 1mol | |
| C | 106g | 1mol | |
| D | 106g | 2NA |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 下表中对各项化学事实解释不正确的是
| 选项 | 事实 | 解释 |
| A |  可为航天员供氧 可为航天员供氧 |  能与 能与 反应生成 反应生成 |
| B |  可用于治疗胃酸过多 可用于治疗胃酸过多 |  可与盐酸反应 可与盐酸反应 |
| C | 向滴有酚酞的水中加入一定量的 ,溶液变红色 ,溶液变红色 |  溶液呈碱性 溶液呈碱性 |
| D | 高压钠灯发出透雾性强的黄光 | 金属钠具有强还原性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_______ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
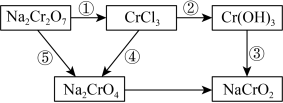
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是_______ (填序号,下同),发生还原反应的是_______ ,既没发生氧化反应又没发生还原反应的是_______ 。(提示:铬元素的化合价有+6、+3)_______ 。
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目_______ 。
②上述反应中氧化产物和还原产物的质量比为_______ 。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目
②上述反应中氧化产物和还原产物的质量比为
您最近半年使用:0次
名校
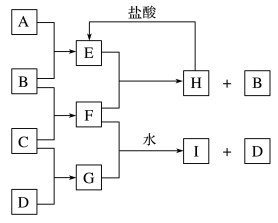
9 . A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组空气的成分。化合物F的焰色试验呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2,在一定条件下,各物质之间的相互转化关系如下图(图中部分产物未列出):
(1)A是___________ 。
(2)写出F和E反应的化学方程式___________ 。
(3)3.9克F与足量的E反应转移的电子数目为___________ 。
(4)在1L含1mol·L-1H的溶液中逐滴滴加1L0.75mol·L-1的 溶液生成标准状况下气体的体积是
溶液生成标准状况下气体的体积是___________ L(不考虑气体的溶解)
(5)F与G的水溶液反应生成I和D的离子方程式是___________ 。
(1)A是
(2)写出F和E反应的化学方程式
(3)3.9克F与足量的E反应转移的电子数目为
(4)在1L含1mol·L-1H的溶液中逐滴滴加1L0.75mol·L-1的
 溶液生成标准状况下气体的体积是
溶液生成标准状况下气体的体积是(5)F与G的水溶液反应生成I和D的离子方程式是
您最近半年使用:0次
解题方法
10 . 物质类别和元素价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:___________ ;通常将①的固体保存在___________ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式为___________ 。
(3)纯碱和小苏打都是重要的化工原料,根据下列三组实验,回答:___________ ;试管b中发生反应的离子方程式为___________ 。
②相比乙和丙而言,丙组能更便捷的验证两者的热稳定性,丙组实验中A处盛放的物质为___________ (填化学式)。

(2)写出淡黄色固体②与二氧化碳反应的化学方程式为
(3)纯碱和小苏打都是重要的化工原料,根据下列三组实验,回答:
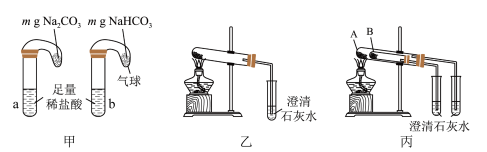
②相比乙和丙而言,丙组能更便捷的验证两者的热稳定性,丙组实验中A处盛放的物质为
您最近半年使用:0次



